题目内容
1.化学在生产和生活中有重要的应用,下列说法正确的是( )| A. | 新型材料聚酯纤维、光导纤维都属于有机高分子化合物 | |
| B. | 14C可用于文物年代的鉴定,14C与12C互为同素异形体 | |
| C. | 福尔马林可作食品的保鲜剂 | |
| D. | “开发利用新能源”、“汽车尾气催化净化”都能提高空气质量 |
分析 A.二氧化硅为无机物;
B.同素异形体是指由同种元素组成的不同单质;
C.食品添加剂包括酸度调节剂、抗结剂、消泡剂、抗氧化剂、漂白剂、膨松剂、着色剂、护色剂、酶制剂、增味剂、营养强化剂、防腐剂、甜味剂、增稠剂、香料等;
D.化石燃料燃烧能够产生大量污染污染物.
解答 解:A.光导纤维主要成分是二氧化硅,二氧化硅为无机物,不是有机高分子材料,故A错误;
B.14C与12C是碳元素的不同核素,不是单质,故B错误;
C.我国把营养强化剂也归为食品添加剂的范畴,包括对人体有益的某些氨基酸类,盐类,矿物质类,膳食纤维等,合理使用食品添加剂,对丰富食品生产,且对人体健康无害,可以食用,但不能过量,福尔马林有毒,不能作食品添加剂,故C错误;
D.“开发利用新能源”、“汽车尾气催化净化”能够减少化石燃料燃烧,有利于提高空气质量,故D正确;
故选D.
点评 本题考查了化学与生产和生活,涉及材料的分类、同素异形体概念、食品添加剂的应用、空气污染与治理,题目难度不大,注意对相关知识的积累.

练习册系列答案
相关题目
12.新版人民币的发行,引发了人们对有关人民币中化学知识的关注.下列表述不正确的是( )
| A. | 制造人民币所用的棉花、优质针叶木等原料的主要成分是纤维素 | |
| B. | 用于人民币票面文字等处的油墨中所含有的氧化铁是一种磁性物质 | |
| C. | 防伪荧光油墨由颜料与树脂连接料等制成,其中树脂属于有机高分子材料 | |
| D. | 某种验钞笔中含有碘酒溶液,遇假钞呈现蓝色,其中遇碘变蓝的是淀粉 |
12. 五种短周期元素的部分性质数据如下:
五种短周期元素的部分性质数据如下:
(1)Z离子的结构示意图为 .
.
(2)关于Y、Z两种元素,下列叙述正确的是b(填序号).
a.简单离子的半径 Y>Z
b.气态氢化物的稳定性Y比 Z强
c.最高价氧化物对应水化物的酸性Z比Y强
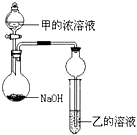
(3)甲是由T、X两种元素形成的10e-分子,乙是由Y、W两种元素形成的化合物.某同学设计了如图所示装置(夹持仪器省略)进行实验,将甲的浓溶液逐滴加入到NaOH固体中,烧瓶中即有甲放出,原因是氢氧化钠遇水放热,增大了OH-离子的浓度,有利于氨气的逸出.一段时间后,观察到试管中的现象是白色沉淀生成,发生反应的离子方程式是3NH3.H2O+Al3+=Al(OH)3↓+3NH4+.
(4)T、X两种元素形成XT5固体,它的所有原子的最外层都符合相应稀有气体原子的最外层结构,则其电子式为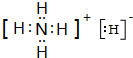 .
.
(5)XO2是导致光化学烟雾的“罪魁祸首”之一.它被氢氧化钠溶液吸收的化学方程式是:2XO2+2NaOH═M+NaXO3+H2O(已配平),产物M中元素X的化合价为+3.
(6)常温下,Z2Y2是一种橙黄色液体,广泛用于橡胶工业的硫化机,其分子结构与双氧水分子相似.试写出其结构式Cl-S-S-Cl.
 五种短周期元素的部分性质数据如下:
五种短周期元素的部分性质数据如下:| 元素 | T | X | Y | Z | W |
| 原子半径(nm) | 0.037 | 0.075 | 0.099 | 0.102 | 0.143 |
| 最高或最低化合价 | +1 | +5-3 | +7-1 | +6-2 | +3 |
 .
.(2)关于Y、Z两种元素,下列叙述正确的是b(填序号).
a.简单离子的半径 Y>Z
b.气态氢化物的稳定性Y比 Z强
c.最高价氧化物对应水化物的酸性Z比Y强
(3)甲是由T、X两种元素形成的10e-分子,乙是由Y、W两种元素形成的化合物.某同学设计了如图所示装置(夹持仪器省略)进行实验,将甲的浓溶液逐滴加入到NaOH固体中,烧瓶中即有甲放出,原因是氢氧化钠遇水放热,增大了OH-离子的浓度,有利于氨气的逸出.一段时间后,观察到试管中的现象是白色沉淀生成,发生反应的离子方程式是3NH3.H2O+Al3+=Al(OH)3↓+3NH4+.
(4)T、X两种元素形成XT5固体,它的所有原子的最外层都符合相应稀有气体原子的最外层结构,则其电子式为
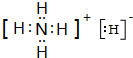 .
.(5)XO2是导致光化学烟雾的“罪魁祸首”之一.它被氢氧化钠溶液吸收的化学方程式是:2XO2+2NaOH═M+NaXO3+H2O(已配平),产物M中元素X的化合价为+3.
(6)常温下,Z2Y2是一种橙黄色液体,广泛用于橡胶工业的硫化机,其分子结构与双氧水分子相似.试写出其结构式Cl-S-S-Cl.
9.在多电子原子中,轨道能量是由以下哪些因素决定( )
①能层 ②能级 ③空间伸展方向 ④自旋状态.
①能层 ②能级 ③空间伸展方向 ④自旋状态.
| A. | ①② | B. | ①④ | C. | ②③ | D. | ③④ |
16.常温下,下列溶液的离子浓度关系式正确的是( )
| A. | 浓度相同的Na2CO3和NaHCO3混合溶液中,c(Na+)>c(CO32-)=c(HCO3-)>c(OH-)>c(H+) | |
| B. | 0.1mol/L①醋酸②氯化铵③硫酸溶液中,水电离产生的氢离子浓度大小顺序是②>①>③ | |
| C. | 0.1mol/L的NaHCO3溶液中 C(Na+)+c(H+)=c(OH-)+c(HCO3-) | |
| D. | pH相同的①CH3COONa②NaHCO3③NaClO三种溶液的c(Na+):③>②>① |
6.下列说法正确的是( )
| A. | $\frac{c(O{H}^{-})}{c({H}^{+})}$=1012的溶液中NH4+、Al3+、NO3-、Cl-可以共存 | |
| B. | 氧化镁可以用作耐火材料 | |
| C. | 淀粉和纤维素都可用(C6H10O5)n表示,二者互为同分异构体 | |
| D. | 浓氨水中滴加FeCl3饱和溶液可制得Fe(OH)3胶体 |
13.用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 25℃时,50 g 98%浓硫酸和50 g 98%浓磷酸混合后含氧原子数为4NA | |
| B. | 标准状况下,活泼金属与稀硫酸反应转移2NA个电子时,可产生22.4 L 气体 | |
| C. | 6.4g SO2溶于水配成1L溶液,含有H2SO3的分子数为0.1NA | |
| D. | 1 mol N2与足量H2反应生成NH3,有6NA个共价键生成 |
10.设NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A. | 100g 30% CH3COOH溶液中含氢原子数为2NA | |
| B. | 标准状况下,11.2 L CCl4中含有C-Cl键的数目为2NA | |
| C. | 16gO3和O2混合物中含氢原子数为NA | |
| D. | 精炼铜过程中阳极质量减少6.4g时,电路中转移电子数等于0.2NA |
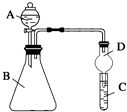 某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验.
某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验.