题目内容
人工合成化合物NH5 可改写成NH4H,能和水反应:NH5+H2O═NH3H2O+H2↑.下列说法正确的是( )
| A、NH5属于离子化合物,该反应中水做氧化剂 |
| B、该反应属于氧化还原反应,NH5既是氧化剂又是还原剂 |
| C、该反应不属于氧化还原反应,属于复分解反应 |
| D、标准状况下每生成22.4LH2时,转移2NA电子 |
考点:氧化还原反应
专题:氧化还原反应专题
分析:NH5所有原子的最外层都符合相应稀有气体原子的最外层电子层结构,即氮原子最外层达到8电子稳定结构,所有氢原子达到2电子稳定结构,所以,NH5是离子化合物氢化铵,与水反应生成一水合氨和氢气,只有H元素的化合价变化,以此来解答.
解答:
解:A.NH4H铵根离子与氢负离子以离子键结合,铵根离子中存在N-H键,含离子键的化合物一定为离子化合物,与水反应时,NH4H中H元素化合价由-1价升高到0价,被氧化,则水为氧化剂,NH4H为还原剂,故A正确;
B.H元素化合价发生变化,属于氧化还原反应,NH4H为还原剂,故B错误;
C.NH5与水的反应中,生成氢气,H元素的化合价变化,是氧化还原反应,故C错误;
D.标准状况下每生成22.4LH2时,即1mol时,只有1molNH4H参加反应,转移1NA电子,故D错误.
故选A.
B.H元素化合价发生变化,属于氧化还原反应,NH4H为还原剂,故B错误;
C.NH5与水的反应中,生成氢气,H元素的化合价变化,是氧化还原反应,故C错误;
D.标准状况下每生成22.4LH2时,即1mol时,只有1molNH4H参加反应,转移1NA电子,故D错误.
故选A.
点评:本题考查化学键和氧化还原反应,为高频考点,把握NH4H类似NH4Cl为解答的关键,注意与水反应生成一水合氨和氢气,题目难度不大.

练习册系列答案
相关题目
下列叙述正确的是( )
| A、1.00molNaCl中含有6.02×1023个NaCl分子 |
| B、欲配置1.00L1.00mol/L的NaCl溶液,可将58.5gNaCl溶于1.00L水中 |
| C、1molNO2和N2O4混合气体中含有原子总数为3NA |
| D、1molNa与足量的O2反应,生成Na2O和Na2O2的混合物,共转移NA个电子 |
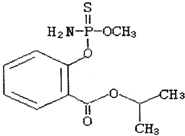 毒豇豆、毒黄瓜等毒蔬菜中含有禁用农药水胺硫磷,水胺硫磷的结构简式如图所示,对该化合物的叙述正确的是( )
毒豇豆、毒黄瓜等毒蔬菜中含有禁用农药水胺硫磷,水胺硫磷的结构简式如图所示,对该化合物的叙述正确的是( )| A、该化合物属于芳香烃 |
| B、该化合物中至少有7个碳原子在同一平面 |
| C、该化合物的分子式为C11H14O4NPS |
| D、该化合物能发生加聚反应、水解反应和酯化反应 |
下列最简式中,不需要知道对应物质的相对分子质量即可确定其分子式的是( )
| A、C3H4 |
| B、CH |
| C、CH2 |
| D、C2H5O |
下列各实验装置图与操作正确且能达到实验目的( )
A、 实验室干燥氯气 |
B、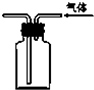 实验室收集SO2气体 |
C、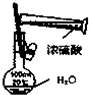 稀释浓硫酸 |
D、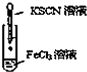 鉴定Fe3+ |
下列有机物命名正确的是( )
| A、H2N-CH2COOH 氨基乙酸 |
B、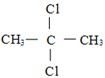 2-二氯丙烷 2-二氯丙烷 |
C、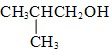 2-甲基丙醇 2-甲基丙醇 |
| D、C17H33COOH 硬脂酸 |
对于实验的描述正确的是( )
A、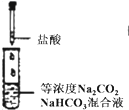 逐滴滴加稀盐酸时,试管中立即产生大量气泡 |
B、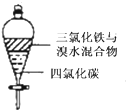 充分振荡后静置,下层溶液为橙红色,上层无色 |
C、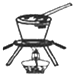 从饱和食盐水中提取NaCl晶体 |
D、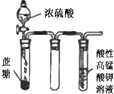 酸性KMnO4溶液中有气泡出现,且溶液颜色逐渐变浅乃至褪去 |