题目内容
4.下列有关叙述正确的是( )| A. | CCl4可用于鉴别溴水和碘水 | |
| B. | 甲苯(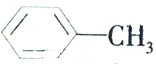 )中所有原子都在同一平面内 )中所有原子都在同一平面内 | |
| C. | 1mol甲苯含有6NA个C-H键 | |
| D. | 苯与甲苯互为同系物,均能使酸性KMnO4溶液褪色 |
分析 A.四氯化碳萃取溶液中的溴、碘,分别呈橙红色、紫红色;
B.含有甲基,具有四面体结构;
C.甲苯分子中含有8个C-H键;
D.苯不能使酸性高锰酸钾溶液褪色.
解答 解:A.四氯化碳萃取溶液中的溴、碘,分别呈橙红色、紫红色,现象不同,可以区别,故A正确;
B.含有甲基,具有四面体结构,所有原子不可能都在同一平面内,当碳原子都处于同一平面内,故B错误;
C.甲苯分子中含有8个C-H键,1mol甲苯含有8NA个C-H键,故C错误;
D.苯与甲苯属于同系物,甲苯可以使酸性高锰酸钾溶液褪色,但苯不能,故D错误,
故选:A.
点评 本题考查有机物的结构与性质、有机物的鉴别,难度不大,注意苯的同系物中连接苯环的碳原子上含有H原子的可以被酸性高锰酸钾溶液氧化.

练习册系列答案
相关题目
14.下列晶体熔化时不需破坏化学键的是( )
| A. | 晶体硅 | B. | 金刚石 | C. | 干冰 | D. | 二氧化硅 |
15.含苯酚的工业废水处理的流程图细下图所示,下列说法不确的是( )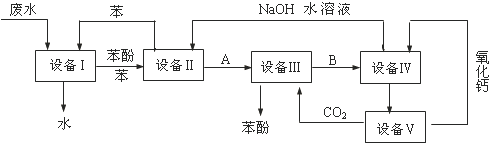

| A. | 上述流程里,设备Ⅰ、Ⅱ中进行的是分液操作;实验室里该操作可以用分液漏斗进行 | |
| B. | 上述流程里,设备Ⅲ、Ⅳ中进行的是过滤操作;实验室里该操作用到的玻璃仪器有:漏斗、烧杯、玻璃棒 | |
| C. | 在设备Ⅲ中发生反应的化学方程式为:C6H5ONa+CO2+H2O→C6H5OH+NaHCO3 | |
| D. | 图中循环使用的物质是C6H6、CaO、CO2和NaOH |
19.《后汉书•郡国志》中记载:“石出泉水…其水有肥,燃之极明,不可食,县人谓之石漆.”《酉阳杂俎》一书:“高奴县石脂水,水腻,浮上如漆,采以膏车及燃灯极明.”这里的“石漆”“石脂水”是指( )
| A. | 油脂 | B. | 油漆 | C. | 石油 | D. | 煤焦油 |
9.设NA代表阿伏加德罗常数,下列说法正确的是( )
| A. | 1.5mol单质Fe粉在足量氧气中完全燃烧,失去4NA个电子 | |
| B. | 在25g质量分数为60%的乙酸水溶液中,含有氢原子数为NA | |
| C. | 7.8 gNa2S和Na2O2 的混合物中,含有的阴离子数等于0.15NA | |
| D. | 在5×107Pa、500°C和铁触媒作用下,1molN2和3molH2可生成氨气分子数为2NA |
5.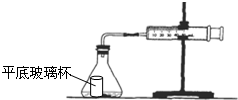 盐酸与碳酸钙反应生成CO2,运用如图,通过测量一定时间内产生CO2气体的体积,可测定该反应的速率.室温是29.5℃.请根据要求填空:
盐酸与碳酸钙反应生成CO2,运用如图,通过测量一定时间内产生CO2气体的体积,可测定该反应的速率.室温是29.5℃.请根据要求填空:
(1)检查装置的性能:组装好如图所示的装置后,用双手握住锥形瓶.观察现象.如果玻璃注射器中的活塞比较均匀地向外滑行,说明该装置的性能好,可用.
(2)在图中的锥形瓶中加入5g大理石,在平底玻璃杯中加入20mL1mol•L-1盐酸,并小心放于锥形瓶底,塞好带导管的塞子,玻璃注射器中的活塞归0.倾斜锥形瓶,使平底玻璃杯中的盐酸全部流到锥形瓶底部.每隔10s观测玻璃注射器中气体的体积,并填入表中:
(3)以mL•s-1为反应速率的单位,计算每10s时间间隔内的反应速率,将计算结果填入第23题表中:
(4)从第23题表中反应速率随时间变化的数据得到的结论是:本实验中反应速率随时间推移,先小后大最后又变小.
(5)以上结论的原因是:开始时,虽然盐酸浓度较大,但温度较低,反应速率较小;后来一段时间内,主要是碳酸钙跟盐酸反应放出热量,体系温度升高,速率较大;最后盐酸浓度明显减小,反应速率小,单位时间放出的热量少,加上散热使温度降低,速率变小.
 盐酸与碳酸钙反应生成CO2,运用如图,通过测量一定时间内产生CO2气体的体积,可测定该反应的速率.室温是29.5℃.请根据要求填空:
盐酸与碳酸钙反应生成CO2,运用如图,通过测量一定时间内产生CO2气体的体积,可测定该反应的速率.室温是29.5℃.请根据要求填空:(1)检查装置的性能:组装好如图所示的装置后,用双手握住锥形瓶.观察现象.如果玻璃注射器中的活塞比较均匀地向外滑行,说明该装置的性能好,可用.
(2)在图中的锥形瓶中加入5g大理石,在平底玻璃杯中加入20mL1mol•L-1盐酸,并小心放于锥形瓶底,塞好带导管的塞子,玻璃注射器中的活塞归0.倾斜锥形瓶,使平底玻璃杯中的盐酸全部流到锥形瓶底部.每隔10s观测玻璃注射器中气体的体积,并填入表中:
| 时间/s | 10 | 20 | 30 | 40 | 50 | 60 |
| 气体体积/mL | 4 | 14 | 25 | 38 | 47 | 55 |
| 反应速率/mL•s-1 | 0.4 | 1.0 | 1.1 | 1.3 | 0.9 | 0.8 |
(4)从第23题表中反应速率随时间变化的数据得到的结论是:本实验中反应速率随时间推移,先小后大最后又变小.
(5)以上结论的原因是:开始时,虽然盐酸浓度较大,但温度较低,反应速率较小;后来一段时间内,主要是碳酸钙跟盐酸反应放出热量,体系温度升高,速率较大;最后盐酸浓度明显减小,反应速率小,单位时间放出的热量少,加上散热使温度降低,速率变小.
2.判断下列元素中不属于主族元素的是( )
| A. | 铁 | B. | 钠 | C. | 磷 | D. | 氯 |
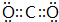 .D2A2中所含化学键类型为非极性共价键和离子键.
.D2A2中所含化学键类型为非极性共价键和离子键. .
.