题目内容
12.将乙醇和乙酸按照一定比例混合得到混合液A,取一定质量的该混合液A进行完全燃烧实验,生成CO2、H2O的质量如图所示.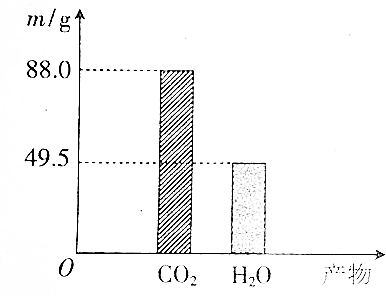
计算:
(1)混合液A中乙醇与乙酸的物质的量之比.
(2)198g混合液A在浓硫酸作催化剂的条件下发生酯化反应,乙酸乙酯的产率为60%,则生成的乙酸乙酯的质量是多?
分析 (1)设混合物中含有乙醇为xmol,乙酸为ymol,根据C2H5OH+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O,CH3COOH+2O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+2H2O计算;
(2)乙酸与乙醇反应的方程式为:CH3COOH+CH3CH2OH$?_{△}^{浓H_{2}SO_{4}}$CH3COOCH2CH3+H2O,根据乙酸和乙醇的质量关系判断反应的过量问题,根据不足的物质结合方程式计算.
解答 解:(1)设混合物中含有乙醇为xmol,乙酸为ymol,
C2H5OH+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2 +3H2O,
xmol 2xmol 3xmol
CH3COOH+2O2$\frac{\underline{\;点燃\;}}{\;}$2CO2 +2H2O;
ymol 2ymol 2ymol
则2x+2y=$\frac{88}{44}$,3x+2y=$\frac{49.5}{18}$,解得$\left\{\begin{array}{l}{x=0.75}\\{y=0.25}\end{array}\right.$,则乙醇与乙酸的物质的量之比0.75:0.25=3:1;
答:混合液A中乙醇与乙酸的物质的量之比为3:1;
(2)混合物中乙醇的质量分数为$\frac{3×46}{3×46+1×60}$=0.697,则198g混合液A中含有乙醇198×0.697=138,则乙酸为198-138=60g,已知混合物A中乙醇与乙酸的物质的量之比为3:1,乙醇过量,按照乙酸计算,
则CH3COOH+CH3CH2OH$?_{△}^{浓H_{2}SO_{4}}$CH3COOCH2CH3+H2O,
60 88
60g mg
则m=$\frac{60g×88}{60}$=88g,乙酸乙酯的产率为60%,则生成的乙酸乙酯的质量是88g×60%=52.8g;
答:生成的乙酸乙酯的质量是52.8g
点评 本题考查混合物的计算、化学方程式的计算,题目难度中等大,注意反应的理论产率的运用以及反应方程式的书写,侧重于考查学生的分析能力和计算能力.

 名校课堂系列答案
名校课堂系列答案| A. | 燃烧氧化法可以对有机物进行定性与定量的元素分析 | |
| B. | 提纯液体混合物常用重结晶法 | |
| C. | 红外光谱与核磁共振氢谱可以用于确定有机物的官能团和结构式 | |
| D. | 常用质谱法进行有机物相对分子质量的测定 |
| A. | X可能是金属元素 | |
| B. | 由X形成的含氧酸均为强酸 | |
| C. | X不能形成化学式为KXO4的含氧酸盐 | |
| D. | 元素X的气态氢化物一定极易溶于水 |
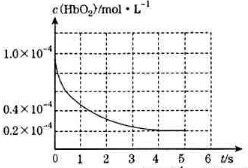 人体吸入CO后在肺部发生反应CO+HbO2?O2+HbCO导致人体缺氧.向某血样中通入CO与O2的混合气[c(CO)=1.0×10-4mol/L,c(O2)=9.9×10-4mol/L]氧合血红蛋白HbO2浓度随时间变化曲线如图所示,下列说法正确的是( )
人体吸入CO后在肺部发生反应CO+HbO2?O2+HbCO导致人体缺氧.向某血样中通入CO与O2的混合气[c(CO)=1.0×10-4mol/L,c(O2)=9.9×10-4mol/L]氧合血红蛋白HbO2浓度随时间变化曲线如图所示,下列说法正确的是( )| A. | 反应开始至4s内用HbO2表示的平均反应速率为2×10-4mol/(L•s) | |
| B. | 反应达平衡之前,O2与HbO2的反应速率逐渐减小 | |
| C. | 将CO中毒病人放入高压氧舱治疗是利用了化学平衡移动原理 | |
| D. | 该温度下反应CO+HbO2?O2+HbCO的平衡常数为107 |
| A. | CCl4可用于鉴别溴水和碘水 | |
| B. | 甲苯(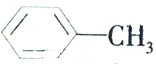 )中所有原子都在同一平面内 )中所有原子都在同一平面内 | |
| C. | 1mol甲苯含有6NA个C-H键 | |
| D. | 苯与甲苯互为同系物,均能使酸性KMnO4溶液褪色 |
 现有10种元素的性质、数据如下表所列,它们均为短周期元素.
现有10种元素的性质、数据如下表所列,它们均为短周期元素.| A | B | C | D | E | F | G | H | I | J | |
| 原子半径(10-10m) | 0.74 | 1.60 | 1.52 | 1.10 | 0.99 | 1.86 | 0.75 | 0.82 | 1.02 | 0.037 |
| 最高或最低 化合价 | +2 | +1 | +5 | +7 | +1 | +5 | +3 | +6 | +1 | |
| -2 | -3 | -1 | -3 | -2 |
(1)D的元素名称是磷,H的元素符号是B.
(2)在以上元素形成的最高价氧化物的水化物中,酸性最强的化合物的分子式是HClO4;化合物J2A2的电子式是:
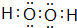 ,构成该物质的化学键类型有极性键和非极性键;画出A与B形成化合物的形成过程表示式:
,构成该物质的化学键类型有极性键和非极性键;画出A与B形成化合物的形成过程表示式: _.
_.(3)若将标况下E的单质3.36L与通入到100mL 2mol/L的FeBr2溶液中,反应的离子方程式3Cl2+4Fe2++2Br-=6Cl-+4Fe3++Br2
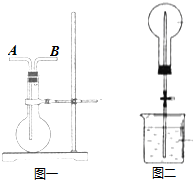
(4)G的氢化物是一种极易溶于水的气体.若用图1所示装置来收集此气体并完成喷泉实验,则气体应从图一的B口进入烧瓶(填字母).烧瓶内收集气体完成后,经测定瓶内气体的密度是相同条件下氢气密度的10.5倍,将此烧瓶按图二完成喷泉实验,请说明引发喷泉的方法用热毛巾将烧瓶捂热,NH3受热膨胀,赶出玻璃导管内的空气和水,NH3与水接触,即发生喷泉.实验完后液体将上升到容器容积的$\frac{2}{3}$.
(5)在Fe(GO3)2溶液中加入稀硫酸,溶液变成了黄色,有关反应的离子方程式为:3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O
(6)甲同学认为I的氧化物IO2与Na2O2反应类似于CO2与Na2O2的反应,该反应的化学方程式是2Na2O2+2SO2=2Na2SO3+O2.乙同学认为也有可能部分IO2被Na2O2氧化了,因此固体产物应该是混合物,为了检验是否有氧化产物生成,他们设计了如下方案:

上述方案是否合理?不合理.请简要说明两点理由:
①若反应后的固体中还残留有Na2O2,则溶于水后,残留的Na2O2会将SO32-氧化为SO42-;
②即使Na2O2已完全反应,加入的稀硝酸也能将BaSO3氧化为BaSO4.
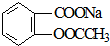 转变为
转变为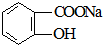 的方法为( )
的方法为( )| A. | 与足量NaOH溶液共热后,再通入CO2 | |
| B. | 与足量NaOH溶液共热后,再加入稀硫酸 | |
| C. | 与稀硫酸共热后,加入足量NaOH溶液 | |
| D. | 与足量稀硫酸共热后,加入足量Na2CO3 |