题目内容
2.下列叙述中错误的是( )| A. | 在合成氨工业中,加压有利于提高NH3的产率 | |
| B. | 直接燃烧煤不如将煤进行深加工后再燃烧的效率好 | |
| C. | 化石燃料包括石油、天然气、煤和氢能 | |
| D. | 在时间允许的情况下,从节能上分析,步行>坐公交>坐出租车 |
分析 A、合成氨反应是一个反应前后气体体积减小的可逆反应;
B、将煤进行深加工后,脱硫处理、气化处理很好地减少污染气体,提高燃烧效率,燃烧的效果好;
C、化石燃料包括石油、天然气、煤;
D、步行不消耗燃料,而公交载人多消耗能源少.
解答 解:A、合成氨反应是一个反应前后气体体积减小的可逆反应,增大压强,平衡向正反应方向移动,故A正确;
B、直接燃烧煤会排放出大量的有害气体灰尘等,将煤进行深加工后,脱硫处理、气化处理很好地减少污染气体,提高燃烧效率,燃烧的效果好,故B正确;
C、化石燃料包括石油、天然气、煤,不包括氢能,故C错误;
D、步行不消耗燃料,而公交载人多消耗能源少,所以从节能上分析,步行>坐公交>坐出租车,故D正确;
故选C.
点评 本题主要考查化石燃料的燃烧和防污染提效率的措施,比较基础,侧重对基础知识的巩固,注意对基础知识的理解掌握.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
13.常温常压下,下列各组离子在指定溶液中能大量共存的是( )
| A. | c(Fe3+)=0.1 mol/L溶液中:Na+、NH4+、SCN-、SO42- | |
| B. | 能溶解CaCO3的溶液中:Fe3+、Ca2+、Cl-、NO3- | |
| C. | 由水电离出的c(H+)=1×10-2mol/L的溶液中:Na+、Ba2+、HCO3-、Cl- | |
| D. | 强碱性溶液中:K+、Na+、ClO-、I- |
17.工业制硝酸过程中的一个重要反应为4NH3+5O2 $\frac{\underline{\;催化剂\;}}{△}$4NO+6H2O.下列有关该反应的说法不正确的是( )
| A. | O2是氧化剂 | B. | NH3是氧化剂 | C. | O2被还原 | D. | NH3发生氧化反应 |
7.用酸式滴定管准确移取10.00mL某未知浓度的盐酸溶于一洁净的锥形瓶中,然后用0.20mol•L -1的氢氧化钠溶液(指示剂为酚酞).滴定结果如下:
(1)根据以上数据可以计算出盐酸的物质的量浓度为0.364mol•L-1.
(2)达到滴定终点的标志是无色变为红色,且30s内不变色.
(3)以下操作造成测定结果偏高的原因可能是AD.
A.未用标准液润洗碱式滴定管
B.滴定终点读数时,俯视滴定管的刻度,其它操作均正确
C.盛装未知液的锥形瓶用蒸馏水洗过,未用待测液润洗
D.滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液.
| NaOH起始读数 | NaOH终点读数 | |
| 第一次 | 0.50mL | 18.60mL |
| 第二次 | 0.70mL | 19.00mL |
(2)达到滴定终点的标志是无色变为红色,且30s内不变色.
(3)以下操作造成测定结果偏高的原因可能是AD.
A.未用标准液润洗碱式滴定管
B.滴定终点读数时,俯视滴定管的刻度,其它操作均正确
C.盛装未知液的锥形瓶用蒸馏水洗过,未用待测液润洗
D.滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液.
14. 阅读分析下列材料:
阅读分析下列材料:
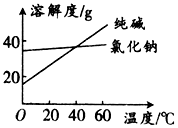
材料1:纯碱和氯化钠溶解度随温度变化的曲线图:
材料2:两种有机物的物理性质:
(1)将纯碱从氯化钠和纯碱的混合物中分离出来,合适的方法是C(填字母,下同);将乙二醇和丙三醇混合液相互分离的最佳方法是:蒸馏.
A、萃取 B、蒸馏 C、溶解、蒸发浓缩、冷却结晶、过滤 D、分液
(2)某纯碱样品中可能含有氯化钠,设计一个简易实验加以证明:取样品少许于试管中,加入蒸馏水溶解,加入硝酸酸化的硝酸银溶液.出现白色沉淀,证明含有氯化钠 (写出简要操作方法、现象和结论)
(3)某同学设计两套方案测定纯碱样品(含少量的氯化钠)中碳酸钠的质量分数.
方案1:取mg纯碱样品,加入过量的盐酸,充分反应后,蒸发、灼烧、称重得bg固体,计算出纯碱样品纯度.
方案2:取mg纯碱样品,溶于水加入过量的氯化钙溶液,过滤、洗涤、烘干、称重得ag固体,计算出纯碱样品纯度.
①写出方案1涉及的反应的化学方程式:Na2CO3+2HCl=2NaCl+H2O+CO2↑;
②利用方案2中的数据计算该纯碱的纯度:$\frac{53a}{50m}$×100%.
 阅读分析下列材料:
阅读分析下列材料:材料1:纯碱和氯化钠溶解度随温度变化的曲线图:
材料2:两种有机物的物理性质:
| 物质 | 熔点/℃ | 沸点/℃ | 密度/g•cm-3 | 溶解性 |
| 乙二醇 C2H6O2 | -11.5 | 198 | 1.11 | 易溶于水和乙醇及其他有机溶剂 |
| 丙三醇 C3H8O3 | 17.9 | 290 | 1.26 | 能跟水和酒精以任意比互溶;易溶于其他有机溶剂 |
A、萃取 B、蒸馏 C、溶解、蒸发浓缩、冷却结晶、过滤 D、分液
(2)某纯碱样品中可能含有氯化钠,设计一个简易实验加以证明:取样品少许于试管中,加入蒸馏水溶解,加入硝酸酸化的硝酸银溶液.出现白色沉淀,证明含有氯化钠 (写出简要操作方法、现象和结论)
(3)某同学设计两套方案测定纯碱样品(含少量的氯化钠)中碳酸钠的质量分数.
方案1:取mg纯碱样品,加入过量的盐酸,充分反应后,蒸发、灼烧、称重得bg固体,计算出纯碱样品纯度.
方案2:取mg纯碱样品,溶于水加入过量的氯化钙溶液,过滤、洗涤、烘干、称重得ag固体,计算出纯碱样品纯度.
①写出方案1涉及的反应的化学方程式:Na2CO3+2HCl=2NaCl+H2O+CO2↑;
②利用方案2中的数据计算该纯碱的纯度:$\frac{53a}{50m}$×100%.
5.利用所学化学知识回答问题
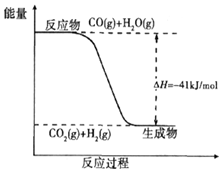
Ⅰ、甲醇是重要的化工原料,又可称为燃料.工业上利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主反应如下:
①CO(g)+2H2(g)═CH3OH(g)△H=?
②CO2(g)+3H2(g)═CH3OH(g)+H2O(g)△H=-58kJ/mol
③CO2(g)+H2(g)═CO(g)+H2O(g)△H=+41kJ/mol
回答下列问题:
(1)已知反应①中的相关的化学键键能数据如下:
则x=413kJ/mol.
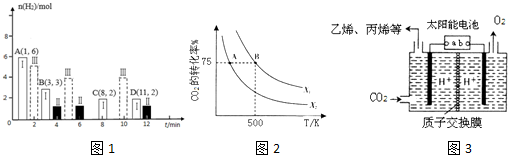
(2)若T℃时将6molCO2和8molH2充入2L密闭容器中发生反应②,测得H2的物质的量随时间变化如图1中状态Ⅰ(图1中实线)所示.图1中数据A(1,6)代表在1min时H2的物质的量是6mol.
①T℃时,状态Ⅰ条件下,平衡常数K=0.5;
②其他条件不变,仅改变温度时,测得H2的物质的量随时间变化如图中状态Ⅲ所示,则状态Ⅲ对应的温度>(填“>”“<”或“=”)T℃;
③一定温度下,此反应在恒容容器中进行,能判断该反应达到化学平衡状态依据的是bc.
a. 2个C=O断裂的同时有2个H-O生成 b.容器中混合气体平均摩尔质量不变
c.v逆(H2)=3v正(CH3OH) d.甲醇和水蒸气的体积比保持不变
Ⅱ、二氧化碳的回收利用是环保领域研究的热点课题.
(1)CO2经过催化氢化合成低碳烯烃.在2L恒容密闭容器中充入2moI CO2和nmol H2,在一定条件下发生反应:2C02(g)+6H2(g)?CH2=CH2(g)+4H20(g),△H=-128kJ/mol.CO2的转化率与温度、投料比[X=$\frac{n({H}_{2})}{n(C{O}_{2})}$]的关系如图2所示.
①X2> X1(填“>”、“<”或“=”)
②在500K时,若B点的投料比为3.5,且从反应开始到B点需要10min,则v(H2)=0.225mol/(L.min).
(2)以稀硫酸为电解质溶液,利用太阳能将CO2转化为低碳烯烃,工作原理图3如下,则左侧产生乙烯的电极反应式为2CO2+12e-+12H+=CH2=CH2+4H2O.

Ⅰ、甲醇是重要的化工原料,又可称为燃料.工业上利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主反应如下:
①CO(g)+2H2(g)═CH3OH(g)△H=?
②CO2(g)+3H2(g)═CH3OH(g)+H2O(g)△H=-58kJ/mol
③CO2(g)+H2(g)═CO(g)+H2O(g)△H=+41kJ/mol
回答下列问题:
(1)已知反应①中的相关的化学键键能数据如下:
| 化学键 | H-H | C-O | C $\frac{\underline{\;←\;}}{\;}$O | H-O | C-H |
| E/(kJ•mol-1) | 436 | 343 | 1076 | 465 | x |
(2)若T℃时将6molCO2和8molH2充入2L密闭容器中发生反应②,测得H2的物质的量随时间变化如图1中状态Ⅰ(图1中实线)所示.图1中数据A(1,6)代表在1min时H2的物质的量是6mol.
①T℃时,状态Ⅰ条件下,平衡常数K=0.5;
②其他条件不变,仅改变温度时,测得H2的物质的量随时间变化如图中状态Ⅲ所示,则状态Ⅲ对应的温度>(填“>”“<”或“=”)T℃;
③一定温度下,此反应在恒容容器中进行,能判断该反应达到化学平衡状态依据的是bc.
a. 2个C=O断裂的同时有2个H-O生成 b.容器中混合气体平均摩尔质量不变
c.v逆(H2)=3v正(CH3OH) d.甲醇和水蒸气的体积比保持不变
Ⅱ、二氧化碳的回收利用是环保领域研究的热点课题.
(1)CO2经过催化氢化合成低碳烯烃.在2L恒容密闭容器中充入2moI CO2和nmol H2,在一定条件下发生反应:2C02(g)+6H2(g)?CH2=CH2(g)+4H20(g),△H=-128kJ/mol.CO2的转化率与温度、投料比[X=$\frac{n({H}_{2})}{n(C{O}_{2})}$]的关系如图2所示.
①X2> X1(填“>”、“<”或“=”)
②在500K时,若B点的投料比为3.5,且从反应开始到B点需要10min,则v(H2)=0.225mol/(L.min).
(2)以稀硫酸为电解质溶液,利用太阳能将CO2转化为低碳烯烃,工作原理图3如下,则左侧产生乙烯的电极反应式为2CO2+12e-+12H+=CH2=CH2+4H2O.
 煤炭可以转化为清洁能源和化工原料.
煤炭可以转化为清洁能源和化工原料.