题目内容
19.下列说法不正确的是( )| A. | 甲烷和Cl2的反应与乙烯和Br2的反应属于同一类型的反应 | |
| B. | 28 g乙烯和环丁烷(C4H8)的混合气体中含有的碳原子数为2NA | |
| C. | 甲烷和氯气反应生成一氯甲烷与苯和硝酸反应生成硝基苯的反应类型相同 | |
| D. | 苯不能使溴的四氯化碳溶液褪色,说明苯分子中没有与乙烯分子中类似的碳碳双键 |
分析 A.甲烷和Cl2的反应为取代反应,乙烯和Br2的反应为加成反应;
B.乙烯和环丁烷(C4H8)最简式均为CH2,n(CH2)=$\frac{28g}{14g/mol}$=2mol;
C.反应中甲烷中H、苯中H被取代;
D.苯中不含双键.
解答 解:A.甲烷和Cl2的反应为取代反应,乙烯和Br2的反应为加成反应,反应类型不同,故A错误;
B.乙烯和环丁烷(C4H8)最简式均为CH2,n(CH2)=$\frac{28g}{14g/mol}$=2mol,则含有的碳原子数为2NA,故B正确;
C.反应中甲烷中H、苯中H被取代,则均为取代反应,故C正确;
D.苯中不含双键,则苯不能使溴的四氯化碳溶液褪色,故D正确;
故选A.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系、有机反应为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
相关题目
10. 现有五种元素,其中A、B、C、D、E为原子序数依次增大,且原子序数都不超过36.请根据下列相关信息,回答问题.
现有五种元素,其中A、B、C、D、E为原子序数依次增大,且原子序数都不超过36.请根据下列相关信息,回答问题.
(1)请把B以及B同周期且原子序数比B小的原子按第一电离能从大到小的顺序排列:Mg>Al>Na(用相应的元素符号表示).A、D两种元素中,电负性A>D (填“>”或“<”)
(2)A3分子的空间构型为V形,与其互为等电子体的分子为SO2;
(3)解释在水中的溶解度C7H15OH比乙醇低的原因是:乙醇中的羟基与水的羟基结构相似所以溶解度大,C7H15OH中烃基大,与水的羟基结构相似程度小所以溶解度小,C7H15OH 中采用sp3杂化的原子共有8个;
(4)【E(NH3)4】2+配离子中存在的化学键类型有①③(填序号):
①配位键 ②金属键 ③极性共价键 ④非极性共价键 ⑤离子键 ⑥氢键
若【E(NH3)4】2+具有对称的空间构型.且当【E(NH3)4】2+中的两个NH3分子被两个Cl-取代时.能得到两种不同结构的产物,则【E(NH3)4】2+的空间构型为a(填序号).
a.平面正方形b.正四面体 c.三角锥形 d.V形
(5)单质E晶胞如图所示,已知E元素相对原子质量为M,原子半径为r pm,密度为ρg/cm3(1pm=10-10cm)那么写出阿伏伽德罗常数NA的表达式${N_A}=\frac{{\sqrt{2}×{{10}^{30}}M}}{{8{r^3}ρ}}$.(用M、r、ρ表示)
 现有五种元素,其中A、B、C、D、E为原子序数依次增大,且原子序数都不超过36.请根据下列相关信息,回答问题.
现有五种元素,其中A、B、C、D、E为原子序数依次增大,且原子序数都不超过36.请根据下列相关信息,回答问题.| A | 基态原子最外层电子数是次外层的三倍 |
| B | 基态原子核外有13种不同运动状态的电子 |
| C | 与B同一周期,原子中未成对电子数是同周期中最多的 |
| D | D2-的核外电子排布与氩原子相同 |
| E | 是ds区原子序数最小的元素 |
(2)A3分子的空间构型为V形,与其互为等电子体的分子为SO2;
(3)解释在水中的溶解度C7H15OH比乙醇低的原因是:乙醇中的羟基与水的羟基结构相似所以溶解度大,C7H15OH中烃基大,与水的羟基结构相似程度小所以溶解度小,C7H15OH 中采用sp3杂化的原子共有8个;
(4)【E(NH3)4】2+配离子中存在的化学键类型有①③(填序号):
①配位键 ②金属键 ③极性共价键 ④非极性共价键 ⑤离子键 ⑥氢键
若【E(NH3)4】2+具有对称的空间构型.且当【E(NH3)4】2+中的两个NH3分子被两个Cl-取代时.能得到两种不同结构的产物,则【E(NH3)4】2+的空间构型为a(填序号).
a.平面正方形b.正四面体 c.三角锥形 d.V形
(5)单质E晶胞如图所示,已知E元素相对原子质量为M,原子半径为r pm,密度为ρg/cm3(1pm=10-10cm)那么写出阿伏伽德罗常数NA的表达式${N_A}=\frac{{\sqrt{2}×{{10}^{30}}M}}{{8{r^3}ρ}}$.(用M、r、ρ表示)
7.按下述实验方法制备气体,合理又实用的是( )
| A. | 锌粒与稀 HNO3反应制备 H2 | B. | 加热分解 NH4Cl 固体制 NH3 | ||
| C. | 大理石与稀 H2SO4反应制备 CO2 | D. | 亚硫酸钠与浓 H2SO4反应制备 SO2 |
14.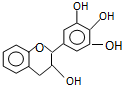 “茶倍健”牙膏中含有茶多酚,但茶多酚是目前尚不能人工合成的纯天然、多功能、高效的抗氧化剂和自由基净化剂.其中没食子儿茶素(EGC)的结构如图所示.关于EGC的下列叙述中不正确的是( )
“茶倍健”牙膏中含有茶多酚,但茶多酚是目前尚不能人工合成的纯天然、多功能、高效的抗氧化剂和自由基净化剂.其中没食子儿茶素(EGC)的结构如图所示.关于EGC的下列叙述中不正确的是( )
 “茶倍健”牙膏中含有茶多酚,但茶多酚是目前尚不能人工合成的纯天然、多功能、高效的抗氧化剂和自由基净化剂.其中没食子儿茶素(EGC)的结构如图所示.关于EGC的下列叙述中不正确的是( )
“茶倍健”牙膏中含有茶多酚,但茶多酚是目前尚不能人工合成的纯天然、多功能、高效的抗氧化剂和自由基净化剂.其中没食子儿茶素(EGC)的结构如图所示.关于EGC的下列叙述中不正确的是( )| A. | 分子中所有的原子共面 | B. | 1molEGC与3molNaOH恰好完全反应 | ||
| C. | 易发生氧化反应和取代反应 | D. | 遇FeCl3溶液发生显色反应 |
9.某有机化合物3.1g完全燃烧生成4.4g CO2和2.7gH2O,无其它物质生成.下列说法正确的是( )
| A. | 该化合物肯定含O元素 | B. | 该化合物属于烃 | ||
| C. | 该化合物的相对分子质量肯定为3l | D. | 该化合物的结构只有一种 |

 .
.
 .
. .
. 已知铜元素能形成多种化合物.
已知铜元素能形成多种化合物.