题目内容
4.有机物的结构可用“键线式”简化表示,有机物X的键线式为
(1)有机物Y是X的同分异构体,且属于芳香烃,写出Y的结构简式:
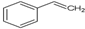 .
.(2)Y在一定条件下发生加聚反应,写出反应的化学方程式:
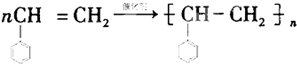 .
.(3)X与足量的H2在一定条件下反应可生成环状的饱和烃Z,Z的一氯代物有2种.
分析 (1)由有机物X的键线式为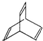 可知,X的分子式为C8H8,其不饱和度为$\frac{8×2+2-8}{2}$=5,一个苯环的不饱和度是4,有机物Y是X的同分异构体,所以属于芳香烃的Y中除了有一个苯环外还有一个碳碳双键,据此可写出结构简式;
可知,X的分子式为C8H8,其不饱和度为$\frac{8×2+2-8}{2}$=5,一个苯环的不饱和度是4,有机物Y是X的同分异构体,所以属于芳香烃的Y中除了有一个苯环外还有一个碳碳双键,据此可写出结构简式;
(2)含碳碳双键,可发生加聚反应;
(3) 与足量的H2在一定条件下反应可生成环状的饱和烃为
与足量的H2在一定条件下反应可生成环状的饱和烃为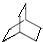 ,据此写它的一氯代物的结构简式.
,据此写它的一氯代物的结构简式.
解答 解:(1)由有机物X的键线式为 可知,X的分子式为C8H8,其不饱和度为$\frac{8×2+2-8}{2}$=5,一个苯环的不饱和度是4,有机物Y是X的同分异构体,所以属于芳香烃的Y中除了有一个苯环外还有一个碳碳双键,所以Y的结构简式为
可知,X的分子式为C8H8,其不饱和度为$\frac{8×2+2-8}{2}$=5,一个苯环的不饱和度是4,有机物Y是X的同分异构体,所以属于芳香烃的Y中除了有一个苯环外还有一个碳碳双键,所以Y的结构简式为 ,
,
故答案为: ;
;
(2)苯乙烯在引发剂作用下发生加成反应生成聚苯乙烯,发生的是加聚反应,反应的化学方程式为 ,
,
故答案为: ;
;
(3) 与足量的H2在一定条件下反应可生成环状的饱和烃为
与足量的H2在一定条件下反应可生成环状的饱和烃为 ,它的一氯代物有
,它的一氯代物有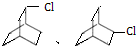 ,共2种,
,共2种,
故答案为:2.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系、有机物的结构对称性为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
相关题目
14.已知(NH4)2SO4在高温下分解,产物是SO2、H2O、N2和NH3.有关该反应的下列说法正确的是( )
| A. | N2既是氧化产物又是还原产物 | |
| B. | NH4+部分被氧化 | |
| C. | 氧化产物和还原产物的物质的量比为3:1 | |
| D. | 氧化产物和还原产物的物质的量比为1:4 |
15.一种微生物燃料电池如图所示,下列关于该电池的说法正确的是( )

| A. | b电极反应式为2NO3-+10e-+12H+=N2↑+6H2O | |
| B. | a电极发生还原反应 | |
| C. | H+由右室通过质子交换膜进入左室 | |
| D. | 电池工作时,电流由a电极沿导线流向b电极 |
12.下列说法中正确的是( )
| A. | 苯酚俗称石炭酸,酸性比碳酸强 | |
| B. | 能发生银镜反应的有机物都是醛 | |
| C. | 含有羟基的有机物称为醇 | |
| D. | 酯在碱性条件下的水解程度大于酸性条件下的水解程度 |
19.下列说法不正确的是( )
| A. | 甲烷和Cl2的反应与乙烯和Br2的反应属于同一类型的反应 | |
| B. | 28 g乙烯和环丁烷(C4H8)的混合气体中含有的碳原子数为2NA | |
| C. | 甲烷和氯气反应生成一氯甲烷与苯和硝酸反应生成硝基苯的反应类型相同 | |
| D. | 苯不能使溴的四氯化碳溶液褪色,说明苯分子中没有与乙烯分子中类似的碳碳双键 |
16.等质量的下列烃分别完全燃烧,消耗氧气最少的是( )
| A. | 乙烷 | B. | 丙烯 | C. | 丁炔 | D. | 甲苯 |
13.用质量均为100g的铜棒作电极,电解硝酸银溶液,电解一段时间后,两个电极的质量差为28g,则阴极的质量为( )
| A. | 128 g | B. | 114 g | C. | 119 g | D. | 121.6 g |
14.标准状况下,将5.6L由CO、CH4、C2H4、C2H2组成的混合气体与18L O2混合于某密闭容器中点燃,反应完成后再恢复到原状况,得CO2气体7.50L,则下列判断正确的是( )
| A. | 原混合气体中CO与CH4的体积分数和为33.9% | |
| B. | 原混合气体中,C2H4与C2H2的体积共为1.9L | |
| C. | 反应完成后,生成水的质量为9g | |
| D. | 原混合气体中,CO与CH4的体积比一定为1:1 |