题目内容
9.某有机化合物3.1g完全燃烧生成4.4g CO2和2.7gH2O,无其它物质生成.下列说法正确的是( )| A. | 该化合物肯定含O元素 | B. | 该化合物属于烃 | ||
| C. | 该化合物的相对分子质量肯定为3l | D. | 该化合物的结构只有一种 |
分析 根据n=$\frac{m}{M}$计算4.4g CO2和2.7g H2O的物质的量,计算C、H元素的质量,根据质量守恒定律判断该化合物中是否含有氧元素,再根据原子守恒确定该化合物最简式,以此解答该题.
解答 解:4.4g CO2的物质的量=$\frac{4.4g}{44g/mol}$=0.1mol,n(C)=0.1mol,m(C)=0.1mol×12g/mol=1.2g,
2.7g H2O的物质的量=$\frac{2.7g}{18g/mol}$=0.15mol,n(H)=0.3mol,m(H)=0.3mol×1g/mol=0.3g,
由于m(C)+m(H)=1.2g+0.3g=1.5g<3.1g,故该化合物中还含有氧元素,m(O)=3.1g-1.5g=1.6g,n(O)=$\frac{1.6g}{16g/mol}$=0.1mol,
则n(C):n(H):n(O)=0.1mol:0.3mol:0.1mol=1:3:1,即该有机物最简式为CH3O,有机物中H原子数目一定为偶数,2个C原子最多需要6个H原子饱和,故该有机物的分子式为C2H6O2,相对分子质量为62,其结构简式可能为HOCH2CH2OH、HOCH2OCH3等,
综上所述,选项中A正确,BCD错误,
故选A.
点评 本题考查有机物组成的判断,为高频考点,侧重考查学生的分析能力和计算能力,注意质量守恒定律的运用,比较基础,注意利用最简式不一定能确定有机物的组成.

练习册系列答案
 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案
相关题目
19.下列说法不正确的是( )
| A. | 甲烷和Cl2的反应与乙烯和Br2的反应属于同一类型的反应 | |
| B. | 28 g乙烯和环丁烷(C4H8)的混合气体中含有的碳原子数为2NA | |
| C. | 甲烷和氯气反应生成一氯甲烷与苯和硝酸反应生成硝基苯的反应类型相同 | |
| D. | 苯不能使溴的四氯化碳溶液褪色,说明苯分子中没有与乙烯分子中类似的碳碳双键 |
17.下列实验装置图(有些图中部分夹持仪器未画出)能达到其实验目的是( )
| A. | 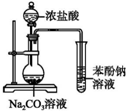 证明酸性:盐酸>碳酸>苯酚 | B. |  溴水褪色一定产生了乙烯 | ||
| C. |  分离溴乙烷和水 | D. | 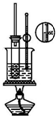 实验室制取硝基苯 |
14.标准状况下,将5.6L由CO、CH4、C2H4、C2H2组成的混合气体与18L O2混合于某密闭容器中点燃,反应完成后再恢复到原状况,得CO2气体7.50L,则下列判断正确的是( )
| A. | 原混合气体中CO与CH4的体积分数和为33.9% | |
| B. | 原混合气体中,C2H4与C2H2的体积共为1.9L | |
| C. | 反应完成后,生成水的质量为9g | |
| D. | 原混合气体中,CO与CH4的体积比一定为1:1 |
1.A、B、C、D、E是同周期元素,A、B的最高价氧化物的水化物呈碱性,且B比A的碱性强,C、D最高价氧化物水化物是酸,且C比D的酸性强,E是这五种元素中离子半径最小的,则它们的原子序数由小到大的顺序是( )
| A. | E、C、D、B、A | B. | B、A、E、D、C | C. | E、B、A、D、C | D. | A、B、C、D、E |
18.用惰性电极和相同电量分别电解①HCl ②KNO3 ③CuCl2 ④CuSO4四种电解质溶液,在理论上生成气体的总体积(同温同压下)由多到少的顺序是( )
| A. | ④③②① | B. | ①②③④ | C. | ④②①③ | D. | ③④①② |