题目内容
16.利用太阳能分解水制氢,若光解0.02mol水,下列说法正确的是( )| A. | 可生成H2的质量为0.02g | |
| B. | 可生成氢的原子数为2.408×1023个 | |
| C. | 可生成H2的体积为0.224L(标准情况) | |
| D. | 生成H2的量理论上等于0.04mol Na与水反应产生H2的量 |
分析 根据方程式2H2O=2H2↑+O2↑,光解0.02 mol水,可产生0.02 mol H2和0.01 mol O2,结合n=$\frac{m}{M}$=$\frac{V}{{V}_{m}}$=$\frac{N}{{N}_{A}}$结合物质的构成解答该题.
解答 解:根据方程式2H2O=2H2↑+O2↑,光解0.02 mol水,可产生0.02 mol H2和0.01 mol O2.则可得:
A.可生成H2的质量为0.02mol×2g/mol=0.04g,故A错误;
B.可生成氢的原子数为0.02mol×2×6.02×1023/mol=2.408×1022个,故B错误;
C.可生成标准状况下H2的体积为0.02mol×22.4L/mol=0.448L,故C错误;
D.钠与水发生2Na+2H2O=2NaOH+H2↑,则0.04mol Na与水反应产生0.02 molH2,故D正确.
故选D.
点评 本题考查物质的量的计算,侧重于学生的分析、计算能力的考查,本题为2016年海南高考题,难度不大,注意把握相关物理量的计算公式的运用以及物质的构成特点,把握相关反应,难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
7.CPAE是蜂胶的主要活性成分,也可由咖啡酸合成:
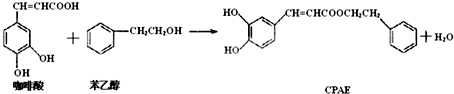
下列说法正确的是( )

下列说法正确的是( )
| A. | 咖啡酸分子中所有原子可能处在同一个平面上 | |
| B. | 通常条件下,咖啡酸和苯乙醇都能发生取代、加成、消去、氧化反应 | |
| C. | 1molCPAE与H2反应,最多可消耗8molH2 | |
| D. | 可用FeCl3溶液检测上述反应是否有CPAE生成 |
11.下列叙述错误的是( )
| A. | 氦气可用于填充飞艇 | B. | 氯化铁可用于硬水的软化 | ||
| C. | 石英砂可用于生产单晶硅 | D. | 聚四氟乙烯可用于厨具表面涂层 |
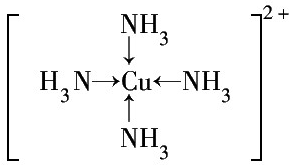 .
. (R为烃基).其中一种辣椒素酯类化合物J的合成路线如下:
(R为烃基).其中一种辣椒素酯类化合物J的合成路线如下:

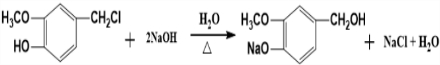 .
. .
.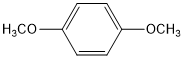 (写结构简式).
(写结构简式).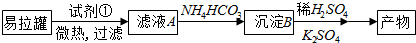
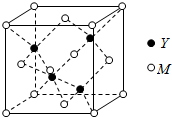 M是第四周期元素,最外层只有1个电子,次外层的所有原子轨道均充满电子.元素Y的负一价离子的最外层电子数与次外层的相同.回答下列问题:
M是第四周期元素,最外层只有1个电子,次外层的所有原子轨道均充满电子.元素Y的负一价离子的最外层电子数与次外层的相同.回答下列问题: