题目内容
4.下列各组中物质用酸性高锰酸钾或溴水均能鉴别的是( )| A. | 乙酸乙酯、裂化汽油、溴苯、福尔马林 | |
| B. | 乙醇、乙酸、乙醛、乙苯 | |
| C. | 苯甲酸溶液、甘油、甲苯、甲酸 | |
| D. | 苯酚、苯乙烯、苯、1,2-二溴乙烷 |
分析 用高锰酸钾酸性溶液和溴水,其中一种物质应含有C=C,可被高锰酸钾氧化,与溴水发生加成反应,以此解答该题.
解答 解:A.裂化汽油、福尔马林均能使溴水、高锰酸钾褪色,不能鉴别,故A不选;
B.乙醇、乙酸均与溴水不反应,乙醇、乙醛、乙苯均使高锰酸钾褪色,不能鉴别,故B不选
C.苯甲酸溶液、甘油、甲酸均与溴水、高锰酸钾不反应,不能鉴别,故C不选;
D.苯酚、苯乙烯、苯、1,2-二溴乙烷分别与溴水混合的现象为:白色沉淀、溴水褪色、分层后有机层在上层、分层后有机层在下层,故D选;
故选D.
点评 本题考查有机物的鉴别,为高频考点,本题注意有机物的官能团的性质,根据物质的性质的异同进行鉴别,题目难度不大.

练习册系列答案
相关题目
12.关于铅蓄电池 Pb+PbO2+2H2SO4 $?_{充电}^{放电}$ 2PbSO4+2H2O 的说法正确的是( )
| A. | 放电时,正极发生的反应是 Pb+SO4+2e═PbSO4 | |
| B. | 放电时,该电池的负极材料是铅板 | |
| C. | 放电时,电池中硫酸的浓度不断变大 | |
| D. | 放电时,每当消耗 1 mol 铅时转移电子 4 mol |
19.在高温下,碘是紫红色蒸气,氢气、碘化氢是无色气体,在某容器中H2+I2?2HI+Q(高温)可逆反应达到平衡,请填写完整表.
| 改变条件 | 平衡移动方向 | 体系内混合气体的颜色变化 |
| (1)加入氢气 | 正反应方向 | 变浅 |
| (2)升高温度 | 逆反应方向 | 变深 |
| (3)加入碘 | 正反应方向 | 变深 |
| (4)使容器的容积压缩到原来的一半 | 不移动 | 变深 |
2.某课外活动小组的同学进行探究银氨溶液温度对丙醛的银镜反应生成速率的影响.实验操作步骤简述如下:
1.准备好实验药品;2.准备好实验仪器;3.配制银氨溶液;4.进行银氨溶液温度对丙醛的银镜反应生成速率的影响探究实验.
请回答下列问题:
(1)丙醛发生银镜反应的化学方程式为:CH3CH2CHO+2Ag(NH3)2OHCH3CH2COONH4+2Ag↓+3NH3+H2O.
(2)银镜反应选择的加热方法是乙(填下列装置编号).
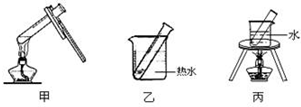
(3)该兴趣小组的同学探究银氨溶液的温度对丙醛的银镜反应生成速率的影响.参照下表格,在实验前拟定好实验记录表格,完整体现实验方案(只列出需记录物理量和单位,不用填写实验数据):
(4)实验完清洗试管内壁附着的银镜方法是:先用稀HNO3溶解,然后再用水清洗
(5)你认为探究丙醛进行银镜反应的最佳条件,除了测定银镜出现的时间外,还需要比较不同条件下形成的银镜的光亮程度.
1.准备好实验药品;2.准备好实验仪器;3.配制银氨溶液;4.进行银氨溶液温度对丙醛的银镜反应生成速率的影响探究实验.
请回答下列问题:
(1)丙醛发生银镜反应的化学方程式为:CH3CH2CHO+2Ag(NH3)2OHCH3CH2COONH4+2Ag↓+3NH3+H2O.
(2)银镜反应选择的加热方法是乙(填下列装置编号).

(3)该兴趣小组的同学探究银氨溶液的温度对丙醛的银镜反应生成速率的影响.参照下表格,在实验前拟定好实验记录表格,完整体现实验方案(只列出需记录物理量和单位,不用填写实验数据):
| 实验变量 实验序号 | 银氨溶液的量/mL | |||
| 1 | ||||
| 2 |
(5)你认为探究丙醛进行银镜反应的最佳条件,除了测定银镜出现的时间外,还需要比较不同条件下形成的银镜的光亮程度.
20.钠及其化合物具有广泛的用途.
(1)常温下,浓度均为0.1mol•L-1的下列五种钠盐溶液的pH如表;
上述盐溶液中,结合H+能力最强的阴离子是CO32-,根据表中数据,浓度均为0.01mol•L-1的下列四种酸的溶液分别稀释100倍,pH变化最大的是C(填编号).
A.HCN B.HClO C.CH3COOH D.H2CO3
(2)实验室中常用NaOH来进行洗气和提纯.
①当300mL 1mol•L-1的NaOH溶液吸收标准状况下4.48LCO2时,所得溶液中各离子浓度由大到小的顺序为C(Na+)>C(HCO3-)>C(CO32-)>C(OH-)>C(H+).
②几种离子开始沉淀时的pH如表:
当向含相同浓度Cu2+、Mg2+、Fe2+离子的溶液中滴加NaOH溶液时,Cu2+(填离子符号)先沉淀,KSP[Fe(OH)2]<KSP[Mg(OH)2](填“>”、“=”或“<”).
(1)常温下,浓度均为0.1mol•L-1的下列五种钠盐溶液的pH如表;
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
A.HCN B.HClO C.CH3COOH D.H2CO3
(2)实验室中常用NaOH来进行洗气和提纯.
①当300mL 1mol•L-1的NaOH溶液吸收标准状况下4.48LCO2时,所得溶液中各离子浓度由大到小的顺序为C(Na+)>C(HCO3-)>C(CO32-)>C(OH-)>C(H+).
②几种离子开始沉淀时的pH如表:
| 离子 | Fe2+ | Cu2+ | Mg2+ |
| pH | 7.6 | 5.2 | 10.4 |

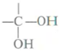 $\stackrel{自动脱水}{→}$
$\stackrel{自动脱水}{→}$
 .
.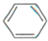 +
+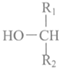 $\stackrel{酶}{→}$
$\stackrel{酶}{→}$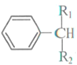 +H2O则可推知反应②发生时,会得到一种副产物,写出该副产物的结构简式
+H2O则可推知反应②发生时,会得到一种副产物,写出该副产物的结构简式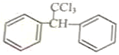 .
.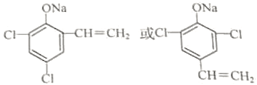 (任写一种)
(任写一种)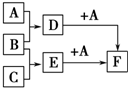 已知A、B、C是三种常见的单质,其中A为固体,B、C为气体;D的饱和溶液滴入沸水中继续煮沸,溶液呈红褐色;B和C反应的产物极易溶于水得无色溶液E.它们之间转化关系如图所示.
已知A、B、C是三种常见的单质,其中A为固体,B、C为气体;D的饱和溶液滴入沸水中继续煮沸,溶液呈红褐色;B和C反应的产物极易溶于水得无色溶液E.它们之间转化关系如图所示.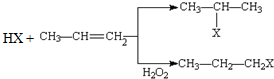 (X为卤素原子)
(X为卤素原子)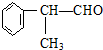 的物质,该物质是一种香料.
的物质,该物质是一种香料.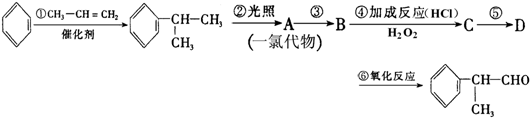
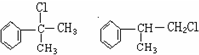 ;
;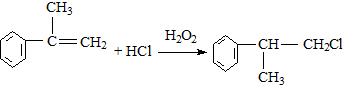 ;
;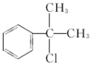 的水解产物
的水解产物 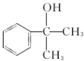 ,不能被氧化生成D,若直接转化为D则会降低D的产率与纯度;
,不能被氧化生成D,若直接转化为D则会降低D的产率与纯度; 等任意一种.
等任意一种.