题目内容
2.某课外活动小组的同学进行探究银氨溶液温度对丙醛的银镜反应生成速率的影响.实验操作步骤简述如下:1.准备好实验药品;2.准备好实验仪器;3.配制银氨溶液;4.进行银氨溶液温度对丙醛的银镜反应生成速率的影响探究实验.
请回答下列问题:
(1)丙醛发生银镜反应的化学方程式为:CH3CH2CHO+2Ag(NH3)2OHCH3CH2COONH4+2Ag↓+3NH3+H2O.
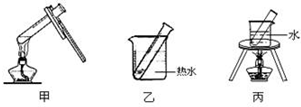
(2)银镜反应选择的加热方法是乙(填下列装置编号).
(3)该兴趣小组的同学探究银氨溶液的温度对丙醛的银镜反应生成速率的影响.参照下表格,在实验前拟定好实验记录表格,完整体现实验方案(只列出需记录物理量和单位,不用填写实验数据):
| 实验变量 实验序号 | 银氨溶液的量/mL | |||
| 1 | ||||
| 2 |
(5)你认为探究丙醛进行银镜反应的最佳条件,除了测定银镜出现的时间外,还需要比较不同条件下形成的银镜的光亮程度.
分析 (1)银镜反应的方程式书写,只有-CHO和2molAg(NH3)2OH反应,配平方法:1mol-CHO和2molAg(NH3)2OH反应;
(2)根据影响银镜产生的效果角度分析,为了受热均匀,采用热水浴加热;
(3)根据单一变量研究方法,保证温度为变量,其它量相同;
(4)用稀硝酸除去银,再用水清洗;
(5)银镜的光亮程度与反应条件有关.
解答 解:(1)银镜反应的方程式书写,只有-CHO和2molAg(NH3)2OH反应,其它结构不变;配平方法:1mol-CHO和2molAg(NH3)2OH反应,反应的方程式为CH3CHO+2Ag(NH3)2OH$\stackrel{水浴}{→}$CH3COONH4+2Ag↓+3NH3+H2O,
故答案为:CH3CHO+2Ag(NH3)2OH$\stackrel{水浴}{→}$CH3COONH4+2Ag↓+3NH3+H2O;
(2)加热时试管抖动或试管中液体沸腾都将影响银镜产生的效果,为了受热均匀,采用热水浴加热,装置乙符合要求,
故答案为:乙;
(3)究银氨溶液的温度对丙醛的银镜反应生成速率的影响,只能将温度定位变量,故答案为:
| 实验变量 实验序号 | 丙醛的量/滴 | 温度 /℃ | 出现银镜的时间/min | |
| 1 | ||||
| 2 |
(5)银镜反应实验如果条件控制适当,析出的银会均匀地分布在试管壁上,形成光亮的银镜,银镜的光亮程度与反应条件有关,故答案为:光亮程度.
点评 本题考查乙醛的银镜反应,侧重于除油污、保证银镜的生成、化学方程式的书写、乙醛进行银镜反应的最佳实验条件探究,银氨溶液废液的处理等,题目难度中等,注意银镜反应实验成功的关键因素.对比实验、银镜反应的实验条件、各条件对反应速率的影响.

练习册系列答案
 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案
相关题目
6.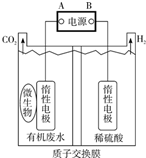 在微生物作用下,电解有机废水(含CH3COOH),实现废水处理的同时,可获得清洁能源H2.其原理如图所示.下列有关说法正确的是( )
在微生物作用下,电解有机废水(含CH3COOH),实现废水处理的同时,可获得清洁能源H2.其原理如图所示.下列有关说法正确的是( )
 在微生物作用下,电解有机废水(含CH3COOH),实现废水处理的同时,可获得清洁能源H2.其原理如图所示.下列有关说法正确的是( )
在微生物作用下,电解有机废水(含CH3COOH),实现废水处理的同时,可获得清洁能源H2.其原理如图所示.下列有关说法正确的是( )| A. | 电极A为负极 | |
| B. | 电解中生成的CO2与H2物质的量之比为1:1 | |
| C. | 阳极反应为:CH3COOH一8e-+8OH-═2CO2↑+6H2O | |
| D. | 电解前后,阴极室的pH几乎保持不变 |
7.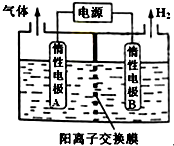 利用LiOH可制备锂离子电池正极材料.LiOH可由电解法制备,如图,两极区电解质溶液分别为LiOH和LiCl溶液.下列说法错误的是( )
利用LiOH可制备锂离子电池正极材料.LiOH可由电解法制备,如图,两极区电解质溶液分别为LiOH和LiCl溶液.下列说法错误的是( )
 利用LiOH可制备锂离子电池正极材料.LiOH可由电解法制备,如图,两极区电解质溶液分别为LiOH和LiCl溶液.下列说法错误的是( )
利用LiOH可制备锂离子电池正极材料.LiOH可由电解法制备,如图,两极区电解质溶液分别为LiOH和LiCl溶液.下列说法错误的是( )| A. | B极区电解质溶液为LiOH溶液 | |
| B. | 阳极电极反应式为2Cl--2e-═Cl2↑ | |
| C. | 电解过程中主要是H+通过阳离子交换膜向B电极迁移 | |
| D. | 电极A连接电源的正极 |
4.下列各组中物质用酸性高锰酸钾或溴水均能鉴别的是( )
| A. | 乙酸乙酯、裂化汽油、溴苯、福尔马林 | |
| B. | 乙醇、乙酸、乙醛、乙苯 | |
| C. | 苯甲酸溶液、甘油、甲苯、甲酸 | |
| D. | 苯酚、苯乙烯、苯、1,2-二溴乙烷 |
11.等质量下列物质与足量稀硝酸反应,放出NO物质的量最多的是( )
| A. | Fe2O3 | B. | FeSO4 | C. | Cu | D. | CuO |
14.下列物质的转化在给定条件下能实现的是( )
| A. | NaCl(aq)$\stackrel{CO_{2}}{→}$NaHCO3(s)$\stackrel{△}{→}$Na2CO3(s) | B. | CuCl2$\stackrel{NaOH(aq)}{→}$Cu(OH)2$→_{△}^{葡萄糖}$Cu | ||
| C. | Al$\stackrel{NaOH(aq)}{→}$NaAlO2(aq)$\stackrel{△}{→}$NaAlO2(s) | D. | MgO(s)$\stackrel{HNO_{3}(aq)}{→}$Mg(NO3)2(aq)$\stackrel{电解}{→}$Mg(s) |
11.已知X、Y、Z三元素原子电子层数相同,X元素最高价氧化物的水化物是强碱,Y元素的最高价氧化物的水化物具有两性,Z元素的最高价氧化物的水化物是一种强酸,则X、Y、Z三种元素的原子序数由大到小的顺序正确的是( )
| A. | X>Y>Z | B. | Y>X>Z | C. | Y>Z>X | D. | Z>Y>X |
12.工业上用菱锰矿(MnCO3)[含FeCO3、SiO2、Cu2(OH)2CO3等杂质]为原料制取二氧化锰,其流程示意图如下:
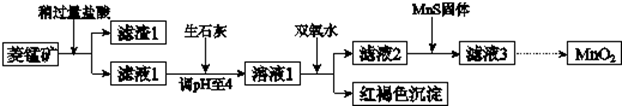
已知:生成氢氧化物沉淀的pH
注:金属离子的起始浓度为0.1mol/L
回答下列问题:
(1)含杂质的菱锰矿使用前需将其粉碎,主要目的是增大接触面积,提高反应速率;盐酸溶解MnCO3的化学方程式是MnCO3+2HCl=MnCl2+CO2↑+H2O;
(2)向溶液1中加入双氧水时,反应的离子方程式是2Fe2++H2O2+4H2O=2Fe(OH)3↓+4H+;
(3)滤液2中加入稍过量的难溶电解质MnS,以除去Cu2+,反应的离子方程式是MnS+Cu2+=Mn2++CuS;
(4)将MnCl2转化为MnO2的一种方法是氧化法.其具体做法是用酸化的NaClO3溶液将MnCl2氧化,该反应的离子方程式为:5Mn2++2ClO3-+4H2O=Cl2↑+5MnO2+8H+;
(5)将MnCl2转化为MnO2的另一种方法是电解法.
①生成MnO2的电极反应式是Mn2+-2e-+2H2O=MnO2+4H+;
②若在上述MnCl2溶液中加入一定量的Mn(NO3)2粉末,则无Cl2产生.其原因是其它条件不变下,增大Mn2+浓度[或增大c(Mn2+)/c(Cl-)],有利于Mn2+放电(不利于Cl-放电).

已知:生成氢氧化物沉淀的pH
| Mn(OH)2 | Fe(OH)2 | Fe(OH)3 | Cu(OH)2 | |
| 开始沉淀时 | 8.3 | 6.3 | 2.7 | 4.7 |
| 完全沉淀时 | 9.8 | 8.3 | 3.7 | 6.7 |
回答下列问题:
(1)含杂质的菱锰矿使用前需将其粉碎,主要目的是增大接触面积,提高反应速率;盐酸溶解MnCO3的化学方程式是MnCO3+2HCl=MnCl2+CO2↑+H2O;
(2)向溶液1中加入双氧水时,反应的离子方程式是2Fe2++H2O2+4H2O=2Fe(OH)3↓+4H+;
(3)滤液2中加入稍过量的难溶电解质MnS,以除去Cu2+,反应的离子方程式是MnS+Cu2+=Mn2++CuS;
(4)将MnCl2转化为MnO2的一种方法是氧化法.其具体做法是用酸化的NaClO3溶液将MnCl2氧化,该反应的离子方程式为:5Mn2++2ClO3-+4H2O=Cl2↑+5MnO2+8H+;
(5)将MnCl2转化为MnO2的另一种方法是电解法.
①生成MnO2的电极反应式是Mn2+-2e-+2H2O=MnO2+4H+;
②若在上述MnCl2溶液中加入一定量的Mn(NO3)2粉末,则无Cl2产生.其原因是其它条件不变下,增大Mn2+浓度[或增大c(Mn2+)/c(Cl-)],有利于Mn2+放电(不利于Cl-放电).
 .
.