题目内容
19.在高温下,碘是紫红色蒸气,氢气、碘化氢是无色气体,在某容器中H2+I2?2HI+Q(高温)可逆反应达到平衡,请填写完整表.| 改变条件 | 平衡移动方向 | 体系内混合气体的颜色变化 |
| (1)加入氢气 | 正反应方向 | 变浅 |
| (2)升高温度 | 逆反应方向 | 变深 |
| (3)加入碘 | 正反应方向 | 变深 |
| (4)使容器的容积压缩到原来的一半 | 不移动 | 变深 |
分析 (1)加入氢气,平衡向着正向移动,碘蒸气的浓度减小;
(2)该反应为放热反应,升高温度后平衡向着逆向移动;
(3)加入碘蒸气,平衡向着逆向移动,但是碘蒸气的浓度会增大;
(4)使容器的容积压缩到原来的一半,平衡不移动,碘蒸气的浓度变为原先的2倍.
解答 解:(1)加入氢气后,反应物浓度增大,平衡向着正向移动,碘蒸气的浓度减小,则混合气体的颜色变浅,
故答案为:正反应方向;变浅;
(2)正反应是放热反应,当温度升高时,平衡向着逆向移动,碘蒸气的浓度增大,混合气体的颜色变深,
故答案为:逆反应方向;变深;
(3)加入碘蒸气,平衡向着正向移动,但是碘蒸气的密度会增大,导致平衡时混合气体的颜色变深,
故答案为:正反应方向;变深;
(4)使容器的容积压缩到原来的一半,增大了压强,由于该反应是气体体积不变的反应,则平衡不移动,但是碘蒸气的浓度变为原先的2倍,所以气体颜色变深,
故答案为:不移动;变深.
点评 本题考查了化学平衡及其影响,题目难度不大,明确化学平衡及其影响因素为解答关键,(3)为易错点,注意加入碘蒸气后平衡向着正向移动,但是达到新的平衡时碘蒸气的浓度反而增大,试题培养了学生的灵活应用能力.

练习册系列答案
 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案
相关题目
9.甲、乙、丙、丁、戊均为短周期主族元素,甲的原子半径是第二周期中最小的;乙的单质能跟冷水剧烈反应产生氢气;丙原子核外p电子比s电子多5个;丁和丙在同周期,丁的最高价为+4价;戊的单质是气体,其密度介于H2和O2的密度之间.下列推断错误的是( )
| A. | 甲的非金属性最强 | |
| B. | 戊的最高价氧化物的水化物酸性最强 | |
| C. | 原子半径大小为:乙>丙>甲 | |
| D. | 乙分别与甲、丙形成晶体M、N的熔点大小为:M<N |
7.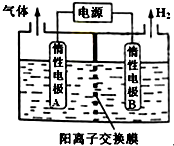 利用LiOH可制备锂离子电池正极材料.LiOH可由电解法制备,如图,两极区电解质溶液分别为LiOH和LiCl溶液.下列说法错误的是( )
利用LiOH可制备锂离子电池正极材料.LiOH可由电解法制备,如图,两极区电解质溶液分别为LiOH和LiCl溶液.下列说法错误的是( )
 利用LiOH可制备锂离子电池正极材料.LiOH可由电解法制备,如图,两极区电解质溶液分别为LiOH和LiCl溶液.下列说法错误的是( )
利用LiOH可制备锂离子电池正极材料.LiOH可由电解法制备,如图,两极区电解质溶液分别为LiOH和LiCl溶液.下列说法错误的是( )| A. | B极区电解质溶液为LiOH溶液 | |
| B. | 阳极电极反应式为2Cl--2e-═Cl2↑ | |
| C. | 电解过程中主要是H+通过阳离子交换膜向B电极迁移 | |
| D. | 电极A连接电源的正极 |
14.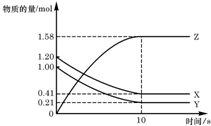 一定温度下,在 2L 的密闭容器中,X、Y、Z 三种气体的物质的量随时间变化的曲线如图所示,下列描述正确的是( )
一定温度下,在 2L 的密闭容器中,X、Y、Z 三种气体的物质的量随时间变化的曲线如图所示,下列描述正确的是( )
 一定温度下,在 2L 的密闭容器中,X、Y、Z 三种气体的物质的量随时间变化的曲线如图所示,下列描述正确的是( )
一定温度下,在 2L 的密闭容器中,X、Y、Z 三种气体的物质的量随时间变化的曲线如图所示,下列描述正确的是( )| A. | 反应开始到 10s,用 Z 表示的反应速率为 0.158mol/(L•s) | |
| B. | 反应开始到 10s,X 的物质的量浓度减少了 0.79mol/L | |
| C. | 反应开始到 10s,Y 的转化率为 79.0% | |
| D. | 反应的化学方程式为:X(g)+Y(g)?Z(g) |
4.下列各组中物质用酸性高锰酸钾或溴水均能鉴别的是( )
| A. | 乙酸乙酯、裂化汽油、溴苯、福尔马林 | |
| B. | 乙醇、乙酸、乙醛、乙苯 | |
| C. | 苯甲酸溶液、甘油、甲苯、甲酸 | |
| D. | 苯酚、苯乙烯、苯、1,2-二溴乙烷 |
11.等质量下列物质与足量稀硝酸反应,放出NO物质的量最多的是( )
| A. | Fe2O3 | B. | FeSO4 | C. | Cu | D. | CuO |
14.下列物质的转化在给定条件下能实现的是( )
| A. | NaCl(aq)$\stackrel{CO_{2}}{→}$NaHCO3(s)$\stackrel{△}{→}$Na2CO3(s) | B. | CuCl2$\stackrel{NaOH(aq)}{→}$Cu(OH)2$→_{△}^{葡萄糖}$Cu | ||
| C. | Al$\stackrel{NaOH(aq)}{→}$NaAlO2(aq)$\stackrel{△}{→}$NaAlO2(s) | D. | MgO(s)$\stackrel{HNO_{3}(aq)}{→}$Mg(NO3)2(aq)$\stackrel{电解}{→}$Mg(s) |
15. 常温下,浓度均为0.10mol/L、体积均为V0的HA和HB溶液,分别加水稀释至体积V,pH随$lg\frac{V}{V_0}$的变化如图所示,下列叙述正确的是( )
常温下,浓度均为0.10mol/L、体积均为V0的HA和HB溶液,分别加水稀释至体积V,pH随$lg\frac{V}{V_0}$的变化如图所示,下列叙述正确的是( )
 常温下,浓度均为0.10mol/L、体积均为V0的HA和HB溶液,分别加水稀释至体积V,pH随$lg\frac{V}{V_0}$的变化如图所示,下列叙述正确的是( )
常温下,浓度均为0.10mol/L、体积均为V0的HA和HB溶液,分别加水稀释至体积V,pH随$lg\frac{V}{V_0}$的变化如图所示,下列叙述正确的是( )| A. | 该温度下HB的电离平衡常数约等于1.11×10-5 | |
| B. | 相同条件下NaA溶液的pH大于NaB溶液的pH | |
| C. | 溶液中水的电离程度:a=c>b | |
| D. | 当$lg\frac{V}{V_0}=3$时,若两溶液同时升高温度,则$\frac{{c({B^-})}}{{c({A^-})}}$减小 |

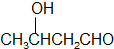 $→_{②}^{△}$CH3CH=CHCHO
$→_{②}^{△}$CH3CH=CHCHO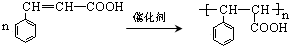 .
.
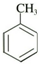 →E 的合成路线(试剂及溶剂任选:合成路线参照“已知①”中书写形式)
→E 的合成路线(试剂及溶剂任选:合成路线参照“已知①”中书写形式) .
.