题目内容
15.高锰酸钾制氯气:2KMnO4+16HCl═2KCl+2MnCl2+5Cl2↑+8H2O 地康法制氯气:4HCl+O2$\frac{\underline{催化剂}}{△}$ 2Cl2+2H2O 二氧锰制氯气:MnO2+4HCl$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O 下列说法正确的是( )| A. | 实验室常用地康法制氯气 | B. | 氧化性强弱顺序是O2>KMnO4>MnO2 | ||
| C. | 氧化性强弱顺序是KMnO4>O2>MnO2 | D. | 氧化性强弱顺序是KMnO4>MnO2>O2 |
分析 根据反应条件判断反应的难易程度,反应条件越少的氧化还原反应越容易发生,越容易发生的氧化还原反应氧化剂的氧化性越强,以此解答该题.
解答 解:地康法制氯气需在催化剂的条件下完成,实验室难以实现,由反应条件可知,反应条件越少的氧化还原反应越容易发生,越容易发生的氧化还原反应氧化剂的氧化性越强,所以氧化性最强的是高锰酸钾,其次是二氧化锰,最后是氧气,
故选D.
点评 本题考查了氧化剂氧化性强弱的判断,根据“反应条件越少的氧化还原反应越容易发生,越容易发生的氧化还原反应氧化剂的氧化性越强”来解答即可,难度不大.

练习册系列答案
相关题目
6.实验室中保存金属钠的方法是( )
| A. | 放在水中 | B. | 放在四氯化碳中 | C. | 放在石蜡油中 | D. | 放在细沙中 |
3.下列事实不能用平衡移动原理解释的是( )
| A. | 由H2、I2(g)、HI组成的平衡体系,加压后颜色加深 | |
| B. | 用加热蒸干AlCl3溶液的方法不能制得无水AlCl3 | |
| C. | 蒸馏水和0.1mol•L-1 NaOH溶液中的c(H+),前者大于后者 | |
| D. | 向含有少量Fe3+的MgCl2酸性溶液中加MgCO3,可将Fe3+转化成Fe(OH)3除去 |
10.若在加入铝粉能放出氢气的溶液中,分别加入下列各组离子,一定大量共存的是( )
| A. | NH4+、I-、CO32-、Fe3+ | B. | Na+、Ba2+、Mg2+、HCO3- | ||
| C. | NO3-、Mg2+、Cl-、Ca2+ | D. | K+、Na+、Cl-、SO42- |
20.下列有机物的说法正确的是( )


| A. | C5H12有2种同分异构体 | |
| B. | C4H10O属于醇的结构有5种 | |
| C. | 甲、丙分别是CH4、苯的比例模型,乙能发生加成反应,丁在一定条件下能转化为乙 | |
| D. | 甲、乙能发生氧化反应,丙、丁不能发生氧化反应 |
4.下列有关热化学方程式书写正确的是( )
| 已知条件 | 热化学方程式 | |
| A | 中和热为57.3kJ/mol | H2SO4(aq)+Ba(OH)2(aq)═ BaSO4(s)+2H2O(l) △H=-114.6kJ/mol |
| B | 合成氨反应生成0.1mol NH3时放出a kJ热量 | N2(g)+3H2(g)?2NH3(g) △H=-20a kJ/mol |
| C | H2的燃烧热为285.8kJ/mol | H2(g)+$\frac{1}{2}$O2(g)═H2O(g) △H=-285.8kJ/mol |
| D | 碳的燃烧热为393.5kJ/mol | 2C(s)+O2(g)═2CO(g) △H=-787kJ/mol |
| A. | A | B. | B | C. | C | D. | D |
5.利用已有的实验器材,规格和数量不限,能完成相应实验的是( )
| 实验器材(省略夹持装置) | 相应实验 | |
| A | 烧杯、玻璃棒、分液漏斗 | 用溴水和CCl4除去NaBr溶液中的少量NaI |
| B | 烧杯、玻璃棒、蒸发皿 | 硫酸铜溶液的结晶 |
| C | 烧杯、玻璃棒、胶头滴管、滤纸 | 用盐酸除去硫酸钡中的少量碳酸钡 |
| D | 烧杯、玻璃棒、胶头滴管、容量瓶 | 用固体氯化钠配制0.5mol/L的溶液 |
| A. | A | B. | B | C. | C | D. | D |
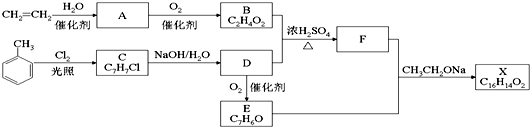
 +Cl2$\stackrel{光照}{→}$
+Cl2$\stackrel{光照}{→}$ .B和D反应生成F的化学方程式
.B和D反应生成F的化学方程式 .D→E的化学方程式2
.D→E的化学方程式2 +O2$→_{△}^{Cu}$2
+O2$→_{△}^{Cu}$2 +2H2O.
+2H2O. .
. CH2OCH2CH2CHO B.
CH2OCH2CH2CHO B. CH=CHCH2CH2CHO
CH=CHCH2CH2CHO COOCH2CH2CH3 D.CH2=CHCH=CHCH=CHCH=CHCOOH.
COOCH2CH2CH3 D.CH2=CHCH=CHCH=CHCH=CHCOOH.