题目内容
5.已知A、B、C是金属单质,甲、乙、丙为常见气体,其中B是地壳中含量居第二位的金属元素.它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出).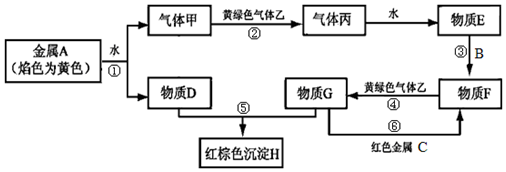
请根据以上信息回答下列问题:
(1)写出下列物质的化学式:BFe,气体丙HCl.
(2)写出反应④的化学方程式:2FeCl2+Cl2=2FeCl3,写出反应⑥的化学方程式:2FeCl3+Cu=CuCl2+2FeCl2.
(3)物质F的溶液中通入过量的空气和氨气的混合气体,同样会产生红棕色沉淀H,写出发生反应的总的离子方程式4Fe2++O2+8NH3+10H2O=8NH4++4Fe(OH)3↓.过滤后,检验滤液中阳离子的方法为取溶液少许于试管中,加入浓NaOH溶液,加热,在试管口用湿润的红色石蕊试纸检验放出的气体,若试纸变蓝,则存在NH4+.
分析 金属A焰色反应为黄色,故A为金属Na,乙是黄绿色气体,乙为Cl2,H为红褐色沉淀,为Fe(OH)3;由反应①Na→气体甲+D,可知甲为H2,D为NaOH,由甲+乙→丙,故丙为HCl,HCl溶于水的物质E,故E为盐酸;B是地壳中含量居第二位的金属元素,应为Fe,则F为FeCl2,G为FeCl3,红色金属C为Cu,FeCl2与氢氧化钠在空气中生成氢氧化铁,符合各物质的转化关系,以此解答该题.
解答 解:(1)由以上分析可知B为Fe,气体丙为HCl,故答案为:Fe;HCl;
(2)反应④为氯化亚铁与氯气的反应,化学方程式为2FeCl2+Cl2=2FeCl3,反应⑥为氯化铁与铜的反应,化学方程式为2FeCl3+Cu=CuCl2+2FeCl2,
故答案为:2FeCl2+Cl2=2FeCl3;2FeCl3+Cu=CuCl2+2FeCl2;
(3)F为FeCl2,通入氨气生成氢氧化亚铁,通入空气,氢氧化亚铁被氧化生成氢氧化铁,反应的总离子方程式为4Fe2++O2+8NH3+10H2O=8NH4++4Fe(OH)3↓,溶液中存在铵根离子,可取溶液少许于试管中,加入浓NaOH溶液,加热,在试管口用湿润的红色石蕊试纸检验放出的气体,若试纸变蓝,则存在NH4+,
故答案为:4Fe2++O2+8NH3+10H2O=8NH4++4Fe(OH)3↓;取溶液少许于试管中,加入浓NaOH溶液,加热,在试管口用湿润的红色石蕊试纸检验放出的气体,若试纸变蓝,则存在NH4+.
点评 本题以无机框图题的形式考查无机物的推断,为高考常见题型,题目侧重考查Na、Al、Fe、Cl等元素单质及其化合物之间的相互转化关系、化学式的书写、离子方程式等,难度中等,注意基础知识的掌握.

练习册系列答案
相关题目
15.用Cl2生产某些含氯有机物时会生成副产物HCl,利用下列反应可实现氯的循环利用:
4HCl(g)+O2(g)?2Cl2(g)+2H2O(g)△H=-115.6kJ/mol
恒温恒容的密闭容器中,充入一定量的反应物发生上述反应,能充分说明该反应达到化学平衡状态的是
( )
4HCl(g)+O2(g)?2Cl2(g)+2H2O(g)△H=-115.6kJ/mol
恒温恒容的密闭容器中,充入一定量的反应物发生上述反应,能充分说明该反应达到化学平衡状态的是
( )
| A. | 气体的质量不再改变 | |
| B. | 氯化氢的转化率不再改变 | |
| C. | 断开4 mol H-Cl键的同时生成4 mol H-O键 | |
| D. | n(HCl):n(O2):n(Cl2):n(H2O)=4:1:2:2 |
16.下列反应中,SO2做还原剂的是( )
| A. | 2Mg+SO2$\frac{\underline{\;△\;}}{\;}$2MgO+S | |
| B. | SO2+Br2+2H2O═2HBr+H2SO4 | |
| C. | Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O | |
| D. | SO2+2NaOH═Na2SO3+H2O |
13.设NA为阿伏加德罗常数,下列叙述中正确的是( )
| A. | 1.7 g氨气所含分子数为0.1 NA | |
| B. | 常温常压下,11.2 L氯气所含原子数为NA | |
| C. | 1 mol•L-1的BaCl2溶液中所含Cl-离子数目为2 NA | |
| D. | 71 g氯气与足量铁粉充分反应,转移的电子数为3 NA |
20.下列能使湿润的淀粉碘化钾变蓝的是( )
| A. | SO2 | B. | HCl | C. | KBr | D. | Cl2 |
10.下列能使品红溶液褪色的是( )
| A. | CO2 | B. | Na2SO3 | C. | Cl2 | D. | HCl |
2.NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A. | 19gNHD2和19gNH2T中含有的中子数均为10NA | |
| B. | 标准状况下,22.4LO2参加反应转移的电子数一定是4NA | |
| C. | 1molCnH2n中含有的共用电子对数为(3n+1)NA | |
| D. | 2molSO2和1molO2在一定条件下充分反应后,所得混合气体的分子数大于2NA |
 已知:A是石油裂解气的主要成份.现以A为主要原料合成乙酸乙酯,其合成路线如图所示.回答下列问题:
已知:A是石油裂解气的主要成份.现以A为主要原料合成乙酸乙酯,其合成路线如图所示.回答下列问题: