题目内容
15.下列物质的水溶液能导电,但属于非电解质的是( )| A. | CH3CH2COOH | B. | Cl2 | C. | NH4HCO3 | D. | SO2 |
分析 电解质是指在水溶液或熔化状态下能导电的化合物,而非电解质是指在水溶液和熔化状态下都不能导电的化合物.
解答 解:A.CH3CH2COOH属于电解质,故A不选;
B.氯气是单质,既不是电解质,也不是非电解质,故B不选;
C.碳酸氢铵是电解质,故C不选;
D.SO2属于非电解质,溶于水,与水反应生成亚硫酸,亚硫酸电离产生自由离子而导电,故D选;
故选:D.
点评 本题考查电解质和非电解质,学生应明确电解质和非电解质都是化合物,并明确判断电解质时发生电离的为化合物本身来分析解答即可.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
18.下列物质的水溶液因水解而呈碱性的是( )
| A. | NaOH | B. | NH4Cl | C. | NaCl | D. | Na2CO3 |
6.“保护环境”是我国的基本国策.下列做法不应该提倡的是( )
| A. | 推广燃煤发电,同时将化工厂迁移至人口稠密的地区 | |
| B. | 加强生活污水的脱氮除磷处理,遏制水体的富营养化 | |
| C. | 加强汽车尾气的处理,减少大气污染物的排放 | |
| D. | 用CO2合成聚碳酸酯可降解塑料,实现“碳”的循环利用 |
3.根据能量变化示意图,下列说法正确的是( )
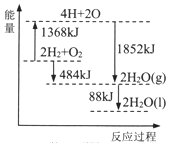

| A. | 拆开2molH2(g)和1 molO2(g)中的化学键,共放出1368 kJ能量 | |
| B. | 1 molH2和0.5molO2的能量之和比1 molH2O(1)的能量大242 kJ | |
| C. | 2H2O(g)=2H2(g)+O2(g)△H=+484KJ/mol | |
| D. | 2H2(g)+O2(g)=2H2O(1)△H=572KJ/mol |
20.铅蓄电池放电时发生的反应是:Pb+SO42--2e-═PbSO4;PbO2+4H++SO42-+2e-═PbSO4+2H2O,使用该电池时,若外电路上转移电子0.05mol,则消耗H2SO4的质量是( )
| A. | 0.05mol | B. | 0.025mol | C. | 4.9g | D. | 9.8g |
7.设NA为阿伏加徳罗常数的值,下列说法正确的是( )
| A. | 23gNa与O2完全反应,生成Na2O和Na2O2的混合物,转移的电子数为NA | |
| B. | 88.0g14CO2与14N2O的混合物中所含中子数为44NA | |
| C. | 0.1L,l.0mol/L的NaAlO2水溶液中含有的氧原子数为0.2NA | |
| D. | 室温下,将1mol铁片投入到0.5L,18.4mol/L的硫酸中,转移的电子数为3NA |
5.短周期元素X、Y、Z、W的原子序数依次增大.它们的原子最外层电子数之和为13,X的原子半径比Y的小,其中X与W同主族.一种常见的无色无味液体分解可以得到X和Z元素的单质.下列说法中不正确的是( )
| A. | X、Y、Z三种元素可以形成离子化合物 | |
| B. | 元素X 和W之间不可能形成二元化合物 | |
| C. | 元素Y的简单气态氧化物的热稳定性比Z的弱 | |
| D. | 元素Y、Z、W中,元素W的简单离子的半径最小 |