题目内容
6.“保护环境”是我国的基本国策.下列做法不应该提倡的是( )| A. | 推广燃煤发电,同时将化工厂迁移至人口稠密的地区 | |
| B. | 加强生活污水的脱氮除磷处理,遏制水体的富营养化 | |
| C. | 加强汽车尾气的处理,减少大气污染物的排放 | |
| D. | 用CO2合成聚碳酸酯可降解塑料,实现“碳”的循环利用 |
分析 A.燃煤发电,消耗大量的化石能源,且排放二氧化硫及固体颗粒物;
B.N、P均可导致水中藻类植物大量生长,导致水体变质;
C.汽车尾气含S、N的氧化物,可导致光化学烟雾;
D.CO2合成聚碳酸酯可降解塑料,可减少塑料的使用,缓解白色污染.
解答 解:A.燃煤发电,消耗大量的化石能源,且排放二氧化硫及固体颗粒物,会污染环境,则不能将化工厂迁移至人口稠密的地区,故A错误;
B.N、P均可导致水中藻类植物大量生长,导致水体变质,则加强生活污水的脱氮除磷处理,遏制水体的富营养化,故B正确;
C.汽车尾气含S、N的氧化物,可导致光化学烟雾,则加强汽车尾气的处理,减少大气污染物的排放,故C正确;
D.CO2合成聚碳酸酯可降解塑料,可减少塑料的使用,缓解白色污染,则用CO2合成聚碳酸酯可降解塑料,实现“碳”的循环利用,故D正确;
故选A.
点评 本题考查三废处理及环境保护,为高频考点,把握物质的性质、环境污染物及环保为解答的关键,侧重分析与应用能力的考查,注意化学与生活的联系,题目难度不大.

练习册系列答案
 鹰派教辅衔接教材河北教育出版社系列答案
鹰派教辅衔接教材河北教育出版社系列答案 初中暑期衔接系列答案
初中暑期衔接系列答案
相关题目
9.下列化学反应的离子方程式正确的是( )
| A. | 氯化铝溶液中加入过量氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| B. | Cl2通入NaOH溶液中:Cl2+OH-═Cl-+ClO-+H2O | |
| C. | 二氧化氮与水反应:3NO2+H2O═2H++2NO3-+NO | |
| D. | 往碳酸镁中滴加稀盐酸:CO32-+2H+═CO2↑+H2O |
10.下列说法正确的是( )
| A. | 相同体积、相同浓度的氨水和NaOH溶液中和盐酸的能力相同 | |
| B. | 醋酸溶液中只存在一个电离平衡体系 | |
| C. | 0.1mol•L-1的氨水能使酚酞试液变红,说明氨水是弱电解质水溶液 | |
| D. | 同浓度同体积的醋酸和盐酸分别与足量镁反应时,放出H2的速率相同 |
1.空气是人类生存所必须的重要资源.下列措施不利于建设“蓝天工程”的是( )
| A. | 严禁露天焚烧农作物秸秆 | |
| B. | 加强植树造林,增大绿化面积 | |
| C. | 大力推行汽车使用天然气或氢气为燃料 | |
| D. | 生产生活中加大煤炭和石油等燃料的使用量 |
11.某元素的一种同位素X的原子质量数为A,含N个中子,它与1H原子组成HmX分子,在ag HmX中所含质子的物质的量是( )
| A. | $\frac{a}{m+A}$(A-N+m)mol | B. | a/N(A-N)mol | C. | a/A(A-N+m)mol | D. | a/A(A-N-m)mol |
18.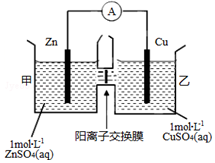 锌铜原电池装置如图所示,中间被阳离子交换膜隔开且只允许阳离子和水分子通过,下列有关叙述正确的是( )
锌铜原电池装置如图所示,中间被阳离子交换膜隔开且只允许阳离子和水分子通过,下列有关叙述正确的是( )
 锌铜原电池装置如图所示,中间被阳离子交换膜隔开且只允许阳离子和水分子通过,下列有关叙述正确的是( )
锌铜原电池装置如图所示,中间被阳离子交换膜隔开且只允许阳离子和水分子通过,下列有关叙述正确的是( )| A. | 铜电极上发生氧化反应 | |
| B. | 外电路中电子由Cu流向Zn | |
| C. | 电池工作一段时间后,乙池溶液的总质量增加 | |
| D. | 电池工作一段时间后,甲池的C(SO42-)增大 |
15.下列物质的水溶液能导电,但属于非电解质的是( )
| A. | CH3CH2COOH | B. | Cl2 | C. | NH4HCO3 | D. | SO2 |
16.下列各叙述中不正确的是( )
| A. | 电解精炼铜时当阳极溶解32 g铜时,转移电子数大于NA个(Cu-64) | |
| B. | 向酸性FeSO4溶液中滴入少量NaClO溶液,反应的离子方程式为:2Fe2++ClO-+2H+═Cl-+2Fe3++H2O | |
| C. | 向10 mL 0.1mol•L-1 NH4Al(SO4)2溶液中,滴加等浓度Ba(OH)2溶液20 mL,反应的离子方程式为:2Ba2++4OH-+NH4++Al3++2SO42-=2BaSO4↓+Al(OH)3↓+NH3•H2O | |
| D. | 浓盐酸与KClO3混合受热制Cl2:6HCl+KClO3═3Cl2↑+3H2O+KCl,1molKClO3反应转移6 NA个电子 |