题目内容
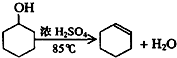
7.化合物H具有似龙延香、琥珀香气息,香气淡而持久,广泛用作香精的稀释剂和定香剂.合成它的一种路线如图: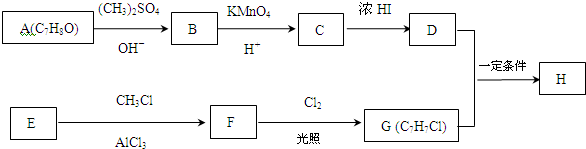
已知以信息:
①
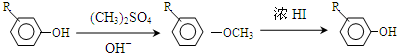
②核磁共振氢谱显示A苯环上有四种化学环境的氢,它们的位置相邻
③在D溶液中滴加几滴FeCl3溶液,溶液呈紫色
④芳烃 F的相对分子质量介于90~100之间,0.1molF充分燃烧可生成7.2g水
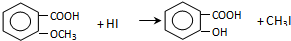
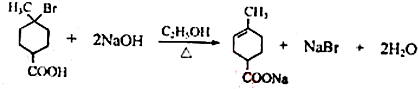
⑤

回答下列问题:
(1)A的化学名称是2-甲基苯酚,由C生成D的化学方程式为
 .
.(2)由F生成G的化学方程式为:
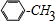 +Cl2$\stackrel{光照}{→}$
+Cl2$\stackrel{光照}{→}$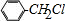 +HCl,反应类型为取代反应.
+HCl,反应类型为取代反应.(3)H的结构简式为
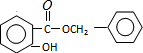 .
.(4)C的同分异构体中含有三取代苯结构和两个A中的官能团,又可发生银镜反应的有6种(不考虑立体异构),其中核磁共振氢谱为5组峰,且面积比为1:2:2:2:1的结构简式是
 (或
(或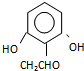 )(任写一种即可)
)(任写一种即可) (5)由苯酚和已有的信息经以下步骤可以合成化合物
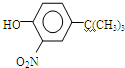
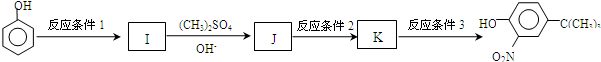
反应条件1所用的试剂为(CH3)3CCl/AlCl3,K的结构简式为
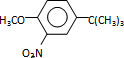 ,反应条件3所用的试剂为浓HI.
,反应条件3所用的试剂为浓HI.
分析 核磁共振氢谱显示A苯环上有四种化学环境的氢,它们的位置相邻,结合A的分子式及信息反应①可知A为邻甲基苯酚: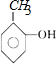 ;A发生信息反应①生成B,则B为
;A发生信息反应①生成B,则B为 ;B中侧链的甲基被酸性高锰酸钾溶液氧化成羧基,则C为
;B中侧链的甲基被酸性高锰酸钾溶液氧化成羧基,则C为 ;C按照信息反应①生成D,在D溶液中滴加几滴FeCl3溶液,溶液呈紫色,说明D中含有酚羟基,则D为:
;C按照信息反应①生成D,在D溶液中滴加几滴FeCl3溶液,溶液呈紫色,说明D中含有酚羟基,则D为: ;芳烃F的相对分子质量介于90~100之间,0.1molF充分燃烧可生成7.2g水,1molF中含有氢原子的数目为:$\frac{\frac{7.2g}{18g/mol}×2}{0.1mol}$=8,结合F与氯气发生在取代反应生成的G的分子式可知,F的分子式为:C7H8,则F为甲苯:
;芳烃F的相对分子质量介于90~100之间,0.1molF充分燃烧可生成7.2g水,1molF中含有氢原子的数目为:$\frac{\frac{7.2g}{18g/mol}×2}{0.1mol}$=8,结合F与氯气发生在取代反应生成的G的分子式可知,F的分子式为:C7H8,则F为甲苯: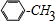 ,故G为:
,故G为: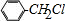 ;E与一氯甲烷在氯化铝存在条件下反应生成F,则E为
;E与一氯甲烷在氯化铝存在条件下反应生成F,则E为 ;D和G按照信息⑤反应生成H,则H为:
;D和G按照信息⑤反应生成H,则H为: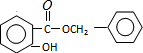 ,据此进行解答.
,据此进行解答.
解答 解:核磁共振氢谱显示A苯环上有四种化学环境的氢,它们的位置相邻,结合A的分子式及信息反应①可知A为邻甲基苯酚: ;A发生信息反应①生成B,则B为
;A发生信息反应①生成B,则B为 ;B中侧链的甲基被酸性高锰酸钾溶液氧化成羧基,则C为:
;B中侧链的甲基被酸性高锰酸钾溶液氧化成羧基,则C为: ;C按照信息反应①生成D,在D溶液中滴加几滴FeCl3溶液,溶液呈紫色,说明D中含有酚羟基,则D为:
;C按照信息反应①生成D,在D溶液中滴加几滴FeCl3溶液,溶液呈紫色,说明D中含有酚羟基,则D为: ;芳烃F的相对分子质量介于90~100之间,0.1molF充分燃烧可生成7.2g水,1molF中含有氢原子的数目为:$\frac{\frac{7.2g}{18g/mol}×2}{0.1mol}$=8,结合F与氯气发生在取代反应生成的G的分子式可知,F的分子式为:C7H8,则F为甲苯:
;芳烃F的相对分子质量介于90~100之间,0.1molF充分燃烧可生成7.2g水,1molF中含有氢原子的数目为:$\frac{\frac{7.2g}{18g/mol}×2}{0.1mol}$=8,结合F与氯气发生在取代反应生成的G的分子式可知,F的分子式为:C7H8,则F为甲苯: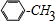 ,故G为:
,故G为: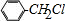 ;E与一氯甲烷反应生成F,则E为
;E与一氯甲烷反应生成F,则E为 ;D和G按照信息⑤反应生成H,则H为:
;D和G按照信息⑤反应生成H,则H为: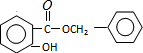 ,
,
(1)A的结构简式为 ,其名称为2-甲基苯酚;由C生成D的化学方程式为:
,其名称为2-甲基苯酚;由C生成D的化学方程式为:
故答案为:2-甲基苯酚; ;
;
(2)F为甲苯: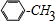 ,甲苯在光照条件下与氯气发生取代反应生成
,甲苯在光照条件下与氯气发生取代反应生成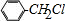 ,反应的化学方程式为:
,反应的化学方程式为: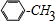 +Cl2$\stackrel{光照}{→}$
+Cl2$\stackrel{光照}{→}$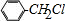 +HCl,
+HCl,
故答案为: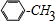 +Cl2$\stackrel{光照}{→}$
+Cl2$\stackrel{光照}{→}$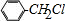 +HCl;取代反应;
+HCl;取代反应;
(3)根据分析可知,H的结构简式为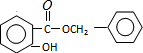 ,故答案为:
,故答案为: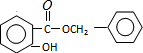 ;
;
(4)C为 ,其同分异构体中含有三取代苯结构和两个A中的官能团,A中官能团为酚羟基,说明该有机物分子中含有两个羟基;又可发生银镜反应,其分子中一定含有醛基,所以满足条件的C的同分异构体中含有2个酚羟基、1个-CH2CHO,①当3个取代基都相邻时,中间为羟基或醛基,有2种结构;②当两个羟基相邻时,存在1种结构;③当1个羟基与-CH2CHO相邻时,另一个羟基可以在间位,有2种结构;④3个取代基都不相邻时有1种结构,所以总共存在6种同分异构体;其中核磁共振氢谱为5组峰,且面积比为1:2:2:2:1,该有机物分子中含有5种H原子,且具有一定的对称结构,满足条件的有机物的结构简式为:
,其同分异构体中含有三取代苯结构和两个A中的官能团,A中官能团为酚羟基,说明该有机物分子中含有两个羟基;又可发生银镜反应,其分子中一定含有醛基,所以满足条件的C的同分异构体中含有2个酚羟基、1个-CH2CHO,①当3个取代基都相邻时,中间为羟基或醛基,有2种结构;②当两个羟基相邻时,存在1种结构;③当1个羟基与-CH2CHO相邻时,另一个羟基可以在间位,有2种结构;④3个取代基都不相邻时有1种结构,所以总共存在6种同分异构体;其中核磁共振氢谱为5组峰,且面积比为1:2:2:2:1,该有机物分子中含有5种H原子,且具有一定的对称结构,满足条件的有机物的结构简式为: 或
或 ,
,
故答案为:6; (或
(或 );
);
(5)由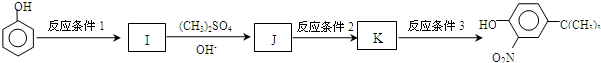 ,根据初始原料苯酚、最终产物
,根据初始原料苯酚、最终产物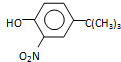 可知,反应过程中需要引进硝基、-C(CH3)3,结合信息反应可知,I转化成J是为了保护酚羟基,反应1中一定引进了-C(CH3)3,所以反应条件1为(CH3)3CCl/AlCl3,I为
可知,反应过程中需要引进硝基、-C(CH3)3,结合信息反应可知,I转化成J是为了保护酚羟基,反应1中一定引进了-C(CH3)3,所以反应条件1为(CH3)3CCl/AlCl3,I为 ;再利用逆推法,反应条件3应该为将酚羟基还原,则K为
;再利用逆推法,反应条件3应该为将酚羟基还原,则K为 ,反应条件3为浓HI;反应2通过硝化反应引进硝基,
,反应条件3为浓HI;反应2通过硝化反应引进硝基,
故答案为:(CH3)3CCl/AlCl3; ;浓HI.
;浓HI.
点评 本题考查了有机合成,题目难度较大,根据合成流程明确合成原理为解答关键,注意熟练掌握常见有机物结构与性质及同分异构体的概念及书写原则,(5)为难点,需要充分利用题中信息反应原理,试题充分考查了学生的分析、理解能力及逻辑推理能力.

 阅读快车系列答案
阅读快车系列答案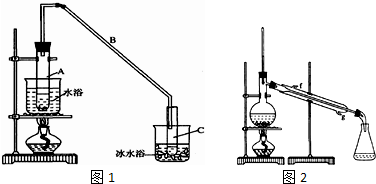
已知:
| 密度(g/cm3) | 熔点(℃) | 沸点(℃) | 溶解性 | |
| 环己醇 | 0.96 | 25 | 161 | 能溶于水 |
| 环己烯 | 0.81 | -103 | 83 | 难溶于水 |
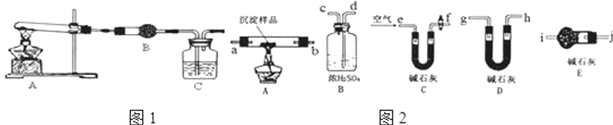
将12.5mL环己醇加入试管A中,再加入lml浓硫酸,摇匀后放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品.
①A采用水浴加热的优点是均匀受热,容易控制反应温度.
②试管C置于冰水浴中的目的是试管C置于冰水浴中.
(2)制备精品 ①环己烯粗品中含有环己醇和少量酸性杂质等.加入饱和食盐水,振荡、静置、分层,环己烯在上层(填上或下),分液后用c(填字母,单选)洗涤.
a.KMnO4溶液 b.稀H2SO4 c.Na2CO3溶液
②再将环己烯按图2装置蒸馏,冷却水从g口进入(填g或f).蒸馏时要加入生石灰,目的是生石灰吸收水分,便于蒸馏出更纯净的产品.
③收集产品时,控制的温度应在83℃左右,实验制得的环己烯精品质量低于理论产量,可能的原因是c(填字母,单选).
a.蒸馏时从70℃开始收集产品
b.环己醇实际用量多了
c.制备粗品时环己醇随产品一起蒸出
(3)以下区分环己烯精品和粗品的方法,合理的是bc.
a.用酸性高锰酸钾溶液 b.用金属钠 c.测定沸点.
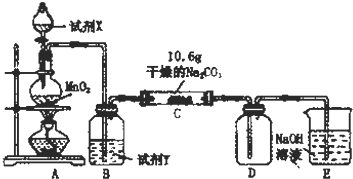
(1)A中制取Cl2的离子方程式4H++2Cl-+MnO2$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O.
(2)通入一定量潮湿的Cl2反应后,经检测,D中只有Cl2O一种气体,C中只含一种氯盐外,同时含有NaHCO3等,某同学对C中所得固体残渣的成分进行探究.
①提出合理假设.
假设1:存在两种成分:NaHCO3和NaCl;
假设2:存在三种成分:NaHCO3和NaCl、Na2CO3.
②设计方案,进行实验.写出实验步骤以及预期现象和结论.
限选实验试剂和仪器:蒸馏水、稀HNO3、BaCl2溶液、澄清石灰水、AgNO3溶液、试管、小烧杯.
| 实验步骤 | 预期现象和结论 |
| 步骤1:取C中的少量固体样品于试管中,滴加足量蒸馏水 至固体溶解,然后将所得溶液分别置于A、B试管中. | |
| 步骤2:向A试管中滴加适量BaCl2溶液. | a.若无明显现象,证明固体中不含Na2CO3 b.若溶液变浑浊,证明固体中含Na2CO3 |
| 步骤3:向B试管中滴加过量的稀硝酸,再滴加AgNO3溶液 | 若溶液变浑浊,证明固体中含有NaCl |
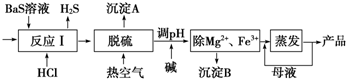
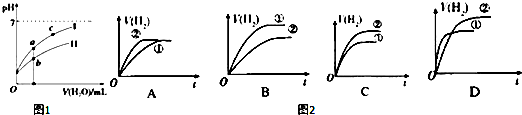
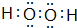 .
.


 .
. .
.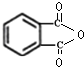 .
.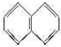 .
.
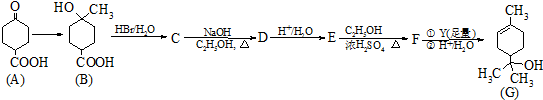
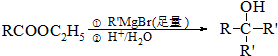
 .
.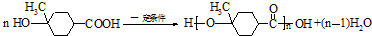 .
. .
. .
.