题目内容
12.下列说法正确的是( )| A. | 按系统命名法,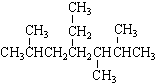 的名称为2,5,6-三甲基-4-乙基庚烷 的名称为2,5,6-三甲基-4-乙基庚烷 | |
| B. | 常压下,正戊烷、异戊烷、新戊烷的沸点依次升高 | |
| C. | “糖类”物质均具有明显的甜味 | |
| D. | 1mol的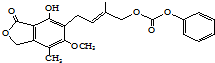 最多能与含5mol NaOH的水溶液完全反应 最多能与含5mol NaOH的水溶液完全反应 |
分析 A.未满足取代基位次之和最小,主链编号错误;
B.烷烃同分异构体中支链越多,沸点越低;
C.淀粉、纤维素等多糖没有甜味;
D.酚-OH、-COOC能与NaOH溶液反应.
解答 解:A.主链含有7个碳为庚烷,从右端编号,化合物的名称应是2,3,5-三甲基-4-乙基庚烷,故A错误;
B.烷烃同分异构体中支链越多,沸点越低,则正戊烷、异戊烷、新戊烷的沸点依次降低,故B错误;
C.糖类中像淀粉、纤维素等多糖没有甜味,故C错误;
D.分子中含有1个酚羟基、3个酯基,都能与NaOH反应,其中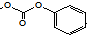 能和3molNaOH反应,则1mol该有机物最多能和含5molNaOH的水溶液完全反应,故D正确;
能和3molNaOH反应,则1mol该有机物最多能和含5molNaOH的水溶液完全反应,故D正确;
故选D.
点评 本题考查有机物的结构和性质,为高考常见题型,侧重于学生的分析能力的考查,注意把握有机物的官能团的性质,为解答该类题目的关键,难度不大.

练习册系列答案
相关题目
10.干冰晶胞是一个面心立方体,在该晶体中每个顶角各有1个二氧化碳分子,每个面心各有一个二氧化碳分子,实验测得25℃时干冰晶体的晶胞边长为acm,其摩尔质量为Mg/mol,阿伏加德罗常数为NA,则该干冰晶体的密度为(单位:g/cm3).( )
| A. | $\frac{14M}{{a}^{3}{N}_{A}}$ | B. | $\frac{M}{{a}^{3}{N}_{A}}$ | C. | $\frac{2M}{{a}^{3}{N}_{A}}$ | D. | $\frac{4M}{{a}^{3}{N}_{A}}$ |
20.下述实验方案不能达到实验目的是( )
| A. |  目的:验证乙炔的还原性 | |
| B. |  目的:收集氨气 | |
| C. |  操作:片刻后在Fe电极附近滴入 K3[Fe(CN)6]溶液,目的:验证Fe电极被保护 | |
| D. | 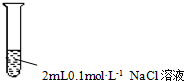 操作:①加入3滴同浓度的AgNO3溶液、②再加入3滴同浓度的Na2S溶液,目的:验证AgCl的溶解度大于Ag2S |
7.能正确表示下列化学反应的离子方程式的是( )
| A. | 盐酸与Fe(OH)3反应:Fe(OH)3+3H+═Fe3++3H2O | |
| B. | 稀硫酸与铁粉反应:2Fe+6H+═2Fe3++3H2↑ | |
| C. | 氢氧化钡溶液与稀硫酸反应:Ba2++SO${\;}_{4}^{2-}$═BaSO4↓ | |
| D. | Fe3O4与盐酸反应:Fe3O4+8H+═3Fe3++4H2O |
17.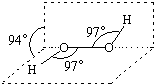 过氧化氢被称为绿色氧化剂,它的分子结构如图所示.已知该分子H-O-O键角都是97°.下列有关H2O2的说法正确的是( )
过氧化氢被称为绿色氧化剂,它的分子结构如图所示.已知该分子H-O-O键角都是97°.下列有关H2O2的说法正确的是( )
 过氧化氢被称为绿色氧化剂,它的分子结构如图所示.已知该分子H-O-O键角都是97°.下列有关H2O2的说法正确的是( )
过氧化氢被称为绿色氧化剂,它的分子结构如图所示.已知该分子H-O-O键角都是97°.下列有关H2O2的说法正确的是( )| A. | 过氧化氢分子中存在离子键、共价键 | |
| B. | 在1.00mol H2O2中,核外电子总数为10×6.02×1023个 | |
| C. | 过氧化氢既有氧化性又有还原性 | |
| D. | 3.4g过氧化氢中含有6.02×1022个原子 |
1.化学在生产和日常生活中有着重要的应用.下列说法不正确的是( )
| A. | 明矾水解形成的Al(OH)3胶体能吸附水中悬浮,可用于水的净化 | |
| B. | 在海轮外壳上镶入锌块,可减缓船体的腐蚀速率 | |
| C. | 工业制铝的原料是AlCl3,可以降低能耗 | |
| D. | MgO的熔点很高,可用于制作耐高温材料 |

 ,反应类型为加成反应.
,反应类型为加成反应. ,该酯化反应生成的产物在一定条件下可以发生加聚反应得到有机玻璃,有机玻璃的结构简式为
,该酯化反应生成的产物在一定条件下可以发生加聚反应得到有机玻璃,有机玻璃的结构简式为 .
.