题目内容
1.化学在生产和日常生活中有着重要的应用.下列说法不正确的是( )| A. | 明矾水解形成的Al(OH)3胶体能吸附水中悬浮,可用于水的净化 | |
| B. | 在海轮外壳上镶入锌块,可减缓船体的腐蚀速率 | |
| C. | 工业制铝的原料是AlCl3,可以降低能耗 | |
| D. | MgO的熔点很高,可用于制作耐高温材料 |
分析 A、根据明矾净水的原理是铝离子水解生成的氢氧化铝净水来分析;
B、根据原电池的工作原理和应用来回答,锌和铁在电解质溶液中形成原电池反应,锌做负极;
C、根据氯化铝为共价化合物分析;
D、根据氧化镁是熔点高的物理性质来分析其应用.
解答 解:A、明矾净水的原理是:Al3++3H2O=Al(OH)3(胶体)+3H+,利用Al(OH)3(胶体)的吸附性进行净水,故A正确;
B、因为轮船主要用铁造外壳,铁在海水中易被腐蚀,镀上比铁活泼的锌,形成原电池,锌作负极,失去电子先被腐蚀,从而起到保护铁的作用,从而可减缓船体的腐蚀速率,故B正确;
C、氯化铝为共价化合物,熔融不能电离,工业制铝的原料是Al2O3,故C错误;
D、氧化镁的熔点是2852℃,可用于制作耐高温材料,故D正确;
故选:C.
点评 本题主要考查了物质的水解反应以及水解反应的用途、常见物质在生产生活中的具体用途、常见物质的制备及发生的化学反应方程式等方面的知识,是一道综合题目.

练习册系列答案
 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案
相关题目
19.下列物质的变化,必须通过盐溶液才能反应实现的是( )
| A. | CuO→CuCl2 | B. | K2SO4→KCl | C. | CaCO3→CaCl2 | D. | Mg(OH)2→MgCl2 |
12.下列说法正确的是( )
| A. | 按系统命名法,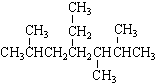 的名称为2,5,6-三甲基-4-乙基庚烷 的名称为2,5,6-三甲基-4-乙基庚烷 | |
| B. | 常压下,正戊烷、异戊烷、新戊烷的沸点依次升高 | |
| C. | “糖类”物质均具有明显的甜味 | |
| D. | 1mol的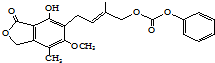 最多能与含5mol NaOH的水溶液完全反应 最多能与含5mol NaOH的水溶液完全反应 |
16.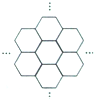 据报道,科学家己经研制出世界上最薄的材料一-碳膜片,其厚度只有一根头发的二十万分之一.如图所示,这种碳膜片状如蜂巢,是由碳原子构成的六边形单元向外延展而成,下列有关碳膜片的说法中,正确的是( )
据报道,科学家己经研制出世界上最薄的材料一-碳膜片,其厚度只有一根头发的二十万分之一.如图所示,这种碳膜片状如蜂巢,是由碳原子构成的六边形单元向外延展而成,下列有关碳膜片的说法中,正确的是( )
 据报道,科学家己经研制出世界上最薄的材料一-碳膜片,其厚度只有一根头发的二十万分之一.如图所示,这种碳膜片状如蜂巢,是由碳原子构成的六边形单元向外延展而成,下列有关碳膜片的说法中,正确的是( )
据报道,科学家己经研制出世界上最薄的材料一-碳膜片,其厚度只有一根头发的二十万分之一.如图所示,这种碳膜片状如蜂巢,是由碳原子构成的六边形单元向外延展而成,下列有关碳膜片的说法中,正确的是( )| A. | 碳膜片属于碳元素的同素异形体 | |
| B. | 碳膜片与C60是同一种物质 | |
| C. | 碳膜片属于人工合成的有机高分子材料 | |
| D. | 碳膜片在氧气中完全燃烧的产物和碳在氧气中完全燃烧的产物不同 |
6.工厂经常用浓氯水检验管道是否漏氯气,其反应为:3Cl2+8NH3═6NH4Cl+N2,如果观察到产生白烟现象,则说明管道漏气.关于该反应的有关判断错误的( )
| A. | 该反应属于置换反应 | B. | 该反应的还原剂是NH3 | ||
| C. | Cl2的氧化性小于N2 | D. | 被氧化的NH3占参加反应NH3的1/4 |
10.阿伏伽德罗常数约为6.02×1023mol-1,下列叙述中不正确的是( )
| A. | 0.1 mol OH-含有6.02×1023个电子 | |
| B. | 氯化氢气体的摩尔质量等于6.02×1023氯气分子和6.02×1023个氢分子的质量之和 | |
| C. | 1 mol醋酸的质量与6.02×1023个醋酸分子的质量相等 | |
| D. | 28 g氮气所含的原子数目为12.04×1023 |
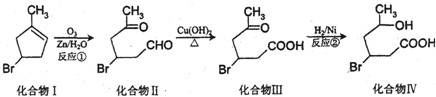
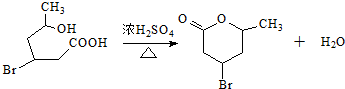 .
.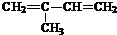 (2-甲基-1,3-丁二烯)发生类似①的反应,得到有机物VI和VII,结构简式分别是为
(2-甲基-1,3-丁二烯)发生类似①的反应,得到有机物VI和VII,结构简式分别是为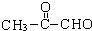 、HCHO.
、HCHO.