题目内容
10.干冰晶胞是一个面心立方体,在该晶体中每个顶角各有1个二氧化碳分子,每个面心各有一个二氧化碳分子,实验测得25℃时干冰晶体的晶胞边长为acm,其摩尔质量为Mg/mol,阿伏加德罗常数为NA,则该干冰晶体的密度为(单位:g/cm3).( )| A. | $\frac{14M}{{a}^{3}{N}_{A}}$ | B. | $\frac{M}{{a}^{3}{N}_{A}}$ | C. | $\frac{2M}{{a}^{3}{N}_{A}}$ | D. | $\frac{4M}{{a}^{3}{N}_{A}}$ |
分析 干冰晶胞中二氧化碳分子个数=8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,晶胞边长为acm,晶胞体积=a3cm3,晶胞密度=$\frac{\frac{M}{{N}_{A}}×4}{V}$,据此分析解答.
解答 解:干冰晶胞中二氧化碳分子个数=8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,晶胞边长为acm,晶胞体积=a3cm3,晶胞密度=$\frac{\frac{M}{{N}_{A}}×4}{V}$=$\frac{\frac{M}{{N}_{A}}×4}{{a}^{3}}$g/cm3=$\frac{4M}{{a}^{3}{N}_{A}}$g/cm3,故选D.
点评 本题考查晶胞计算,为高频考点,侧重考查学生空间想象能力、计算能力,明确密度公式中各个字母含义是解本题关键,题目难度不大.

练习册系列答案
相关题目
20.二甲醚是一种重要的清洁燃料,也可替代氟利昂作制冷剂等,对臭氧层无破坏作用.工业上可利用煤的气化产物(水煤气)合成二甲醚.请回答下列问题:
(1)煤的气化的主要化学反应方程式为:C+H2O$\frac{\underline{\;高温\;}}{\;}$CO+H2.
(2)煤的气化过程中产生的有害气体H2S用Na2CO3溶液吸收,生成两种酸式盐,该反应的化学方程式为:Na2CO3+H2S═NaHCO3+NaHS.
(3)利用水煤气合成二甲醚的三步反应如下:
①2H2(g)+CO(g)?CH3OH(g);△H=-90.8kJ•mol-1
②2CH3OH(g)?CH3OCH3(g)+H2O(g);△H=-23.5kJ•mol-1
③CO(g)+H2O(g)?CO2(g)+H2(g);△H=-41.3kJ•mol-1
总反应:3H2(g)+3CO(g)?CH3OCH3(g)+CO2 (g)的△H=-246.4kJ•mol-1;
若总反应平衡后,要提高CO的转化率,可以采取的措施是ce(填字母代号)
a.升温 b.加催化剂 c.减少CO2的浓度 d.增加CO的浓度 e.分离出二甲醚
(4)已知反应②2CH3OH(g)?CH3OCH3(g)+H2O(g)某温度下平衡常数为400.此温度下,在密闭容器中加入CH3OH,某时刻测得各组分的浓度如表:
①比较此时正、逆反应速率的大小:v正> v逆 (填“>”、“<”或“=”).
②若加入CH3OH后,经10min达到平衡,此时c(CH3OH)=0.04mol/L;该时间内反应速率v(CH3OH)=0.16 mol/(L•min).
(5)2H2+CO?CH3OH的催化剂为Cu2O,据研究,需要向反应体系中额外加入少量CO2,原因是:Cu2O+CO?2Cu+CO2(用化学方程式表示).
(1)煤的气化的主要化学反应方程式为:C+H2O$\frac{\underline{\;高温\;}}{\;}$CO+H2.
(2)煤的气化过程中产生的有害气体H2S用Na2CO3溶液吸收,生成两种酸式盐,该反应的化学方程式为:Na2CO3+H2S═NaHCO3+NaHS.
(3)利用水煤气合成二甲醚的三步反应如下:
①2H2(g)+CO(g)?CH3OH(g);△H=-90.8kJ•mol-1
②2CH3OH(g)?CH3OCH3(g)+H2O(g);△H=-23.5kJ•mol-1
③CO(g)+H2O(g)?CO2(g)+H2(g);△H=-41.3kJ•mol-1
总反应:3H2(g)+3CO(g)?CH3OCH3(g)+CO2 (g)的△H=-246.4kJ•mol-1;
若总反应平衡后,要提高CO的转化率,可以采取的措施是ce(填字母代号)
a.升温 b.加催化剂 c.减少CO2的浓度 d.增加CO的浓度 e.分离出二甲醚
(4)已知反应②2CH3OH(g)?CH3OCH3(g)+H2O(g)某温度下平衡常数为400.此温度下,在密闭容器中加入CH3OH,某时刻测得各组分的浓度如表:
| 物质 | CH3OH | CH3OCH3 | H2O |
| 浓度/(mol/L) | 0.44 | 0.6 | 0.6 |
②若加入CH3OH后,经10min达到平衡,此时c(CH3OH)=0.04mol/L;该时间内反应速率v(CH3OH)=0.16 mol/(L•min).
(5)2H2+CO?CH3OH的催化剂为Cu2O,据研究,需要向反应体系中额外加入少量CO2,原因是:Cu2O+CO?2Cu+CO2(用化学方程式表示).
1.下列关于化学用语的表示正确的是( )
| A. | 过氧化钠电子式:Na${\;}_{•}^{•}$$\underset{\stackrel{••}{O}}{••}$${\;}_{•}^{•}$$\underset{\stackrel{••}{O}}{••}$${\;}_{•}^{•}$Na | |
| B. | 质子数35、中子数45的溴原子:${\;}_{35}^{80}$Br | |
| C. | 硫离子结构示意图: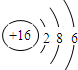 | |
| D. | 乙烯的结构简式:C2H4 |
18.下列各组离子能在溶液中大量共存的是( )
| A. | K+、H+、SO42-、OH- | B. | Na+、H+、CO32-、Cl- | ||
| C. | Na+、Ca2+、NO3-、CO32- | D. | Na+、K+、Cl-、SO42- |
15.己烯雌酚是一种激素类药物,结构如图,下列有关叙述中正确的是( )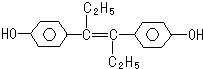

| A. | 遇FeCl3溶液显紫色,因为该物质与苯酚属于同系物 | |
| B. | 1mol该有机物可以与5mol Br2发生反应 | |
| C. | 可分别与NaOH和NaHCO3发生反应 | |
| D. | 该有机物分子中,所有原子可能共平面 |
19.下列物质的变化,必须通过盐溶液才能反应实现的是( )
| A. | CuO→CuCl2 | B. | K2SO4→KCl | C. | CaCO3→CaCl2 | D. | Mg(OH)2→MgCl2 |
12.下列说法正确的是( )
| A. | 按系统命名法,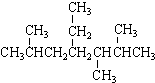 的名称为2,5,6-三甲基-4-乙基庚烷 的名称为2,5,6-三甲基-4-乙基庚烷 | |
| B. | 常压下,正戊烷、异戊烷、新戊烷的沸点依次升高 | |
| C. | “糖类”物质均具有明显的甜味 | |
| D. | 1mol的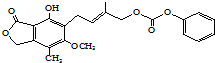 最多能与含5mol NaOH的水溶液完全反应 最多能与含5mol NaOH的水溶液完全反应 |