题目内容
15.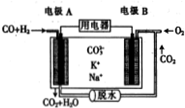 水煤气(CO、H2)作燃料电池的燃料可提高利用率和减少碳的排放,以水煤气为燃料的某熔融碳酸盐燃料电池的工作原理如图所示.下列说法正确的( )
水煤气(CO、H2)作燃料电池的燃料可提高利用率和减少碳的排放,以水煤气为燃料的某熔融碳酸盐燃料电池的工作原理如图所示.下列说法正确的( )| A. | 电极A上H2参与的电极反应为H2+2OH--2e-=2H2O | |
| B. | 电极B上发生的电极反应为O2+2CO2+4e-=2CO32- | |
| C. | 电池工作时,K+向电极A移动 | |
| D. | 若电极B上消耗2molO2,则电极A上消耗4molCO |
分析 原电池工作时,CO和H2失电子在负极反应,则A为负极,CO和H2被氧化生成二氧化碳和水,正极B上为氧气得电子生成CO32-,以此解答该题.
解答 解:A.A为负极,负极上CO和H2被氧化生成二氧化碳和水,电极A反应为:H2+CO+2CO32--4e-=H2O+3CO2,故A错误;
B.B为正极,正极为氧气得电子生成CO32-,反应为O2+2CO2+4e-=2CO32-,故B正确;
C.电池工作时,阳离子向正极移动,K+向电极B移动,故C错误;
D.电极A反应为H2+CO+2CO32--4e-=H2O+3CO2,B极反应为O2+2CO2+4e-=2CO32-,电极B上消耗2molO2,转移8mol电子,则电极A上消耗2molCO,故D错误.
故选B.
点评 本题考查了化学电源新型电池,明确原电池中物质得失电子、离子流向即可解答,难点是电极反应式书写,要根据电解质确定正负极产物,难度中等.

练习册系列答案
相关题目
5.铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,且不会造成二次污染.已知高铁酸盐热稳定性差,高铁酸盐在碱性环境中比酸性环境中相对稳定.工业上用湿法制备高铁酸钾的基本流程如图所示:

下列有关说法不正确的是( )

下列有关说法不正确的是( )
| A. | 控制反应温度30℃以下的原因是防止生成的K2FeO4发生分解 | |
| B. | 结晶过程中加入浓KOH溶液其作用是增大K+浓度,促进K2FeO4晶体析出 | |
| C. | 滤液2中阳离子可通过焰色反应检验确定 | |
| D. | 湿法制备高铁酸钾,也可以在Fe(OH)3料浆中直接通入足量氯气 |
6.某研究性学习小组讨论甲、乙、丙、丁四种仪器装置的有关用法,其中不合理的是( )
| A. |  装置:可用来证明碳酸的酸性比硅酸强 | |
| B. |  装置:可用来检验二氧化硫气体 | |
| C. |  装置:用图示的方法不能检查此装置的气密性 | |
| D. |  装置:先从①口进气集满二氧化碳,再从②口进气,可收集氢气 |
3.今有甲、乙、丙、丁、戊5种物质,在一定条件下,它们能按图方式进行转化:

其推断正确的是( )

其推断正确的是( )
| 选项 | 甲 | 乙 | 丙 | 丁 | 戊 |
| A | NH3 | O2 | NO | H2O | NO2 |
| B | Mg | CO2 | C | MgO | CO |
| C | C | H2O | CO | H2 | C2H5OH |
| D | FeBr2 | Cl2 | FeCl2 | Br2 | FeCl3 |
| A. | A | B. | B | C. | C | D. | D |
10.下列有关有机物的说法正确的是( )
| A. | C8H10含苯环的烃同分异构体有3种 | |
| B. | 丙烯酸(CH2=CHCOOH)和山梨酸(CH3CH=CHCH=CHCOOH)是同系物 | |
| C. | 油脂在一定条件下水解成高级脂肪酸和甘油,称为皂化反应 | |
| D. | 青蒿素是抗疟疾特效药,结构如图所示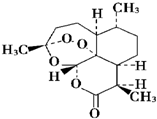 ,有酯基、过氧键和醚键,不溶于水,易溶于氯仿、丙酮等,可以用乙醚从植物中提取,能够发生水解反应,具有强氧化性 ,有酯基、过氧键和醚键,不溶于水,易溶于氯仿、丙酮等,可以用乙醚从植物中提取,能够发生水解反应,具有强氧化性 |
20.某有机物X的结构简式如图所示,则下列有关说法中正确的是( )
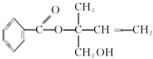

| A. | X的分子式为C12H16O3 | |
| B. | 可用酸性高锰酸钾溶液区分苯和X | |
| C. | 若单键可以旋转,有机物X中一定在同一平面上的碳原子数为8 | |
| D. | 在Ni作催化剂的条件下,1 molX最多只能与1molH2加成 |
4.下列离子方程式正确的是( )
| A. | 硫化钠溶液跟稀硝酸相混合:S2-+2H+=H2S↑ | |
| B. | 在亚硝酸钡沉淀中加入稀硝酸后,沉淀不溶解:3BaSO3+2H++2NO3-=3BaSO4+2NO↑+H2O | |
| C. | 碳酸钠溶液中通入过量SO2:2CO32-+SO2+H2O=2HCO3-+SO32- | |
| D. | 硫酸氢钠溶液与氢氧化钡溶液以等物质的量混合:SO42-+2H++Ba2++2OH-=BaSO4↓+2H2O |

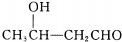
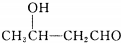 $\stackrel{△}{→}$CH3CH=CHCHO+H2O
$\stackrel{△}{→}$CH3CH=CHCHO+H2O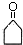 ,G中官能团的名称为碳碳双键、酯基.
,G中官能团的名称为碳碳双键、酯基. ,反应类型为加成反应.
,反应类型为加成反应.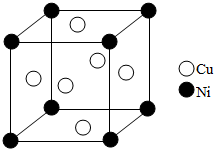 东晋《华阳国志•南中志》卷四中已有关于白铜的记载,云南镍白铜(铜镍合金)闻名中外,曾主要用于造币,亦可用于制作仿银饰品.回答下列问题:
东晋《华阳国志•南中志》卷四中已有关于白铜的记载,云南镍白铜(铜镍合金)闻名中外,曾主要用于造币,亦可用于制作仿银饰品.回答下列问题: