题目内容
10. 东晋《华阳国志•南中志》卷四中已有关于白铜的记载,云南镍白铜(铜镍合金)闻名中外,曾主要用于造币,亦可用于制作仿银饰品.回答下列问题:
东晋《华阳国志•南中志》卷四中已有关于白铜的记载,云南镍白铜(铜镍合金)闻名中外,曾主要用于造币,亦可用于制作仿银饰品.回答下列问题:(1)镍元素基态原子的电子排布式为1s22s22p63s23p63d84s2,3d能级上的未成对电子数为2.
(2)硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液.
①[Ni(NH3)6]SO4中阴离子的立体构型是正四面体.
②在[Ni(NH3)6]SO4中Ni2+与NH3之间形成的化学键称为配位键,提供孤电子对的成键原子是N.
③氨的沸点高于(填“高于”或“低于”)膦(PH3),原因是氨气分子之间形成氢键,分子间作用力更强;氨是极性分子(填“极性”或“非极性”),中心原子的轨道杂化类型为sp3.
(3)单质铜及镍都是由金属键形成的晶体;元素铜与镍的第二电离能分别为:ICu=1958kJ•mol-1、INi=1753kJ•mol-1,ICu>INi的原因是Cu+电子排布呈半充满状态,比较稳定,失电子需要能量高,第二电离能数值大.
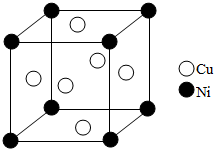
(4)某镍白铜合金的立方晶胞结构如图所示.
①晶胞中铜原子与镍原子的数量比为3:1.
②若合金的密度为d g•cm-3,晶胞参数a=$\root{3}{\frac{251}{d{N}_{A}}}$×107nm.
分析 (1)Ni元素原子核外电子数为28,结合能量最低原理书写核外电子排布式;
(2)①SO42-中S原子的孤电子对数=$\frac{6+2-2×4}{2}$=0,价层电子对数=4+0=4;
②Ni2+提供空轨道,NH3中N原子含有孤电子对,二者之间形成配位键;
③PH3分子之间为范德华力,氨气分子之间形成氢键,增大了物质的沸点;NH3分子为三角锥形结构,分子中正负电荷重心不重合,N原子有1对孤对电子,形成3个N-H键,杂化轨道数目为4;
(3)单质铜及镍都属于金属晶体;Cu+的外围电子排布为3d10,Ni+的外围电子排布为3d84s1,Cu+的核外电子排布更稳定;
(4)①根据均摊法计算晶胞中Ni、Cu原子数目;
②属于面心立方密堆积,结合晶胞中原子数目表示出晶胞质量,再结合m=ρV可以计算晶胞棱长.
解答 解:(1)Ni元素原子核外电子数为28,核外电子排布式为1s22s22p63s23p63d84s2,3d能级上的未成对电子数为2,
故答案为:1s22s22p63s23p63d84s2;2;
(2)①SO42-中S原子的孤电子对数=$\frac{6+2-2×4}{2}$=0,价层电子对数=4+0=4,离子空间构型为正四面体,
故答案为:正四面体;
②Ni2+提供空轨道,NH3中N原子含有孤电子对,二者之间形成配位键,
故答案为:配位键;N;
③PH3分子之间为范德华力,氨气分子之间形成氢键,分子间作用力更强,增大了物质的沸点,故氨气的沸点高于PH3分子的,
NH3分子为三角锥形结构,分子中正负电荷重心不重合,属于极性分子,N原子有1对孤对电子,形成3个N-H键,杂化轨道数目为4,氮原子采取sp3杂化,
故答案为:高于;氨气分子之间形成氢键,分子间作用力更强;极性;sp3;
(3)单质铜及镍都属于金属晶体,都是由金属键形成的晶体;Cu+的外围电子排布为3d10,Ni+的外围电子排布为3d84s1,Cu+的核外电子排布更稳定,失去第二个电子更难,元素铜的第二电离能高于镍的,
故答案为:金属;Cu+电子排布呈半充满状态,比较稳定,失电子需要能量高,第二电离能数值大;
(4)①晶胞中Ni处于顶点,Cu处于面心,则晶胞中Ni原子数目为8×$\frac{1}{8}$=1、Cu原子数目=6×$\frac{1}{2}$=3,故Cu与Ni原子数目之比为3:1,
故答案为:3:1;
②属于面心立方密堆积,晶胞质量质量为$\frac{59+64×3}{{N}_{A}}$g,则$\frac{59+64×3}{{N}_{A}}$g=d g•cm-3×(a×10-7 cm)3,解得a=$\root{3}{\frac{251}{d{N}_{A}}}$×107.
故答案为:$\root{3}{\frac{251}{d{N}_{A}}}$×107.
点评 本题是对物质结构与性质的考查,涉及核外电子排布、空间构型与杂化方式判断、配位键、氢键、电离能、晶胞计算等,是对物质结构主干知识的综合考查,需要学生具备扎实的基础.

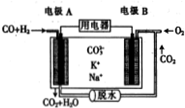 水煤气(CO、H2)作燃料电池的燃料可提高利用率和减少碳的排放,以水煤气为燃料的某熔融碳酸盐燃料电池的工作原理如图所示.下列说法正确的( )
水煤气(CO、H2)作燃料电池的燃料可提高利用率和减少碳的排放,以水煤气为燃料的某熔融碳酸盐燃料电池的工作原理如图所示.下列说法正确的( )| A. | 电极A上H2参与的电极反应为H2+2OH--2e-=2H2O | |
| B. | 电极B上发生的电极反应为O2+2CO2+4e-=2CO32- | |
| C. | 电池工作时,K+向电极A移动 | |
| D. | 若电极B上消耗2molO2,则电极A上消耗4molCO |
| A. | 2-甲基丁烷也称异丁烷 | B. | 由乙烯生成乙醇属于加成反应 | ||
| C. | C4H9Cl有3种同分异构体 | D. | 油脂和蛋白质都属于高分子化合物 |
| A. | 第一阶段中阴、阳两极产生的气体混合引燃后,恰好完全反应得到HCl | |
| B. | 阴极自始至终只产生H2 | |
| C. | 电解过程中,溶液的pH不断增大,最后等于7 | |
| D. | 电解过程中,Na+和SO42-的物质的量保持不变 |
| A. | 向0.1mol•L-1 CH3COOH溶液中加入少量水,溶液中$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$减小 | |
| B. | 将CH3COONa溶液从20℃升温至30℃,溶液中$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)•c(O{H}^{-})}$增大 | |
| C. | 向盐酸中加入氨水至中性,溶液中$\frac{c(N{{H}_{4}}^{+})}{c(C{l}^{-})}$>1 | |
| D. | 向AgCl、AgBr的饱和溶液中加入少量AgNO3,溶液中$\frac{c(C{l}^{-})}{c(B{r}^{-})}$不变 |
| A. | AlCl3 | B. | KOH | C. | HCl | D. | H2O |
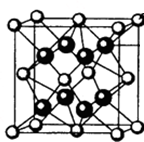 M、R、X、Y为原子序数依次增大的短周期主族元素,Z是一种过渡元素.M基态原子L层中p轨道电子数是s电子数的2倍,R是同周期元素中最活泼的金属元素,X和M形成的一种化合物是引起酸雨的主要大气污染物,Z的基态原子4s和3d轨道半充满.请回答下列问题:
M、R、X、Y为原子序数依次增大的短周期主族元素,Z是一种过渡元素.M基态原子L层中p轨道电子数是s电子数的2倍,R是同周期元素中最活泼的金属元素,X和M形成的一种化合物是引起酸雨的主要大气污染物,Z的基态原子4s和3d轨道半充满.请回答下列问题: