题目内容
13.久置空气中不会变质的物质是( )| A. | 亚硫酸(H2SO3) | B. | 漂白粉[有效成份Ca(C1O)2] | ||
| C. | 食盐(NaCl) | D. | 烧碱(NaOH) |
分析 久置空气中不会变质的物质,与空气中的氧气、水、二氧化碳等均不反应,且不分解,以此来解答.
解答 解:A.亚硫酸(H2SO3)易被氧气氧化而变质,故A不选;
B.漂白粉与空气中的水、二氧化碳反应生成HClO,且HClO易分解而变质,故B不选;
C.食盐性质稳定,不分解,不与空气中的物质反应,故C选;
D.烧碱易吸收空气中的二氧化碳而变质,故D不选;
故选C.
点评 本题考查物质的性质,为高频考点,把握物质的性质、发生的反应为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
相关题目
3.下列说法正确的是( )
| A. | 1mol N2 的质量是14g | B. | H2SO4的摩尔质量是98 g | ||
| C. | H2O的摩尔质量是18 g/mol | D. | 1mol HCl的质量是36.5 g/mol |
4.下列离子方程式书写正确的是( )
| A. | 碳酸钙与盐酸反应 C032-+2H+═C02↑+H20 | |
| B. | KI溶液中通氯气 2Iˉ+C12═2C1?+I2 | |
| C. | 氯气通入氯化亚铁溶液中:Fe2++Cl2═Fe3++2Cl- | |
| D. | 硫酸与氢氧化钡溶液反应 H十+OHˉ═H2O |
1.甲苯苯环上的三溴代物有( )
| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
8.一定温度下在一容积不变的密闭容器中发生可逆反应2X(g)═Y(g)+Z(s),以下不能说明该反应达到化学平衡状态的是( )
| A. | v正(X)=2v正(Y) | |
| B. | 单位时间内生成1 mol Y的同时生成2molX | |
| C. | 混合气体的密度不再变化 | |
| D. | 反应容器中Y的质量分数不变 |
5.常温下,将某一元酸HA和NaOH溶液等体积混合,实验信息如表:
下列判断不正确的是( )
| 实验编号 | c(HA)/mol•L-1 | c(NaOH)/mol•L-1 | 反应后溶液pH |
| 甲 | 0.1 | 0.1 | pH=9 |
| 乙 | c1 | 0.2 | pH=7 |
| A. | 0.1mol•L-1的HA溶液中由水电离出的c(H+)>1×10-13mol/L | |
| B. | c1一定大于0.2 mol•L-1 | |
| C. | 甲反应后的溶液中:HA占含A-微粒总数的0.01% | |
| D. | 乙反应后的溶液中:c(Na+)<c(HA)+c(A-) |
2.下列离子方程式中,正确的是( )
| A. | Na2O2与H2O反应:Na2O2+H2O═2Na++2OH-+O2↑ | |
| B. | AlCl3溶液中滴加过量的氨水:Al3++4 NH3•H2O═AlO2-+2H2O+4NH4+ | |
| C. | 铜与浓硝酸反应:Cu+4H++2NO3-═Cu2++2NO2↑+2H2O | |
| D. | 向小苏打溶液中滴入醋酸:CO32-+2CH3COOH═CO2↑+H2O+2CH3COO- |
3.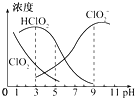 亚氯酸钠在溶液中可生成ClO2、HClO2、ClO2-、Cl-等,其中HClO2和ClO2都具有漂白作用 但ClO2是有毒的气体,25℃时各离子浓度随pH变化如图所示下列分析错误的是( )
亚氯酸钠在溶液中可生成ClO2、HClO2、ClO2-、Cl-等,其中HClO2和ClO2都具有漂白作用 但ClO2是有毒的气体,25℃时各离子浓度随pH变化如图所示下列分析错误的是( )
 亚氯酸钠在溶液中可生成ClO2、HClO2、ClO2-、Cl-等,其中HClO2和ClO2都具有漂白作用 但ClO2是有毒的气体,25℃时各离子浓度随pH变化如图所示下列分析错误的是( )
亚氯酸钠在溶液中可生成ClO2、HClO2、ClO2-、Cl-等,其中HClO2和ClO2都具有漂白作用 但ClO2是有毒的气体,25℃时各离子浓度随pH变化如图所示下列分析错误的是( )| A. | 25℃时HClO2的电离平衡常数Ka=10-6 | |
| B. | 使用漂白剂的最佳pH为3 | |
| C. | 25℃时,等浓度的HClO2溶液和NaClO2溶液等体积混合混合溶液中c(HClO2)+2c(H+)=c(ClO2-)+2c(OH-) | |
| D. | 25℃时 用0.1000mol/LNaOH溶液滴定20.00ml某未知浓度的HClO2溶液 当滴入NaOH溶液体积为20.00ml时溶液呈中性 则HClO2溶液的实际浓度为0.11mol/L |