题目内容
17.下列说法不符合人与自然和谐相处的是( )| A. | 很多城市对废旧电池进行回收处理 | |
| B. | 有些国家对聚乙烯等塑料垃圾进行了深埋或者倾倒入大海处理 | |
| C. | 不少地区正在使用沼气,太阳能,风能等能源替代传统的煤炭 | |
| D. | 许多地方政府出台相关法规来保护生物物种多样性 |
分析 做到人与自然和谐相处,应减少污染物的排放,积极处理垃圾,减少化石能源的使用,饱和生物物种,以此解答该题.
解答 解:A.对废旧电池进行回收处理可以减少对环境的污染,符合人与自然和谐相处,故A正确;
B.将塑料垃圾埋入地下或倾倒入海,仍会产生污染,不符合人与自然和谐相处,故B错误;
C.使用沼气、太阳能、风能等代替煤炭,减少污染物的排放,符合人与自然和谐相处,故C正确;
D.保护生物物种多样性,符合人与自然和谐相处,故D正确.
故选B.
点评 本题考查化学与环境,为高频考点,侧重于化学与生活、生产和环境的考查,有利于培养学生良好的科学素养,提高学习的积极性,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
8.在密闭容器中反应aR(g)+bQ(g)?cX(g)+dY(g)达平衡后,保持温度不变,将容器体积增加一倍,达到新平衡时,X浓度是原来的60%,则下列说法正确的是( )
| A. | 平衡向正反应方向移动了 | B. | 物质R的转化率减少了 | ||
| C. | 物质X的质量分数减少了 | D. | a+b<c+d |
5.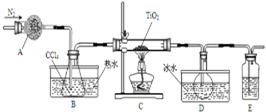 实验室利用反应TiO2(s)+CCl4(g)$\frac{\underline{\;\;△\;\;}}{\;}$TiCl4(g)+CO2(g),在无水无氧条件下制备TiCl4,实验装置示意图如下,有关物质性质如表.
实验室利用反应TiO2(s)+CCl4(g)$\frac{\underline{\;\;△\;\;}}{\;}$TiCl4(g)+CO2(g),在无水无氧条件下制备TiCl4,实验装置示意图如下,有关物质性质如表.
(1)仪器A的名称是干燥管,装置E中的试剂是浓硫酸.反应开始前依次进行如下操作:组装仪器、检验气密性、加装药品、通N2一段时间后点燃酒精灯.
(2)反应结束后的操作包括:a停止通N2 b熄灭酒精灯 c冷却至室温.正确的顺序为bca(填序号).选择这种顺序的理由是防止倒吸或避免生成的产物在受热情况下与氧气反应(二者任写其一均给分);欲分离D中的液态混合物,所采用操作的名称是蒸馏.
 实验室利用反应TiO2(s)+CCl4(g)$\frac{\underline{\;\;△\;\;}}{\;}$TiCl4(g)+CO2(g),在无水无氧条件下制备TiCl4,实验装置示意图如下,有关物质性质如表.
实验室利用反应TiO2(s)+CCl4(g)$\frac{\underline{\;\;△\;\;}}{\;}$TiCl4(g)+CO2(g),在无水无氧条件下制备TiCl4,实验装置示意图如下,有关物质性质如表.| 物质 | 熔点/℃ | 沸点/℃ | 其他 |
| CCl4 | -23 | 76 | 与TiCl4互溶 |
| TiCl4 | -25 | 136 | 遇潮湿空气产白雾 |
(2)反应结束后的操作包括:a停止通N2 b熄灭酒精灯 c冷却至室温.正确的顺序为bca(填序号).选择这种顺序的理由是防止倒吸或避免生成的产物在受热情况下与氧气反应(二者任写其一均给分);欲分离D中的液态混合物,所采用操作的名称是蒸馏.
12.下列叙述正确的是( )
| A. | 单体的质量之和就是所生成高聚物的质量 | |
| B. | 氨基酸能发生的反应有:酯化反应、水解反应、成肽反应、与酸或碱的中和反应 | |
| C. | 天然蛋白质的水解产物为α-氨基酸,遇饱和硫酸铵或硫酸钠溶液会发生变性 | |
| D. | 淀粉和纤维素因聚合度不同所以他们不是同分异构体 |
2.在温度t1和t2(t2>t1)下,X2(g)和H2反应生成HX的平衡常数如下表:
下列说法不正确的是( )
| 化学方程式 | K(t1) | K(t2) | |
| ① | Br2 (g)+H2(g)?2HBr(g) | 5.6×107 | 9.3×106 |
| ② | I2 (g)+H2 (g)?2HI(g) | 43 | 34 |
| A. | ①和②均是放热反应 | |
| B. | 相同条件下,平衡体系中HX所占的比例:①>② | |
| C. | 其他条件不变时,增大压强可提高X2的平衡转化率 | |
| D. | 其他条件不变时,升高温度可加快HX的生成速率 |
9.2014年初全国各地多个城市都遭遇“十面霾伏”,造成“阴霾天”的主要根源之一是汽车尾气和燃煤尾气排放出来的固体小颗粒.将汽车尾气通过排气管加装催化装置,可有效减少CO和NO的排放,催化装置内发生的反应为:2NO+2CO$\stackrel{催化剂}{?}$2CO2+N2,已知该反应属于放热反应.下列关于此反应的说法不正确的是( )
| A. | 该反应会放出热量 | |
| B. | 每生成1mol N2,转化电子数为4mol | |
| C. | 等物质的量N2和CO质量相同 | |
| D. | 该反应不需要催化剂常温下也能发生 |
6.在容积为2L的容器内,发生反应2A(s)+3B(g)?2C(g)+D(g),起始时充入3molA和2.5molB混合气体;经过5min达到平衡,生成0.5molD,下列说法正确的是( )
| A. | 若单位时间内生成的B和D的物质的量之比为3:1,则体系处于平衡状态 | |
| B. | C的平衡浓度为1mol/L | |
| C. | 5min内B的平均消耗速率为0.3mol/(L•min) | |
| D. | 平衡后,增大压强,平衡向正反应方向移动 |
7.下列电离方程式中,正确的是( )
| A. | H2SO4=H2++SO42- | B. | Ba(OH)2=Ba2++OH- | ||
| C. | KClO3=K++ClO3- | D. | MgSO4═Mg+2+SO42- |