题目内容
8.在密闭容器中反应aR(g)+bQ(g)?cX(g)+dY(g)达平衡后,保持温度不变,将容器体积增加一倍,达到新平衡时,X浓度是原来的60%,则下列说法正确的是( )| A. | 平衡向正反应方向移动了 | B. | 物质R的转化率减少了 | ||
| C. | 物质X的质量分数减少了 | D. | a+b<c+d |
分析 先假设体积增加一倍时若平衡未移动,X的浓度应为原来的50%,实际平衡时X的浓度是原来的60%,比假设大,说明平衡向生成X的方向移动,即减小压强平衡向逆反应方向移动,则a+b>c+d,以此解答该题.
解答 解:A.将容器体积增加一倍,达到新平衡时,X浓度是原来的60%,由以上分析可知平衡向正反应方向移动了,故A正确;
B.平衡正向移动,则R的转化率增大,故B错误;
C.平衡正向移动,X的质量分数增大,故C错误;
D.由以上分析可知a+b>c+d,故D错误.
故选A.
点评 本题考查了化学平衡的影响因素分析判断,为高频考点,侧重于学生的分析能力的考查,主要是化学平衡移动原理的实质理解应用,题目难度中等.

练习册系列答案
相关题目
12.下列说法正确的是( )
| A. | 不能发生丁达尔效应的分散系是溶液 | |
| B. | 将1 L 2 mol/L的FeCl3溶液制成胶体后,其中含有氢氧化铁胶粒数为2NA | |
| C. | 纳米粒子的大小与胶体粒子相当,但纳米粒子的体系不一定是胶体 | |
| D. | 将饱和FeCl3溶液加热至沸腾,制得Fe(OH)3胶体 |
19.在某合成氨厂的合成氨反应中,测得合成塔入口处气体N2、H2、NH3的体积比为6:18:1,出口处N2、H2、NH3的体积比为9:27:8,则N2的转化率为( )
| A. | 75% | B. | 50% | C. | 25% | D. | 20% |
16.下列反应可以制备MgO;MgSO4(s)+CO(g)?MgO(s)+CO2(g)+SO2 (g);△H>0;在恒容条件下,达平衡后,增大(加入)x,重新平衡后,y也增大,符合此要求的组合是( )
| 选项 | A | B | C | D |
| x | 温度 | 压强 | SO2的浓度 | 加入催化剂 |
| y | 容器内气体密度 | CO2的体积分数 | 平衡常数 | CO的转化率 |
| A. | A | B. | B | C. | C | D. | D |
3.对于反应2A(g)+B(g)?2C(g)△H<0,下列图象正确的是( )
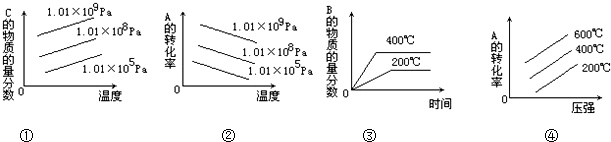

| A. | ①④ | B. | ②③ | C. | ①③ | D. | ②④ |
13.a1、a2分别为A在甲、乙两个恒温容器中建立平衡体系A(g)?2B(g)时的转化率,已知甲容器保持压强不变,乙容器保持容器体积不变.在温度不变的情况下,均增加A的物质的量,下列判断正确的是( )
| A. | a1、a2均减小 | B. | a1减小,a2增大 | C. | a1、不变,a2增大 | D. | a1不变,a2减小 |
20.一定温度时,在容积可变的密闭容器中发生反应:X(g)+Y(g)?Z(?)+W(g),达到平衡后容积为V,压缩容积至0.5V,并保持容积不变,再次达到平衡时,X的浓度为原平衡状态的1.8倍,下列叙述正确是( )
| A. | 该条件下Z是气态 | B. | 平衡常数K=$\frac{c(Z)•c(W)}{c(X)•c(Y)}$ | ||
| C. | 增加Z平衡逆向移动 | D. | 上述过程中X的转化率变大 |
17.下列说法不符合人与自然和谐相处的是( )
| A. | 很多城市对废旧电池进行回收处理 | |
| B. | 有些国家对聚乙烯等塑料垃圾进行了深埋或者倾倒入大海处理 | |
| C. | 不少地区正在使用沼气,太阳能,风能等能源替代传统的煤炭 | |
| D. | 许多地方政府出台相关法规来保护生物物种多样性 |