题目内容
20.加热时,Cu(ClO4)2的分解方式有以下两种:2Cu(ClO4)2═2CuO+7O2↑+2Cl2↑ 2Cu(ClO4)2═CuCl2+4O2↑
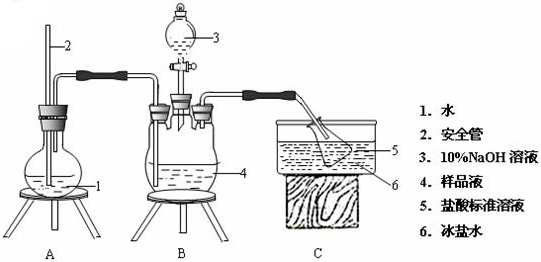
取一定质量的Cu(ClO4)2•6H2O样品,加热至某温度使其完全分解,得到7.75g固体.在常温下将生成的气体通过盛有NaOH溶液的洗气瓶时体积减少$\frac{1}{5}$.通过计算确定得到固体产物中CuO的质量百分含量(写出计算过程,结果保留两位小数)
分析 在常温下将生成的气体通过盛有NaOH溶液的洗气瓶时体积减少$\frac{1}{5}$,说明生成的气体的成分为氧气和氯气,体积减少的部分是氯气;混合气体中氯气占$\frac{1}{5}$,氧气占$\frac{4}{5}$,设生成氯气的物质的量为x,则生成的氧气的物质的量为4x,
2Cu(ClO4)2═2CuO+7O2↑+2Cl2↑
2 7 2
x 3.5x x
2Cu(ClO4)2═CuCl2+4O2↑
1 4
0.125x 4x-3.5x
根据得到固体的质量7.75g列式,x×80g/mol+0.125x×135g/mol=7.75g,进而求出CuO的质量,最后即可计算质量分数.
解答 解:设生成氯气的物质的量为x,则生成的氧气的物质的量为4x,
2Cu(ClO4)2═2CuO+7O2↑+2Cl2↑
2 7 2
x 3.5x x
2Cu(ClO4)2═CuCl2+4O2↑
1 4
0.125x 4x-3.5x
x×80g/mol+0.125x×135g/mol=7.75g,解得x=0.08mol,
固体产物中,m(CuO)=0.08mol×80g/mol=6.4g,
固体产物中CuO的质量分数为$\frac{6.4g}{7.75g}$×100%=82.58%,
答:固体产物中CuO的质量百分含量为82.58%.
点评 本题考查了混合物的计算,为高频考点,根据题干所给生成气体的比例,正确设置未知数并表示出CuO和CuCl2的质量之和等于7.75g最为关键,整体难度中等.

 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案| A. | 25.4ρ | B. | 12.7ρ | C. | 6.97ρ | D. | 6.35ρ |

| A. | 篮烷的分子式为C12H20 | |
| B. | 篮烷分子中存在2个六元环 | |
| C. | 篮烷分子中存在3个五元环 | |
| D. | 篮烷的一氯代物共有4种同分异构体 |
| A. | 加催化剂 | B. | 降低温度 | C. | 减小压强 | D. | 加入O2 |
| A. | CO2、CH4、N2等均是造成温室效应的气体 | |
| B. | “地沟油”经过加工处理后,可以用来制造燃油 | |
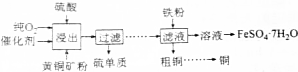
| C. | 铁粉、生石灰、硅胶是食品包装中常用的干燥剂 | |
| D. | 目前加碘食盐主要添加的是KI |
 已知A、B、C、D、E、F、G为前四周期中常见元素,且原子序数依次增大.A的原子半径最小,B的基态原子L层电子数是K层电子数的2倍,D的基态原子最外层电子排布式为nsnnpn+2,E为周期表中电负性最大的元素,F元素有多种化合价,它的一种氢氧化物在空气中易被氧化且最终变为红褐色,G与F同族且原子序数比F大2.回答下列问题:
已知A、B、C、D、E、F、G为前四周期中常见元素,且原子序数依次增大.A的原子半径最小,B的基态原子L层电子数是K层电子数的2倍,D的基态原子最外层电子排布式为nsnnpn+2,E为周期表中电负性最大的元素,F元素有多种化合价,它的一种氢氧化物在空气中易被氧化且最终变为红褐色,G与F同族且原子序数比F大2.回答下列问题: