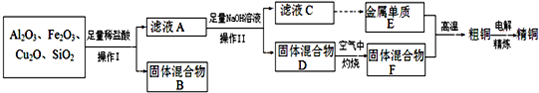
题目内容
 W、X、Y、Z四种短周期元素在元素周期表中的相对位置如图所示,W的气态氢化物可与其最高价含氧酸反应生成离子化合物,由此可知( )
W、X、Y、Z四种短周期元素在元素周期表中的相对位置如图所示,W的气态氢化物可与其最高价含氧酸反应生成离子化合物,由此可知( )| A、X、Y、Z中最简单氢化物稳定性最弱的是X |
| B、氧化物对应水化物的酸性Z一定强于Y |
| C、形成的单核阴离子还原性Y强于X |
| D、Z元素单质在化学反应中只表现氧化性,它在水溶液中有漂白性 |
考点:原子结构与元素的性质
专题:
分析:由W、X、Y、Z四种短周期元素在元素周期表中的相对位置,可知W、X处于第二周期,Y、Z处于第三周期,W的气态氢化物可与其最高价含氧酸反应生成离子化合物,则W为N元素,可推知X为O元素,Y为S元素,Z为Cl,结合元素周期律与元素化合物性质解答.
解答:
解:由W、X、Y、Z四种短周期元素在元素周期表中的相对位置,可知W、X处于第二周期,Y、Z处于第三周期,W的气态氢化物可与其最高价含氧酸反应生成离子化合物,则W为N元素,可推知X为O元素,Y为S元素,Z为Cl,
A.非金属性X>Y,Z>Y,非金属性越强,氢化物越稳定,故Y的氢化物稳定性最弱,故A错误;
B.非金属性Cl>S,应描述为最高价氧化物对应水化物的酸性Z一定强于Y,不是最高价氧化物,则不一定,如硫酸为强酸,而次氯酸为弱酸,故B错误;
C.非金属性O>S,故离子还原性O2-<S2-,故C正确;
D.氯气在反应中可以表现氧化性、还原性,如氯气与水的反应,氯水中次氯酸具有漂白性,氯气没有漂白性,故D错误,
故选C.
A.非金属性X>Y,Z>Y,非金属性越强,氢化物越稳定,故Y的氢化物稳定性最弱,故A错误;
B.非金属性Cl>S,应描述为最高价氧化物对应水化物的酸性Z一定强于Y,不是最高价氧化物,则不一定,如硫酸为强酸,而次氯酸为弱酸,故B错误;
C.非金属性O>S,故离子还原性O2-<S2-,故C正确;
D.氯气在反应中可以表现氧化性、还原性,如氯气与水的反应,氯水中次氯酸具有漂白性,氯气没有漂白性,故D错误,
故选C.
点评:本题考查结构性质位置关系应用,难度中等,推断元素是解题关键,注意对元素周期律的理解掌握.

练习册系列答案
相关题目
将某些化学知识用图象表示,可以收到直观、简明的效果.下列图象所表示的化学知识中,不正确的是
( )
( )
A、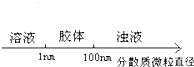 分散系的分类 |
B、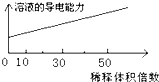 醋酸稀释 |
C、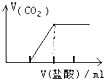 向Na2CO3溶液中逐滴滴入盐酸 |
D、 向AlCl3溶液中滴加过量的NaOH溶液 |
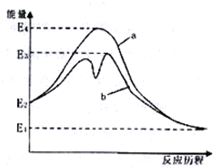 如图表示催化剂对某反应活化能的影响.几种酸的电离常数如下:HClO Kw=2.95×10-8,
如图表示催化剂对某反应活化能的影响.几种酸的电离常数如下:HClO Kw=2.95×10-8,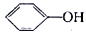 Kw=1.02×10-10H2CO3 Ka1=4.30×10-7 Ka2=5.61×10-11根据图象和数据判断,下列说法错误的是( )
Kw=1.02×10-10H2CO3 Ka1=4.30×10-7 Ka2=5.61×10-11根据图象和数据判断,下列说法错误的是( )| A、图说明了催化剂参与化学反应,并降低了活化能 |
| B、图中该反应没有催化剂参与时活化能为E2-E1 |
| C、将少量CO2通入NaClO溶液中,发生如下反应NaClO+CO2+H2O═HClO+NaHCO 3 |
D、相同浓度的NaClO溶液和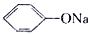 溶液,前者pH小 溶液,前者pH小 |
下列反应既属于氧化还原反应,又是吸热反应的是( )
| A、铝片与稀盐酸的反应 |
| B、Ba(OH)2.8H2O与NH4Cl的反应 |
| C、灼热的炭与CO2的反应 |
| D、甲烷在氧气中的燃烧反应 |
已知氯化钴和盐酸的混合溶液呈紫色,存在如下平衡:Co(H2O)62+(粉红色)+4Cl-?CoCl42-(蓝色)+6H2O△H>0,若使溶液呈粉红色,下列措施可行的是( )
| A、升温 | B、加压 |
| C、加水稀释 | D、滴加浓盐酸 |
一定量的CuS和 Cu2S的混合物投入足量的硝酸中,收集到气体VL(标准状况),向反应后的溶液中(存在Cu2+和SO42-)加入足量的NaOH溶液,产生蓝色沉淀,过滤,洗涤,灼烧,得到24.0gCuO.若上述气体为NO和NO2的混合物,且体积比为1:1,则V可能为( )
| A、18.0L |
| B、27.0L |
| C、31.4L |
| D、33.6L |
对于反应MnO2+4HCl(浓)
MnCl2+2H2O+Cl2↑,下列说法错误的是( )
| ||
| A、该反应是氧化还原反应 |
| B、MnO2发生还原反应 |
| C、HCl是还原剂 |
| D、若生成7.1 g Cl2,则转移0.1 mol电子 |