题目内容
一定量的CuS和 Cu2S的混合物投入足量的硝酸中,收集到气体VL(标准状况),向反应后的溶液中(存在Cu2+和SO42-)加入足量的NaOH溶液,产生蓝色沉淀,过滤,洗涤,灼烧,得到24.0gCuO.若上述气体为NO和NO2的混合物,且体积比为1:1,则V可能为( )
| A、18.0L |
| B、27.0L |
| C、31.4L |
| D、33.6L |
考点:化学方程式的有关计算
专题:计算题
分析:利用极限法解答,假设混合物全是CuS,或混合物全是Cu2S,根据n=
计算n(CuO),根据电子转移守恒计算n(CuS)、n(Cu2S),再根据电子转移数目守恒,计算n(NO)、n(NO2),根据V=nVm计算气体体积,实际气体介于二者之间.
| m |
| M |
解答:
解:若混合物全是CuS,其物质的量n(CuS)=n(CuO)=
=0.3mol,转移电子物质的量=0.3×(6+2)=2.4mol.NO和NO2的体积相等,设NO的物质的量为x、NO2的物质的量为x,则3x+x=2.4,解得x=0.6,故气体体积V=0.6mol×2×22.4L/mol=26.88L;
若混合物全是Cu2S,其物质的量n(Cu2S)=
n(CuO)=
×0.3mol=0.15mol,转移电子物质的量0.15×10=1.5mol,设NO为xmol、NO2为xmol,3x+x=1.5,计算得x=0.375,气体体积0.375mol×2×22.4L/mol=16.8L,
实际气体介于二者之间,即16.8<V<26.88,
故选A.
| 24g |
| 80g/mol |
若混合物全是Cu2S,其物质的量n(Cu2S)=
| 1 |
| 2 |
| 1 |
| 2 |
实际气体介于二者之间,即16.8<V<26.88,
故选A.
点评:本题考查氧化还原反应计算,难度中等,注意守恒思想与极限法的利用,是对学生综合能力的考查.

练习册系列答案
相关题目
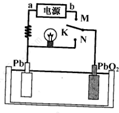 如图是铅蓄电池充、放电时的工作示意图,已知放电时电池反应为( )
如图是铅蓄电池充、放电时的工作示意图,已知放电时电池反应为( )2PbSO4+2H2O
| 充电 |
| 放电 |
2- 4 |
| A、K与N相接时,能量由电能转化为化学能 |
| B、K与N相接时,H+向负极区迁移 |
| C、K与M连接时,所用电源的a极为负极 |
| D、K与M相接时,阳极附近的pH逐渐增大 |
 W、X、Y、Z四种短周期元素在元素周期表中的相对位置如图所示,W的气态氢化物可与其最高价含氧酸反应生成离子化合物,由此可知( )
W、X、Y、Z四种短周期元素在元素周期表中的相对位置如图所示,W的气态氢化物可与其最高价含氧酸反应生成离子化合物,由此可知( )| A、X、Y、Z中最简单氢化物稳定性最弱的是X |
| B、氧化物对应水化物的酸性Z一定强于Y |
| C、形成的单核阴离子还原性Y强于X |
| D、Z元素单质在化学反应中只表现氧化性,它在水溶液中有漂白性 |
某可逆反应过程的能量变化如图所示,下列说法正确的是( )


| A、该反应能量变化类型与CaCO3分解反应相同 |
| B、加催化剂后,正反应速率加快,逆反应速率减少 |
| C、反应热△H=E2-E1 |
| D、若该反应为氧化还原反应,则可以将其设计成原电池 |
设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A、12g石墨烯(单层石墨)中含有六元环的个数为0.5NA |
| B、常温常压下,14g由N2与CO组成的混合气体含有的原子数目为2NA |
| C、已知某种元素的一种原子的质量为 a g,则该元素的相对原子质量近似为a NA |
| D、78 g苯中含有C═C双键的数目为3NA |
已知反应:
①2K2CrO4+H2SO4═K2Cr2O3+K2SO4+H2O,
②Fe2(SO4)3+2HI═2FeSO4+I2+H2SO4,
③K2Cr2O7+6FeSO4+7H2SO4═3Fe2(SO4)3+Cr2(SO4)3+K2SO4+7H2O.
下列结论不正确的是( )
①2K2CrO4+H2SO4═K2Cr2O3+K2SO4+H2O,
②Fe2(SO4)3+2HI═2FeSO4+I2+H2SO4,
③K2Cr2O7+6FeSO4+7H2SO4═3Fe2(SO4)3+Cr2(SO4)3+K2SO4+7H2O.
下列结论不正确的是( )
| A、①②③均是氧化还原反应 |
| B、氧化性强弱顺序:K2Cr2O7>Fe2(SO4)3>I2 |
| C、反应②中1mol还原剂失去电子数为6.02×1023 |
| D、反应③中氧化剂与还原剂的物质的量之比为1:6 |
下列离子检验的方法正确的是( )
| A、某溶液+AgNO3溶液→生成白色沉淀,说明原溶液中有Cl- |
| B、某溶液+BaCl2溶液→生成白色沉淀,说明原溶液中有SO42- |
| C、某溶液+NaOH溶液→生成蓝色沉淀,说明原溶液中有Cu2+ |
| D、某溶液+稀硫酸→产生无色气体,该气体能使澄清石灰水变浑浊,则原溶液中有CO32- |