题目内容
将某些化学知识用图象表示,可以收到直观、简明的效果.下列图象所表示的化学知识中,不正确的是
( )
( )
A、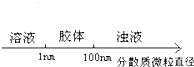 分散系的分类 |
B、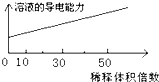 醋酸稀释 |
C、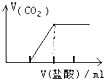 向Na2CO3溶液中逐滴滴入盐酸 |
D、 向AlCl3溶液中滴加过量的NaOH溶液 |
考点:弱电解质在水溶液中的电离平衡,分散系、胶体与溶液的概念及关系,钠的重要化合物,铝的化学性质
专题:
分析:A.依据分散系的本质区别是分散质微粒直径的大小判断;
B.溶液的导电性与溶液中离子浓度有关;
C.根据盐酸与碳酸钠的反应分析;
D.根据可能发生的反应Al3++3OH-=Al(OH)3↓,Al3++4OH-=AlO2-+2H2O分析.
B.溶液的导电性与溶液中离子浓度有关;
C.根据盐酸与碳酸钠的反应分析;
D.根据可能发生的反应Al3++3OH-=Al(OH)3↓,Al3++4OH-=AlO2-+2H2O分析.
解答:
解:A.胶体分散质粒子直径在1到100纳米之间,溶液分散质粒子直径小于1纳米,浊液分散质粒子直径大于100纳米,故A正确;
B.醋酸溶液加水稀释溶液中离子浓度减小,溶液的导电能力逐渐减弱,故B错误;
C.向Na2CO3溶液中逐滴滴加盐酸先后发生Na2CO3+HCl=NaHCO3+NaCl,NaHCO3+HCl=NaCl+H2O+CO2↑,开始无气体,后来才产生气体,且前后所加盐酸的体积比为1:1,故C正确;
D.先后发生的反应为:AlCl3+3NaOH=Al(OH)3↓+3NaCl,Al(OH)3+NaOH=NaAlO2+2H2O,生成沉淀过程消耗的NaOH与沉淀溶解消耗的NaOH体积比是3:1故D正确.
故选B.
B.醋酸溶液加水稀释溶液中离子浓度减小,溶液的导电能力逐渐减弱,故B错误;
C.向Na2CO3溶液中逐滴滴加盐酸先后发生Na2CO3+HCl=NaHCO3+NaCl,NaHCO3+HCl=NaCl+H2O+CO2↑,开始无气体,后来才产生气体,且前后所加盐酸的体积比为1:1,故C正确;
D.先后发生的反应为:AlCl3+3NaOH=Al(OH)3↓+3NaCl,Al(OH)3+NaOH=NaAlO2+2H2O,生成沉淀过程消耗的NaOH与沉淀溶解消耗的NaOH体积比是3:1故D正确.
故选B.
点评:本题考查了常见分散系的特征、物质反应的反应先后顺序、溶液的导电性等,注意把握弱电解质的电离平衡、铝的化合物的性质等,题目难度不大.

练习册系列答案
相关题目
有两种金属的合金13g,与足量稀硫酸反应后,在标准状况下产生气体11.2L,则组成该合金的金属可能是( )
| A、Mg和Al |
| B、Mg和Zn |
| C、Fe和Zn |
| D、Cu和Fe |
下列关于溶液中离子浓度的说法正确的是( )
| A、0.1mol.L-1的NaHCO3溶液中离子浓度关系:c(Na+)=2c(CO32-)+2c(HCO3-)+2c(H2CO3) | ||||
B、室温下,将物质的量浓度相等的一元酸HA和KOH等体积混合,溶液的pH=9,则:c(OH-)=c(K+)-c(A-)=
| ||||
C、将HCN和HF溶液混合,达平衡时:c(H+)=
| ||||
| D、等物质的量的CH3COOH和CH3COONa配置成混合溶液,已知其中c(CH3COO-)>c(Na+),则c(CH3COOH)<c(CH3COO-) |
下列离子方程式正确的是( )
| A、铜氨溶液的制备:Cu2-+2NH3.H2O=Cu(NH3)22++2H2O |
| B、氢氧化钡溶液中滴加明矾溶液至Ba2+恰好完全沉淀:Ba2++30H-+SO42-+Al3+=BaSO4↓+Al(OH)3↓ |
C、水杨酸钠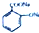 通入过量的CO2; 通入过量的CO2; 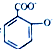 +CO2+H2O→ +CO2+H2O→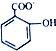 +HCO3- +HCO3- |
| D、在氯化亚铁溶液中加入足量酸性高锰酸钾溶液:5Fe2++8H++Mn04-=5Fe3++Mn2++4H2O |
某兴趣小组的同学,在配制100ml0.5mol?L-1的Na2CO3溶液时有以下实验操作,其中会导致所配制的溶液浓度偏高的是( )
| A、天平左盘放砝码,右盘放固体 |
| B、容量瓶使用时含有少量的蒸馏水 |
| C、定容时水加多了 |
| D、定容时俯视刻度线 |
2013年12月初我国大部分地区被雾霜笼罩,嘉兴等地PM2.5指数频率“爆表”.PM2.5是指大气中直径小于或等于2.5微米(2.5×10-6m)的细小颗粒物,也称为可入肺颗粒物,下列说法中错误的是( )
| A、雾霜空气属于混合物 |
| B、微粒直径为2.5微米的细小颗粒物形成的分散系统能产生丁达尔效应 |
| C、实施绿化工程,实行汽车限行和使用清洁能源可以有效地防治PM2.5污染 |
| D、PM2.5表面积较大,能大量吸附空气中的有毒、有害物质进入人体造成伤害 |
对于反应4Fe(OH)2(s)+2H2O(l)+O2(g)═4Fe(OH)3(s)△H=-444.3kJ/mol,且熵减小,在常温常压下该反应能自发进行,对反应的方向起决定作用的是( )
| A、焓变 | B、温度 | C、压强 | D、熵变 |
 W、X、Y、Z四种短周期元素在元素周期表中的相对位置如图所示,W的气态氢化物可与其最高价含氧酸反应生成离子化合物,由此可知( )
W、X、Y、Z四种短周期元素在元素周期表中的相对位置如图所示,W的气态氢化物可与其最高价含氧酸反应生成离子化合物,由此可知( )| A、X、Y、Z中最简单氢化物稳定性最弱的是X |
| B、氧化物对应水化物的酸性Z一定强于Y |
| C、形成的单核阴离子还原性Y强于X |
| D、Z元素单质在化学反应中只表现氧化性,它在水溶液中有漂白性 |