��Ŀ����
3���������Ƽ���ֳ������Ƽ������Ҫ�������ӷ�Ӧ��ԭ����̼�����Ƶ��ܽ��ԡ����ȶ��Եȣ���������Ʒ�������Ʒ�Ȼ�泥���������ʾ����ͼ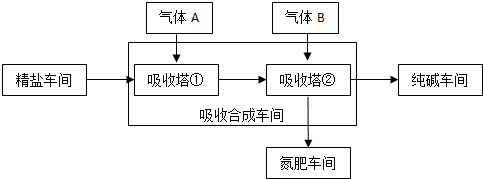
����ʹ�õ����ܽ����Ϣ��ͼ��
�ش��������⣺
��1������A��NH3����ѧʽ���������պϳɳ��䡱��Ҫ�ϳ�̼�����ƹ��壬�����������з�����Ӧ�Ļ�ѧ����ʽΪNaCl+CO2+H2O+NH3�TNaHCO3��+NH4Cl��
��2������Bͨ����ѹ��ѹ���������ڵ���ҪĿ����ͨ����ѹ�����CO2�����������е��ܽ������Ӷ����HCO3-��Ũ�ȣ��������γ�NaHCO3������
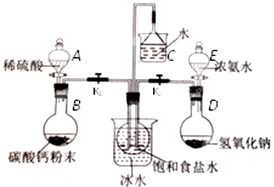
��3����������һ�����սС��������������¶�Լ5�����ң�����������Ӧ�÷�����D��
A�����γ��� B�����պϳɳ��� C������� D�����ʳ���
��4�����ʳ��������Ȼ��֮���ĸҺ������ѭ�������������м���ʹ�ã�����������ҪĿ�������NaCl�������ʣ�����֮�⣬������ѭ�����õ���CO2����ѧʽ����
��5�������ղ�200�ִ����������ҵ��˵�����NaCl��������Ϊ96%�����γ���Ҫ�չ�����230�֣�
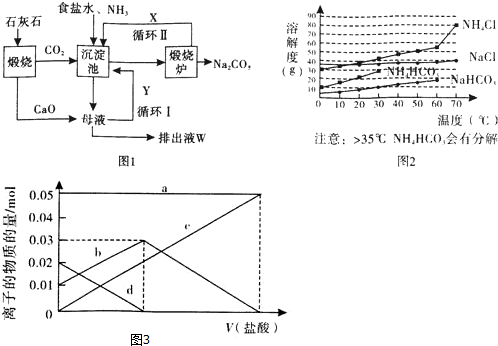
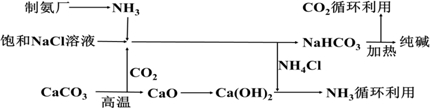
���� ���γ����Ʊ������Ȼ�����Һ��������������ͨ������AΪ����������������������ͨ�������̼�������պϳɳ��䡱��Ҫ�ϳ�̼�����ƹ��壬��Ӧ��õ�̼�����ƾ��塢�Ȼ�泥������Ȼ��Ϊ���ʣ�̼���������ȷֽ����ɴ��������̼��ˮ��������̼ѭ��ʹ�ã�
��1��������֪����AΪ����������BΪ������̼���백���ı����Ȼ�����Һ��ͨ�������̼������Ӧ����̼�����ƾ�����Ȼ�泥�
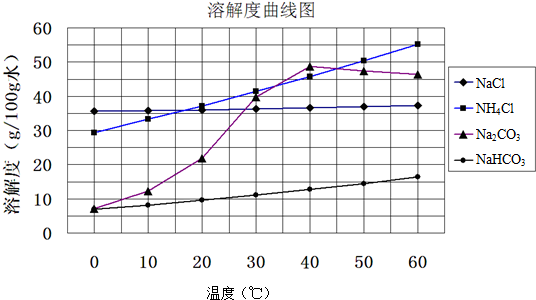
��2��������̼�ܽ��Խ�С������ѹǿ��߶�����̼�ܽ�����
��3����������һ�����սС�������������̼�����ƾ�����˵õ���ҺΪ�Ȼ����Һ��
��4��������Ȼ�狀��ĸҺ����Ҫ���Ȼ��ƣ�����ѭ�������������м���ʹ�ã�����������ҪĿ�������NaCl�������ʣ�̼�����Ʒֽ����ɵĶ�����̼Ҳ����ѭ��ʹ�ã�
��5�����ݷ�Ӧ����ʽ����Ԫ���غ����õ���
��� �⣺���γ����Ʊ������Ȼ�����Һ��������������ͨ������AΪ����������������������ͨ�������̼�������պϳɳ��䡱��Ҫ�ϳ�̼�����ƹ��壬��Ӧ��õ�̼�����ƾ��塢�Ȼ�泥������Ȼ��Ϊ���ʣ�̼���������ȷֽ����ɴ��������̼��ˮ��������̼ѭ��ʹ�ã�
��1��������֪����AΪNH3�������պϳɳ��䡱��Ҫ�ϳ�̼�����ƹ��壬�����������з�����Ӧ�Ļ�ѧ����ʽΪ��NaCl+CO2+H2O+NH3�TNaHCO3��+NH4Cl��
�ʴ�Ϊ��NH3�� NaCl+CO2+H2O+NH3�TNaHCO3��+NH4Cl��
��2������BΪ������̼���ܽ��Խ�С��ͨ����ѹ��ѹ���������ڵ���ҪĿ���ǣ�ͨ����ѹ�����CO2�����������е��ܽ������Ӷ����HCO3-��Ũ�ȣ��������γ�NaHCO3������
�ʴ�Ϊ��ͨ����ѹ�����CO2�����������е��ܽ������Ӷ����HCO3-��Ũ�ȣ��������γ�NaHCO3������
��3����������һ�����սС��������������¶�Լ5�����ң�����������Ӧ�÷����ڵ��ʳ��䣬��������̼�����ƹ��˵õ���Һ�Ȼ�狀;���̼�����ƣ���ѡD��
�ʴ�Ϊ��D��
��4�����ʳ��������Ȼ��֮���ĸҺ������ѭ�������������м���ʹ�ã�����������ҪĿ�������NaCl�������ʣ�����֮�⣬������ѭ�����õ���̼�����Ʒֽ����ɵĶ�����̼��
�ʴ�Ϊ��CO2 ��
��5�������ղ�200�ִ����������ҵ��˵�����NaCl��������Ϊ96%���辫�γ���Ҫ�չ�����Ϊxt�������Ԫ���غ�l��ʽ����õ���
$\frac{200}{106}$��2=$\frac{x��96%}{58.5}$
x=230t
�ʴ�Ϊ��230��
���� ���⿼���˺����Ƽ��ԭ�������̷�������Ҫ������ͨ���˳�����ɲ�����жϣ����ջ����ǽ���ؼ�����Ŀ�Ѷ��еȣ�

| A�� | 1��3 | B�� | 1��5 | C�� | 5��1 | D�� | 3��1 |

| A�� | M�дﵽƽ�����ͨ��һ�����ĺ�����ƽ�ⲻ�ƶ���������������ܶȲ��� | |
| B�� | ��x��y=1��2����ƽ��ʱ��M�е�ת���ʣ�A��B | |
| C�� | ��x��y=1��3����M�зų�����172.8 kJʱ��A��ת����Ϊ90% | |
| D�� | N�дﵽƽ�����ͨ��һ�����ĺ���ʱ��v��������v���棩 |