题目内容
5.元素X、Y、Z、M、N均为短周期主族元素,且原子序数依次增大.已知Y原子最外层电子数与核外电子总数之比为3:4;M元素原子的最外层电子数与电子层数之比为4:3;N-、Z+、X+的半径逐渐减小;化合物XN常温下为气体.据此回答:①X为氢(名称),Y为O(元素符号),Z原子结构示意图为
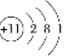 .
.②N的最高价氧化物的水化物的化学式为HClO4.
③工业上制取单质M的化学方程式为SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑.
分析 元素X、Y、Z、M、N均为短周期主族元素,且原子序数依次增大.已知Y原子最外层电子数与核外电子总数之比为3:4,则Y的最外层电子数为6,核外电子数为8符合,即Y为O元素;M元素原子的最外层电子数与电子层数之比为4:3,M为第三周期的Si元素;N-、Z+、X+的半径逐渐减小,可知N为Cl、Z为Na、X为H;化合物HCl常温下为气体,以此来解答.
解答 解:元素X、Y、Z、M、N均为短周期主族元素,且原子序数依次增大.已知Y原子最外层电子数与核外电子总数之比为3:4,则Y的最外层电子数为6,核外电子数为8符合,即Y为O元素;M元素原子的最外层电子数与电子层数之比为4:3,M为第三周期的Si元素;N-、Z+、X+的半径逐渐减小,可知N为Cl、Z为Na、X为H;化合物HCl常温下为气体,
①由上述分析可知,X为氢,Y为O,Z的原子结构示意图为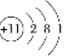 ,故答案为:氢;O;
,故答案为:氢;O;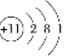 ;
;
②N的最高价氧化物的水化物的化学式为HClO4,故答案为:HClO4;
③工业上制取单质M的化学方程式为SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑,故答案为:SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑.
点评 本题考查原子结构与元素周期律,为高频考点,把握Y原子最外层电子数与核外电子总数之比为3:4推断Y为O元素为解答的关键,侧重分析与推断能力的考查,注意周期律及元素化合物知识的应用,题目难度不大.

练习册系列答案
相关题目
15.用核磁共振仪对分子式为C3H8O的有机物进行分析,核磁共振氢谱有四个峰,峰面积之比是1:1:2:6,则该化合物的结构简式为( )
| A. | CH3OCH2CH2CH3 | B. | CH3CH(OH)CH2CH3 | C. | (CH3)2CHCH2OH | D. | CH3CH2CH2CH2OH |
16.W、X、Y、Z均为短周期主族元素,原子序数依次增加,X与Y形成的化合物能与水反应生成酸且X、Y同主族,两元素核电荷数之和与W、Z的原子序数之和相等,则下列说法正确的是( )
| A. | Z元素的含氧酸一定是强酸 | |
| B. | 原子半径:X>Z | |
| C. | 气态氢化物热稳定性:W>X | |
| D. | W、X与H形成化合物的水溶液可能呈碱性 |
20.下表是元素周期表的一部分,针对表中的①~⑩中元素,用元素符号或化学式填空回答以下问题:
(1)在这些元素中最活泼的非金属元素是F
(2)元素的最高价氧化物对应的水化物中酸性最强的是HClO4,碱性最强的是KOH
(3)呈两性的氢氧化物是Al(OH)3,其与③的最高价氧化物水化物反应的离子方程式为Al(OH)3+OH-=AlO2-+2H2O
(4)在③~⑦元素中,原子半径最大的是Na
(5)在⑦与⑩的单质中,化学性质较活泼的是Cl2,可用什么化学反应说明该事实(写出反应的化学方程式):2NaBr+Cl2=2NaCl+Br2.
| 主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 二 | ① | ② | ||||||
| 三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 四 | ⑨ | ⑩ |
(2)元素的最高价氧化物对应的水化物中酸性最强的是HClO4,碱性最强的是KOH
(3)呈两性的氢氧化物是Al(OH)3,其与③的最高价氧化物水化物反应的离子方程式为Al(OH)3+OH-=AlO2-+2H2O
(4)在③~⑦元素中,原子半径最大的是Na
(5)在⑦与⑩的单质中,化学性质较活泼的是Cl2,可用什么化学反应说明该事实(写出反应的化学方程式):2NaBr+Cl2=2NaCl+Br2.
10.下列实验或操作方法正确的是( )
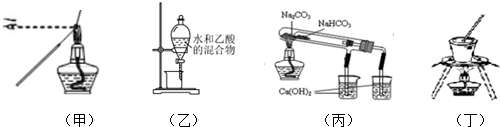

| A. | 甲图装置:用蘸有待测液的铁丝,检验K+ | |
| B. | 乙图装置:分离水和乙酸 | |
| C. | 丙图装置:验证NaHCO3和Na2CO3的热稳定性 | |
| D. | 丁图装置:从食盐水中提取食盐 |
14.下列是卤素单质(F2、Cl2、Br2、I2)的沸点与相对分子质量的关系图,下列说法错误的是( )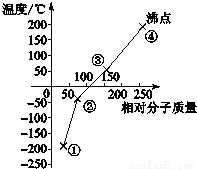

| A. | 单质①是最活泼的非金属单质 | |
| B. | 单质②能使品红溶液褪色 | |
| C. | 保存少量的单质③时加少量水进行水封 | |
| D. | 单质④的氢化物在卤素氢化物中沸点最高 |
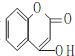 )的路线如下图所示:
)的路线如下图所示: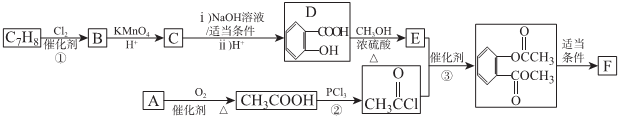
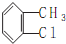 .
.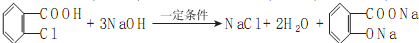 .
.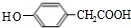 .
.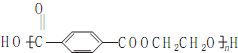 ),参照A→乙酸的表示方法,写出相应的合成路线图
),参照A→乙酸的表示方法,写出相应的合成路线图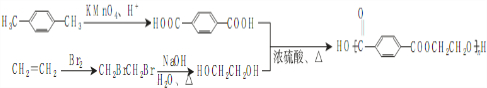 .
.