题目内容
20.在NaCl溶液中含有少量的Na2S,欲将S2-除去,可加入( )| A. | 稀硫酸 | B. | AgCl | C. | NaOH | D. | Ag2S |
分析 沉淀向溶解度小的方向转化,据此解题.
解答 解:因为氯化银的溶解度小于Ag2S,因而加入AgCl生成更难溶的Ag2S.
故选B.
点评 本题考查物质的分离、提纯和除杂等问题,题目难度不大,根据除杂是不能引入新的杂质、不能影响被提纯的物质的性质和量,并且操作简单可行,除杂时要结合物质的物理性质和化学性质进行分离.

练习册系列答案
相关题目
7.用NA表示阿伏加德罗常数的数值,下列说法中不正确的是( )
| A. | 常温下,1L pH=3的硫酸溶液中,SO42-离子的数目约为5×10-4NA | |
| B. | 1mol氨基(NH2)中含有电子的数目为10NA | |
| C. | 一定条件下,1molN2与3molH2充分反应,转移电子的数目可能为2NA | |
| D. | 3molNO2和H2O完全反应,被还原的NO2分子数目为1NA |
8.下列说法正确的是( )
| A. | 蔗糖、淀粉、油脂及其水解产物均为非电解质 | |
| B. | 煤油可由石油分馏获得,可用作燃料和保存少量金属钠 | |
| C. | 乙醇、乙酸、乙酸乙酯都能发生取代反应,乙酸乙酯中的少量乙酸可用NaOH溶液除去 | |
| D. | 苯、油脂均不能使酸性KMnO4溶液褪色 |
8.NA表示阿伏加德罗常数,下列叙述正确的是( )
| A. | 电解精炼铜的过程中,每转移NA个电子时,阳极溶解铜的质量为32g | |
| B. | 1 molNa2O2固体中含离子总数为4NA | |
| C. | 1mol羟基与17gNH3所含电子数之比为9:10 | |
| D. | 1molNa2CO3晶体中含CO32-离子数小于NA |
12.NA代表阿伏加德罗常数的值,下列说法正确的是( )
| A. | 2.3g钠由原子变成离子时,失去的电子数目为0.2NA | |
| B. | 0.2NA个硫酸分子与19.6g磷酸分子含有相同的氧原子数 | |
| C. | 28g氮气所含原子数为NA | |
| D. | NA个氧分子与NA个氢分子的质量比为2:1 |
9.某同学测得物质的量浓度均为0.01mol/L CH3COOH和CH3COONa混合溶液呈酸性后,得出了关系式,你认为其中不正确的是( )
| A. | c(CH3COOH)<c(Na+) | B. | c(CH3COO-)>c(Na+)>c(H+)>c(OH-) | ||
| C. | c(CH3COOH)+c(H+)═c(CH3COO-)+c(OH-) | D. | c(CH3COOH)+c(CH3COO-)═0.02 mol/L |
10.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 盐酸中:K+、Mg2+、Fe2+、MnO4- | |
| B. | NaOH溶液中:Cu2+、NH4+、SO42-、CO32- | |
| C. | FeCl3溶液中:Al3+、Na+、I-、SO42- | |
| D. | NaClO溶液中:K+、SO42-、OH-、NO3- |
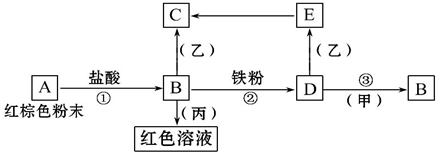 下列物质之间有如下反应关系,已知由E转化成C的现象是:灰白色沉淀迅速变为灰绿色,最后变为红褐色.
下列物质之间有如下反应关系,已知由E转化成C的现象是:灰白色沉淀迅速变为灰绿色,最后变为红褐色.