题目内容
12.NA代表阿伏加德罗常数的值,下列说法正确的是( )| A. | 2.3g钠由原子变成离子时,失去的电子数目为0.2NA | |
| B. | 0.2NA个硫酸分子与19.6g磷酸分子含有相同的氧原子数 | |
| C. | 28g氮气所含原子数为NA | |
| D. | NA个氧分子与NA个氢分子的质量比为2:1 |
分析 A.根据钠的质量计算出钠的物质的量,再根据电子守恒判断钠失去电子的物质的量及数目;
B.硫酸和磷酸摩尔质量相等,而每分子中含有氧原子数相同;
C.氮气是双原子分子;
D.NA个氧分子与NA个氢分子的质量等于摩尔质量之比.
解答 解:A.2.3g钠的物质的量为0.1mol,变成钠离子失去0.1mol电子,失去的电子数目为0.1NA,故A错误;
B.硫酸和磷酸摩尔质量相等,而每分子中含有氧原子数相同,19.6g磷酸分子数也为0.2NA,故B正确;
C.28g氮气是1mol,含有的原子数为2NA,故C错误;
D.NA个氧分子与NA个氢分子的质量等于摩尔质量之比,即32:2=16:1,故D错误;
故选.
点评 本题考查了阿伏伽德罗常数,完成本题需要熟练掌握有关物质的量与摩尔质量、气体摩尔体积、阿伏伽德罗常数等之间的转化关系,题目难度不大.

练习册系列答案
 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案
相关题目
19.2015年7月31日,中国获得2022年冬奥会主办权,这将促进中国冰雪运动的发展.以下关于冰的说法正确的是( )
| A. | 等质量的0℃冰与0℃的水内能相同 | B. | 冰和可燃冰都是结晶水合物 | ||
| C. | 冰和干冰、水晶的空间结构相似 | D. | 氢键影响冰晶体的体积大小 |
20.在NaCl溶液中含有少量的Na2S,欲将S2-除去,可加入( )
| A. | 稀硫酸 | B. | AgCl | C. | NaOH | D. | Ag2S |
17.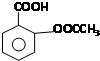 阿司匹林(Aspirin)也叫乙酰水杨酸(结构如图所示)是一种历史悠久的解热镇痛药.下列有关说法正确的是( )
阿司匹林(Aspirin)也叫乙酰水杨酸(结构如图所示)是一种历史悠久的解热镇痛药.下列有关说法正确的是( )
 阿司匹林(Aspirin)也叫乙酰水杨酸(结构如图所示)是一种历史悠久的解热镇痛药.下列有关说法正确的是( )
阿司匹林(Aspirin)也叫乙酰水杨酸(结构如图所示)是一种历史悠久的解热镇痛药.下列有关说法正确的是( )| A. | 与乙酰水杨酸具有相同官能团的芳香族同分异构体共有8种(不考虑立体异构) | |
| B. | 乙酰水杨酸的所有原子均在同一平面上 | |
| C. | 乙酰水杨酸能发生取代、加成、氧化、还原反应 | |
| D. | 乙酰水杨酸易溶于水、乙醇等溶剂 |
4.X、Y、Z、W是原子序数依次增大的四种短周期元素,甲、乙、丙、丁、戊是由其中的两种或三种元素组成的化合物,己是由Z 元素形成的单质.已知:甲+乙=丁+己,甲+丙=戊+己; 0.1mol•L-1丁溶液的pH为13(25℃).下列说法正确的是( )
| A. | 原子半径:W>Z>Y>X | |
| B. | Y元素在周期表中的位置为第三周期第ⅣA族 | |
| C. | X分别与Y、Z、W所形成的化合物均为共价化合物 | |
| D. | X与Y所形成的化合物的沸点可能高于X与Z所形成的化合物 |
1. 已知X、Y、Z、E、F五种常见物质含有同一元素M,在一定条件下它们有如图转化关系,Z是NO,下列推断不合理的是( )
已知X、Y、Z、E、F五种常见物质含有同一元素M,在一定条件下它们有如图转化关系,Z是NO,下列推断不合理的是( )
 已知X、Y、Z、E、F五种常见物质含有同一元素M,在一定条件下它们有如图转化关系,Z是NO,下列推断不合理的是( )
已知X、Y、Z、E、F五种常见物质含有同一元素M,在一定条件下它们有如图转化关系,Z是NO,下列推断不合理的是( )| A. | X可能是一种氢化物 | B. | X生成Z一定是化合反应 | ||
| C. | E可能是一种有色气体 | D. | F中M元素的化合价可能为+5 |
2.下列有关实验说法中不正确的是( )
| A. | 如果汽油、煤油等可燃物着火,应立即用水扑灭 | |
| B. | 在点燃易燃气体前,必须检验气体的纯度 | |
| C. | 为防止试管破裂,加热固体高锰酸钾制氧气时,试管口应略向下倾斜 | |
| D. | 萃取操作时,应选择可以和原溶剂不互溶的萃取剂 |
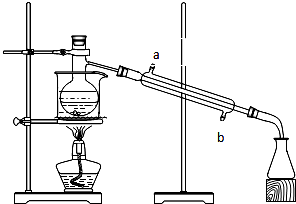 实验题:如图所示的仪器装置,在蒸馏烧瓶中装有冰醋酸、乙醇、浓硫酸和沸石,水浴加热,粗制乙酸乙酯.反应一段时间后,将粗产品倒入装有水的烧杯中,液体分为两层,现用两种方法检验
实验题:如图所示的仪器装置,在蒸馏烧瓶中装有冰醋酸、乙醇、浓硫酸和沸石,水浴加热,粗制乙酸乙酯.反应一段时间后,将粗产品倒入装有水的烧杯中,液体分为两层,现用两种方法检验