题目内容
12. 图中A~I是初中化学常见的物质,且分别是由H、C、O、Na、Al、S、Ca、Cu、Ag中的一种或几种元素组成的.
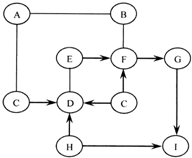
图中A~I是初中化学常见的物质,且分别是由H、C、O、Na、Al、S、Ca、Cu、Ag中的一种或几种元素组成的.在通常情况下,D与其他物质的状态不同;D、G、H、I均为单质,其中G为紫红色固体,H在空气中表面生成一层致密的氧化膜,具有很好的抗腐蚀性能:B可用来改良酸性土壤;A、F均为由三种元素组成的盐.图中“一”表示两端的物质问能发生化学反应;“→”表示物质间存在转化关系:部分反应物、生成物或反应条件已略去.
(l) 写出化学式:GCu.
(2 ) 写出A与C反应的化学方程式Na2CO3+H2SO4=Na2SO4+H2O+CO2↑.写出H→I反应的化学方程式Al+3AgNO3═Al(NO3)3+3Ag.
(3)D与E反应的基本类型置换反应.
分析 “H在空气中表面生成一层致密的氧化膜,具有很好的抗腐蚀性能”,则推测H为Al;“G为紫红色固体”,则推测G为Cu;“B可用来改良酸性土壤”,则推测B为Ca(OH)2;根据“A,F均为由三种元素组成的盐”,结合图框,则推测A,F分别为Na2CO3、CuSO4;“在通常情况下,D与其他物质的状态不同,D、G、H、I均为单质”、“图中A~I是初中化学常见的物质,且分别是由H、C、O、Na、Al、S、Ca、Cu、Ag中的一种或几种元素组成的”,则推测C可能为稀硫酸、D为H2、E为CuO、I为Ag,以此解答该题.
解答 解:(1)由以上分析可知G为Cu,故答案为:Cu;
(2)A与C反应,即碳酸钠和硫酸反应生成硫酸钠、水和二氧化碳,其化学方程式为:Na2CO3+H2SO4=Na2SO4+H2O+CO2↑;H→I反应,即铝与硝酸银溶液反应生成硝酸铝溶液和银,反应的化学方程式为:Al+3AgNO3═Al(NO3)3+3Ag,
故答案为:Na2CO3+H2SO4=Na2SO4+H2O+CO2↑;Al+3AgNO3═Al(NO3)3+3Ag;
(3)D与E反应,即氧化铜和氢气反应生成铜和水,为置换反应,故答案为:置换反应.
点评 本题考查无机物的推断,为高频考点,侧重考查学生的分析能力,注意把握常见物质的性质以及反应的现象,难度不大,要注意知识的积累及综合运用.

练习册系列答案
 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案
相关题目
7.下列除杂方式正确的是( )
| A. | CO2气体中含有的少量杂质SO2可通过饱和Na2CO3溶液除去 | |
| B. | NaOH溶液中含有少量的Ba(OH)2可加入适量的Na2SO4过滤除去 | |
| C. | K2CO3固体中含有少量的NaHCO3杂质可用加热的方式提纯 | |
| D. | Cu粉中含有的少量杂质Fe可加入FeCl3溶液除去 |
8.用NA表示阿伏伽德罗常数的值,下列叙述正确的是( )
| A. | 1mol Cu与足量稀硝酸反应产生NA个NO分子 | |
| B. | 含NA个Na+的Na2O溶解于1L水中,Na+的物质的量浓度为1mol•L-1 | |
| C. | 通常条件下,7.1g 37Cl2含中子数为4.0NA | |
| D. | 2.4g Mg在足量O2中燃烧,转移的电子数为0.2NA |
5.下列有关化学用语表示不正确的是( )
| A. | 甲基的结构式: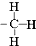 | B. | 硝基苯的结构简式: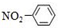 | ||
| C. | 氯乙烷的分子式:C2H5Cl | D. | 丙烷分子的球棍模型示意图: |
7.下列说法正确的是( )
| A. | 1 mol任何气体的摩尔体积都约是22.4 L | |
| B. | 标准状况时,体积均为22.4 L的O2与CO2含有相同的分子数 | |
| C. | 处于标准状况的两种气体,当体积均为22.4 L时的质量完全相同 | |
| D. | 标准状况时,2 mol任何物质的体积均约为44.8 L |
17.表是几种弱酸常温下的电离平衡常数:
(1)①CH3COOH、②H2CO3、③H2S、④H3PO4四种酸的酸性由强到弱的顺序为(填序号)④①②③.
(2)同浓度的①CH3COO-②HCO3-③CO32-④S2-结合H+的能力由强到弱的顺序为(填序号)④③②①.
| ①CH3COOH | ②H2CO3 | ③H2S | ④H3PO4 |
| K=1.8×10-5 | K1=4.3×10-7 K2=5.6×10-11 | K1=9.1×10-8 K2=1.1×10-12 | K1=7.5×10-3 K2=6.2×10-8 K3=2.2×10-13 |
(2)同浓度的①CH3COO-②HCO3-③CO32-④S2-结合H+的能力由强到弱的顺序为(填序号)④③②①.
4.下列说法中正确的是( )
| A. | 1 mol稀硫酸和1 mol稀Ba(OH)2溶液完全中和所放出的热量为中和热 | |
| B. | 中和反应都是放热反应,多数分解反应是吸热反应 | |
| C. | 在101 kPa时,1 mol碳燃烧所放出的热量一定是碳的燃烧热 | |
| D. | 碳与二氧化碳的反应既是放热反应,也是化合反应 |
1.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 常温常压下,0.1mol二氧化硅中所含硅氧键数目为0.2NA | |
| B. | 50mL12mol•L-1盐酸与足量MnO2共热,转移的电子数为0.3NA | |
| C. | 常温常压下,46gNO2含有原子数为3 NA(相对原子质量N:14 O:16) | |
| D. | 标准状况下,11.2LSO3含有分子数为0.5NA |
2.设NA为阿伏伽德罗常数的值,下列叙述正确的是( )
| A. | 标准状态下,22.4LSO3含有原子数为4NA | |
| B. | 4℃时,18gH2O含有2NA 个非极性键 | |
| C. | 1molNa2O和Na2O2混合物中含有的阴、阳离子总数是3NA | |
| D. | 将含1molFeCl3的饱和溶液滴入沸水形成的胶体粒子的数目为NA |