题目内容
16.室温下,下列溶液等体积混合后,所得溶液的pH一定大于7的是( )| A. | 0.1mol/L的盐酸和0.1mol/L的氨水溶液 | |
| B. | 0.1mol/L的盐酸和0.1mol/L的氢氧化钠溶液 | |
| C. | pH=4的醋酸溶液和pH=10的氢氧化钠溶液 | |
| D. | pH=4的盐酸和pH=l0的氨水 |
分析 A、0.1mol/L的盐酸和0.1mol/L的氨水溶液等体积混合后,能恰好完全反应;
B、0.1mol/L的盐酸和0.1mol/L的氢氧化钠溶液等体积混合后,恰好完全反应生成氯化钠;
C、醋酸是弱电解质,没有完全电离;
D、一水合氨为弱电解质,不能完全电离.
解答 解:A、0.1mol/L的盐酸和0.1mol/L的氨水溶液等体积混合后,能恰好完全反应生成氯化铵溶液,为强酸弱碱盐溶液,故水解显酸性,故A错误;
B、0.1mol/L的盐酸和0.1mol/L的氢氧化钠溶液等体积混合后,恰好完全反应生成氯化钠溶液,为强碱强酸盐,溶液显中性,故B错误;
C、pH=4的醋酸溶液中氢离子浓度为10-4mol/L,pH=10的氢氧化钠溶液中氢氧根浓度也为10-4mol/L,但醋酸是弱电解质,没有完全电离,故反应后醋酸过量,故溶液显酸性,故C错误;
D、pH=4的盐酸中氢离子浓度为10-4mol/L,pH=10的氨水溶液中氢氧根浓度也为10-4mol/L,但一水合氨为弱电解质,不能完全电离,故氨水过量,溶液显碱性,故D正确.
故选D.
点评 本题考查了酸碱混合后溶液酸碱性的判断,难度不大,应注意弱电解质不能完全电离,强电解质完全电离.

练习册系列答案
相关题目
7.下列分子中,属于非极性分子的是( )
| A. | SO2 | B. | BeCl2 | C. | NF3 | D. | COCl2 |
4.如表是A、B、C、D、E五种有机物的有关信息:
回答下列问题:
(1)A与溴的四氯化碳溶液反应的生成物的名称是1,2-二溴乙烷.
(2)A与氢气发生加成反应后生成物质F,与F在分子组成和结构上相似的有机物有一大类(俗称“同系物”),它们均符合通式CnH2n+2.当n=4时,这类有机物开始出现同分异构体.
(3)B具有的性质是②③(填序号).
①无色无味液体 ②有毒 ③不溶于水 ④密度比水大
⑤与酸性KMnO4溶液和溴水反应褪色 ⑥任何条件下不与氢气反应
写出在浓硫酸作用下,B与浓硝酸反应的化学方程式: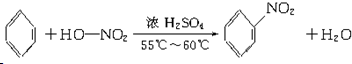 .
.
(4)C与E反应能生成相对分子质量为100的酯,该反应的反应类型为酯化反应;
(5)写出由C氧化生成D的化学方程式2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O.
| A | ①能使溴的四氯化碳溶液褪色;②比例模型为; ③能与水在一定条件下反应生成C ③能与水在一定条件下反应生成C |
| B | ①由C、H两种元素组成;②球棍模型为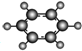 |
| C | ①由C、H、O三种元素组成;②能与Na反应,但不能与NaOH溶液反应;③能与E反应生成相对分子质量为100的酯 |
| D | ①相对分子质量比C少2;②能由C氧化而成 |
| E | ①由C、H、O三种元素组成;②球棍模型为 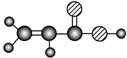 |
(1)A与溴的四氯化碳溶液反应的生成物的名称是1,2-二溴乙烷.
(2)A与氢气发生加成反应后生成物质F,与F在分子组成和结构上相似的有机物有一大类(俗称“同系物”),它们均符合通式CnH2n+2.当n=4时,这类有机物开始出现同分异构体.
(3)B具有的性质是②③(填序号).
①无色无味液体 ②有毒 ③不溶于水 ④密度比水大
⑤与酸性KMnO4溶液和溴水反应褪色 ⑥任何条件下不与氢气反应
写出在浓硫酸作用下,B与浓硝酸反应的化学方程式:
 .
.(4)C与E反应能生成相对分子质量为100的酯,该反应的反应类型为酯化反应;
(5)写出由C氧化生成D的化学方程式2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O.
1.下列叙述中不正确的是( )
| A. | 电镀时,电镀池里的阳极材料发生氧化作用 | |
| B. | 电解饱和食盐水制烧碱,用涂镍碳钢网作阴极 | |
| C. | 惰性电极电解氯化铜溶液,在阴极上和阳极上析出产物的物质的量之比为1:1 | |
| D. | 电解熔融的氧化铝制取金属铝,用铁作阳极 |
8.下列说法中正确的是( )
| A. | 钠的还原性很强,在空气中易变质,久置后变为过氧化钠 | |
| B. | 用湿润的蓝色石蕊试纸检验氨气 | |
| C. | 新制的氯水通常保存在棕色玻璃试剂瓶中,并现用现配 | |
| D. | 漂粉精的有效成分为氯化钙 |
19.自然界中存在一种尖晶石,化学式可表示为MgAl2O4.已知某尖晶石样品中混有Fe2O3,取5.4g该样品,恰好完全溶解于100g一定浓度的盐酸,则该盐酸的质量分数可能为( )
| A. | 6.5% | B. | 8.5% | C. | 11.5% | D. | 12.5% |