题目内容
12.某无色气体可能含有甲烷、一氧化碳、氢气中的一种或几种,依次进行下列实验(假设每步反应或吸收均完全):①无色气体在足量氧气中燃烧;
②燃烧生成的气体通过盛有浓硫酸的洗气瓶,装置增重3.6克;
③再将剩余气体通过盛有澄清石灰水溶液的洗气瓶,装置增重4.4克.下列推断正确的是( )
| A. | 该气体可能只含有一氧化碳、氢气 | B. | 该气体可能只含有甲烷、一氧化碳 | ||
| C. | 该气体一定只含有甲烷 | D. | 该气体一定只含有甲烷、氢气 |
分析 由题意可知,浓硫酸吸收燃烧生成的水,而氢氧化钙溶液用于吸收燃烧生成的二氧化碳,浓硫酸质量与氢氧化钙溶液的质量都增加,说明燃烧既生成了水又生成了二氧化碳,结合可燃物完全燃烧的规律,可判断混合气体中含C、H元素,利用水、二氧化碳的质量进一步确定混合气体中C、H元素的质量比,以此来解答.
解答 解:由生成的气体通过浓硫酸,装置质量增加3.6g,可判断燃烧生成了3.6g水,说明混合气体中含氢元素,且氢元素质量=3.6g×$\frac{2}{18}$×100%=0.4g;
由气体通过氢氧化钠溶液,装置质量增加4.4g,可判断燃烧生成了2.2g二氧化碳,说明混合气体中含碳元素,且碳元素质量=4.4g×$\frac{12}{44}$×100%=1.2g;
甲烷气体中C、H元素质量比=12:(1×4)=3:1,则混合气体中C、H元素质量比=1.2:0.4g=3:1,
因此可判断混合气体可能只有甲烷;也可能只含有CO和H2;也可能是甲烷、氢气、一氧化碳同时存在,不可能含有甲烷和另外任何一种气体.
只有A选项符合题意.
故选A.
点评 本题考查物质的推断,为高频考点,把握物质的性质、发生的反应及守恒法为解答的关键,侧重分析与应用能力的考查,注意守恒法的应用,题目难度不大.

练习册系列答案
 阶梯计算系列答案
阶梯计算系列答案
相关题目
2.下列实验装置或操作不符合实验要求的是( )
| A. |  石油分馏 | B. | 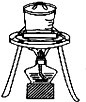 灼烧干海带 | ||
| C. |  用CCl4提取碘水中的碘 | D. | 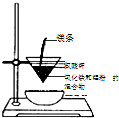 冶炼金属铁 |
3.在强酸性溶液中,下列各组离子一定能大量共存的是( )
| A. | Cl-、Cu2+、SO42-、NO3- | B. | OH-、Na+、SO42-、CH3COO- | ||
| C. | Cl-、Fe2+、MnO4-、NO3- | D. | AlO2-、Na+、CO32-、NO3- |
20.工业上生产Na、Ca、Mg都用电解熔融的氯化物,但K不能用电解熔融态的方法得到,因金属钾易溶于熔融态的KCl而有危险,很难制得K,且降低电流效率.现生产钾是用金属钠和KCl在850℃反应制取,有关的反应式为:KCl+Na=NaCl+K↑下列说法错误的是( )
| A. | 该反应850℃的选择是基于熔沸点的考虑 | |
| B. | 该反应不能在空气中进行 | |
| C. | 该反应属于置换反应的类型 | |
| D. | 该反应表明钠比钾的活动性强 |
7.下列分子中,属于非极性分子的是( )
| A. | SO2 | B. | BeCl2 | C. | NF3 | D. | COCl2 |
17.将铜和碳的混合物在空气中充分灼烧,混合物的质量在冷却后没有变化,则原混合物中铜和碳的质量比为( )
| A. | 1:1 | B. | 1:4 | C. | 4:1 | D. | 无法确定 |
4.如表是A、B、C、D、E五种有机物的有关信息:
回答下列问题:
(1)A与溴的四氯化碳溶液反应的生成物的名称是1,2-二溴乙烷.
(2)A与氢气发生加成反应后生成物质F,与F在分子组成和结构上相似的有机物有一大类(俗称“同系物”),它们均符合通式CnH2n+2.当n=4时,这类有机物开始出现同分异构体.
(3)B具有的性质是②③(填序号).
①无色无味液体 ②有毒 ③不溶于水 ④密度比水大
⑤与酸性KMnO4溶液和溴水反应褪色 ⑥任何条件下不与氢气反应
写出在浓硫酸作用下,B与浓硝酸反应的化学方程式: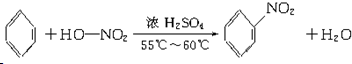 .
.
(4)C与E反应能生成相对分子质量为100的酯,该反应的反应类型为酯化反应;
(5)写出由C氧化生成D的化学方程式2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O.
| A | ①能使溴的四氯化碳溶液褪色;②比例模型为; ③能与水在一定条件下反应生成C ③能与水在一定条件下反应生成C |
| B | ①由C、H两种元素组成;②球棍模型为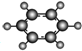 |
| C | ①由C、H、O三种元素组成;②能与Na反应,但不能与NaOH溶液反应;③能与E反应生成相对分子质量为100的酯 |
| D | ①相对分子质量比C少2;②能由C氧化而成 |
| E | ①由C、H、O三种元素组成;②球棍模型为 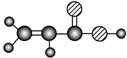 |
(1)A与溴的四氯化碳溶液反应的生成物的名称是1,2-二溴乙烷.
(2)A与氢气发生加成反应后生成物质F,与F在分子组成和结构上相似的有机物有一大类(俗称“同系物”),它们均符合通式CnH2n+2.当n=4时,这类有机物开始出现同分异构体.
(3)B具有的性质是②③(填序号).
①无色无味液体 ②有毒 ③不溶于水 ④密度比水大
⑤与酸性KMnO4溶液和溴水反应褪色 ⑥任何条件下不与氢气反应
写出在浓硫酸作用下,B与浓硝酸反应的化学方程式:
 .
.(4)C与E反应能生成相对分子质量为100的酯,该反应的反应类型为酯化反应;
(5)写出由C氧化生成D的化学方程式2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O.
1.下列叙述中不正确的是( )
| A. | 电镀时,电镀池里的阳极材料发生氧化作用 | |
| B. | 电解饱和食盐水制烧碱,用涂镍碳钢网作阴极 | |
| C. | 惰性电极电解氯化铜溶液,在阴极上和阳极上析出产物的物质的量之比为1:1 | |
| D. | 电解熔融的氧化铝制取金属铝,用铁作阳极 |
15.某种解热镇痛药的结构简式如图所示,当它完全水解时,不可能得到的产物是( )
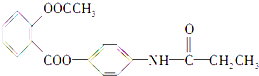
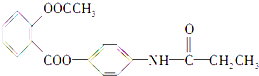
| A. | CH3CH2COOH | B. | CH3COOH | C. | CH3OH | D. | 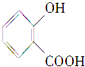 |