题目内容
3.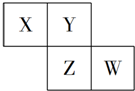 X、Y、Z、W均为短周期元素,它们在元素周期表中的位置如图所示,若W原子的最外层电子数是内层电子总数的$\frac{7}{10}$,下列说法中正确的是( )
X、Y、Z、W均为短周期元素,它们在元素周期表中的位置如图所示,若W原子的最外层电子数是内层电子总数的$\frac{7}{10}$,下列说法中正确的是( )| A. | 阴离子的半径从大到小排列顺序为:X>Y>Z>W | |
| B. | X、Y、Z、W元素的氢化物分子间都可以形成氢键 | |
| C. | Y的两种同素异形体在常温下可以相互转化 | |
| D. | 最高价氧化物对应的水化物的酸性:W>Z |
分析 W原子的最外层电子数是内层电子总数的$\frac{7}{10}$,应为Cl,由元素在周期表中的位置可知X为N元素,Y为O元素,Z为S元素,
A.原子核外电子层数越多,离子半径越大;
B.S、Cl的非金属性较弱,氢化物分子间不存在氢键;
C.Y为O,对应的两种同素异形体在放电条件下可以相互转化;
D.非金属性Cl>S,元素的非金属性越强,对应的最高价氧化物对应的水化物的酸性越强.
解答 解:W原子的最外层电子数是内层电子总数的$\frac{7}{10}$,应为Cl,由元素在周期表中的位置可知X为N元素,Y为O元素,Z为S元素,
A.原子核外电子层数越多,离子半径越大,应为Z>W>X>Y,故A错误;
B.S、Cl的非金属性较弱,氢化物分子间不存在氢键,故B错误;
C.Y为O,对应的两种同素异形体在放电条件下可以相互转化,故C错误;
D.非金属性Cl>S,元素的非金属性越强,对应的最高价氧化物对应的水化物的酸性越强,故D正确.
故选D.
点评 本题考查了元素周期表和元素周期律的综合应用,为高频考点,题目难度中等,正确推断各元素名称为解答关键,注意掌握原子结构与元素周期表、元素周期律的关系.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
20.工业上生产Na、Ca、Mg都用电解熔融的氯化物,但K不能用电解熔融态的方法得到,因金属钾易溶于熔融态的KCl而有危险,很难制得K,且降低电流效率.现生产钾是用金属钠和KCl在850℃反应制取,有关的反应式为:KCl+Na=NaCl+K↑下列说法错误的是( )
| A. | 该反应850℃的选择是基于熔沸点的考虑 | |
| B. | 该反应不能在空气中进行 | |
| C. | 该反应属于置换反应的类型 | |
| D. | 该反应表明钠比钾的活动性强 |
1.下列叙述中不正确的是( )
| A. | 电镀时,电镀池里的阳极材料发生氧化作用 | |
| B. | 电解饱和食盐水制烧碱,用涂镍碳钢网作阴极 | |
| C. | 惰性电极电解氯化铜溶液,在阴极上和阳极上析出产物的物质的量之比为1:1 | |
| D. | 电解熔融的氧化铝制取金属铝,用铁作阳极 |
18.下列关于原子结构及微粒间的数量关系的说法错误的是( )
| A. | 同种元素的原子均有相同的质子数和中子数 | |
| B. | 微粒Na+、Mg2+、O2-具有相同的电子层结构 | |
| C. | 短周期第ⅣA与ⅥIA族元素的原子间构成的分子,均满足原子最外层8电子结构 | |
| D. | ${\;}_{20}^{48}$Ca2+的中子数比核外电子数多10 |
8.某有机物的结构简式如图所示:下列有关该有机物的叙述正确的是( )


| A. | 该有机物的分子式为C11H14O3 | |
| B. | 该有机物可能易溶于水且具有水果香味 | |
| C. | 该有机物可能发生的化学反应类型有:水解、酯化、氧化、取代 | |
| D. | 1mol该有机物在Ni作催化剂的条件下能与4molH2发生加成反应 |
15.某种解热镇痛药的结构简式如图所示,当它完全水解时,不可能得到的产物是( )
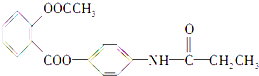
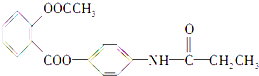
| A. | CH3CH2COOH | B. | CH3COOH | C. | CH3OH | D. | 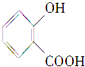 |
13.等质量的两块钠,第一块在足量氧气中加热,第二块在足量氧气(常温)中充分反应,则下列说法正确的是( )
| A. | 第一块钠消耗的氧气多 | B. | 两块钠消耗的氧气一样多 | ||
| C. | 第二块钠的反应产物质量大 | D. | 两块钠的反应产物质量一样大 |