题目内容
X、Y、Z、W四种常见元素,其中X、Y、Z为短周期元素.有关信息如下表:
(1)W在周期表的位置为 ,W(OH)2在空气中不稳定,极易被氧化,由白色迅速变成灰绿色,最后变成红褐色,反应的化学方程式为 .
(2)X的简单阴离子的结构示意图为 ,X的最高价氧化物对应水化物的水溶液与Y的氧化物反应的离子方程式为 .
(3)Z的氧化物在通讯领域用来作 ,工业上制备Z的单质的化学反应方程式为 .
锗与Z是同一主族元素,门捷列夫曾预言了这一元素的存在,它用来制造半导体晶体管,最新研究表明:有机锗具有明显的抗肿瘤活性,锗不与NaOH 溶液反应但在有H2O2 存在时可与NaOH 溶液反应生成锗酸盐,其方程式为 .
(4)在50mL l mol?L-1的YX3溶液中逐滴加入0.5mol?L-1的NaOH溶液,得到1.56g沉淀,则加入NaOH溶液的体积最多为 mL.
| 原子或分子相关信息 | 单质及其化合物相关信息 | |||
| X | ZX4分子是由粗Z提纯Z的中间产物 | X的最高价氧化物对应的水化物为无机酸中最强酸 | ||
| Y | Y原子的最外层电子数等于电子层数 | Y的氧化物是典型的两性氧化物,可用于制造一种极有前途的高温材料 | ||
| Z | Z原子的最外层电子数是次外层电子数的
| Z是无机非金属材料的主角,其单质是制取大规模集成电路的主要原料 | ||
| W | W原子的最外层电子数小于4 | W的常见化合价有+3、+2,WX3稀溶液呈黄色 |
(2)X的简单阴离子的结构示意图为
(3)Z的氧化物在通讯领域用来作
锗与Z是同一主族元素,门捷列夫曾预言了这一元素的存在,它用来制造半导体晶体管,最新研究表明:有机锗具有明显的抗肿瘤活性,锗不与NaOH 溶液反应但在有H2O2 存在时可与NaOH 溶液反应生成锗酸盐,其方程式为
(4)在50mL l mol?L-1的YX3溶液中逐滴加入0.5mol?L-1的NaOH溶液,得到1.56g沉淀,则加入NaOH溶液的体积最多为
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:Z原子的最外层电子数是次外层电子数的
,Z是无机非金属材料的主角,其单质是制取大规模集成电路的主要原料,故Z为Si;
ZX4分子是由粗Si提纯Si的中间产物,X的最高价氧化物对应的水化物为无机酸中最强酸,故可推断为Cl;
Y原子的最外层电子数等于电子层数,Y的氧化物是典型的两性氧化物,可用于制造一种极有前途的高温材料,故Y为Al;
W原子的最外层电子数小于4,W的常见化合价有+3、+2,WX3稀溶液呈黄色,X为Cl,故W为Fe,据此解答各小题即可.
| 1 |
| 2 |
ZX4分子是由粗Si提纯Si的中间产物,X的最高价氧化物对应的水化物为无机酸中最强酸,故可推断为Cl;
Y原子的最外层电子数等于电子层数,Y的氧化物是典型的两性氧化物,可用于制造一种极有前途的高温材料,故Y为Al;
W原子的最外层电子数小于4,W的常见化合价有+3、+2,WX3稀溶液呈黄色,X为Cl,故W为Fe,据此解答各小题即可.
解答:
解:依据分析可知:X为氯,Y为铝,Z为硅,W为铁,
(1)W为Fe,Fe处于第四周期 VIII族,Fe(OH)2在空气中不稳定,极易被氧化,由白色迅速变成灰绿色,最后变成红褐色,反应的化学方程式为:4Fe(OH)2+O2+2H2O═4Fe(OH)3,故答案为:第四周期 VIII族;4Fe(OH)2+O2+2H2O═4Fe(OH)3;
(2)X为Cl,Cl的简单阴离子有3个电子层,最外层得到一个变为8个电子的稳定结构,故离子的结构示意图为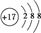 ,强酸与氧化铝反应,氧化铝变为铝离子,水不能拆,故离子反应方程式为:6H++Al2O3=2Al3++3H2O,故答案为:
,强酸与氧化铝反应,氧化铝变为铝离子,水不能拆,故离子反应方程式为:6H++Al2O3=2Al3++3H2O,故答案为: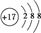 ;6H++Al2O3=2Al3++3H2O;
;6H++Al2O3=2Al3++3H2O;
(3)二氧化硅常用作光导纤维,工业上利用C还原二氧化硅制取硅单质,化学反应方程式为:SiO2+2C
Si+2CO↑,锗不与NaOH 溶液反应但在有H2O2 存在时可与NaOH溶液反应生成锗酸盐,据此可写出化学反应方程式为:Ge+2 H2O2+2NaOH=Na2GeO3+3H2O,
故答案为:光导纤维;SiO2+2C
Si+2CO↑; Ge+2 H2O2+2NaOH=Na2GeO3+3H2O;
(4)50mL 1mol/L的AlCl3溶液中氯化铝的物质的量=0.05L×1mol/L=0.05mol,若Al元素都转化为氢氧化铝沉淀,则氢氧化铝沉淀的质量=0.05mol×78g/mol=3.9g>1.56g,说明有两种情况:一为沉淀不完全,只生成Al(OH)3沉淀;另一种情况为沉淀部分溶解,既生成Al(OH)3沉淀,又生成NaAlO2,
n[Al(OH)3]=
=0.02mol,
①若碱不足,由Al3++3OH-═Al(OH)3↓可知,NaOH的物质的量为0.02mol×3=0.06mol,加入NaOH溶液的体积为
=0.12L=120mL;
②沉淀部分溶解,既生成Al(OH)3沉淀,又生成NaAlO2,则:
Al3++3OH-═Al(OH)3↓
0.05mol 0.15mol 0.05mol
Al(OH)3+OH-═AlO2-+2H2O
(0.05-0.02)mol (0.05-0.02)mol
则消耗的碱的物质的量为0.15mol+(0.05-0.02)mol=0.18mol,
加入NaOH溶液的体积为
=0.36L=360mL,故消耗NaOH的最大体积为360mL,故答案为:360.
(1)W为Fe,Fe处于第四周期 VIII族,Fe(OH)2在空气中不稳定,极易被氧化,由白色迅速变成灰绿色,最后变成红褐色,反应的化学方程式为:4Fe(OH)2+O2+2H2O═4Fe(OH)3,故答案为:第四周期 VIII族;4Fe(OH)2+O2+2H2O═4Fe(OH)3;
(2)X为Cl,Cl的简单阴离子有3个电子层,最外层得到一个变为8个电子的稳定结构,故离子的结构示意图为
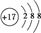 ,强酸与氧化铝反应,氧化铝变为铝离子,水不能拆,故离子反应方程式为:6H++Al2O3=2Al3++3H2O,故答案为:
,强酸与氧化铝反应,氧化铝变为铝离子,水不能拆,故离子反应方程式为:6H++Al2O3=2Al3++3H2O,故答案为: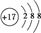 ;6H++Al2O3=2Al3++3H2O;
;6H++Al2O3=2Al3++3H2O;(3)二氧化硅常用作光导纤维,工业上利用C还原二氧化硅制取硅单质,化学反应方程式为:SiO2+2C
| ||
故答案为:光导纤维;SiO2+2C
| ||
(4)50mL 1mol/L的AlCl3溶液中氯化铝的物质的量=0.05L×1mol/L=0.05mol,若Al元素都转化为氢氧化铝沉淀,则氢氧化铝沉淀的质量=0.05mol×78g/mol=3.9g>1.56g,说明有两种情况:一为沉淀不完全,只生成Al(OH)3沉淀;另一种情况为沉淀部分溶解,既生成Al(OH)3沉淀,又生成NaAlO2,
n[Al(OH)3]=
| 1.56g |
| 78g/mol |
①若碱不足,由Al3++3OH-═Al(OH)3↓可知,NaOH的物质的量为0.02mol×3=0.06mol,加入NaOH溶液的体积为
| 0.06mol |
| 0.5mol/L |
②沉淀部分溶解,既生成Al(OH)3沉淀,又生成NaAlO2,则:
Al3++3OH-═Al(OH)3↓
0.05mol 0.15mol 0.05mol
Al(OH)3+OH-═AlO2-+2H2O
(0.05-0.02)mol (0.05-0.02)mol
则消耗的碱的物质的量为0.15mol+(0.05-0.02)mol=0.18mol,
加入NaOH溶液的体积为
| 0.18mol |
| 0.5mol/L |
点评:本题主要考查的是元素的推断以及元素化合物的知识,正确推断出各种元素是解决本题的关键,属于常考题.

练习册系列答案
 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案
相关题目
能正确表示下列化学反应的离子方程式的是( )
| A、氢氧化钡溶液与硫酸的反应:OH-+H+=H2O |
| B、碳酸钙溶于稀盐酸中:CaCO3+2H+=Ca2++H2O+CO2↑ |
| C、CH3COOH溶液与NH3?H2O溶液反应:H++OH-═H2O |
| D、澄清的石灰水与稀盐酸反应:Ca(OH)2+2H+=Ca2++2H2O |
下列叙述正确的是( )
| A、当反应中有一种元素被氧化时,一定有另一种元素被还原 |
| B、在化学反应中,得电子越多的氧化剂,其氧化性就越强 |
| C、阳离子只能得到电子被还原,阴离子只能失去电子被氧化 |
| D、含有最高价元素的化合物不一定具有很强的氧化性 |
设NA为阿伏加德罗常数,下列说法中,正确的是( )
| A、18 g水所含分子数目为NA |
| B、17 g NH3所含氢原子数目为NA |
| C、标准状况下,2.24L O2所含的原子数为0.2NA |
| D、2.4 g金属镁所含电子数目为0.2NA |
在由水电离的c(H+)=10-14 mol?L-1的溶液中,一定能大量共存的离子组是( )
| A、K+、Fe2+、SO42-、Mg2+ |
| B、Na+、Cl-、NH4+、S2- |
| C、Al3+、Na+、Cl-、S2- |
| D、Na+、K+、Br-、Cl- |
下列各组离子在指定溶液中,能大量共存的是( )
①无色溶液中:K+、Na+、MnO4-、SO42-
②pH=13的溶液中:CO32-、Na+、AlO2-、NO3-
③在由水电离出的c(H+)=1×10-12mol/L的溶液中Ba2+
④强酸性溶液中:Fe2+、Na+、NO3-、SO42-
⑤强酸性溶液中:Fe2+、Al3+、NO3-、Cl-.
①无色溶液中:K+、Na+、MnO4-、SO42-
②pH=13的溶液中:CO32-、Na+、AlO2-、NO3-
③在由水电离出的c(H+)=1×10-12mol/L的溶液中Ba2+
④强酸性溶液中:Fe2+、Na+、NO3-、SO42-
⑤强酸性溶液中:Fe2+、Al3+、NO3-、Cl-.
| A、②③ | B、②④⑤ |
| C、①②⑤ | D、②④ |
下列说法正确的是( )
| A、电子层结构相同的微粒,其化学性质一定相似 |
| B、第三周期非金属元素含氧酸的酸性从左到右依次增强 |
| C、非金属元素的原子两两结合形成的化合物不一定是共价化合物 |
| D、元素周期律是元素原子核外电子排布周期性变化的结果 |
X、Y、Z和W代表原子序数依次增大的四种短周期元素,X原子核内没有中子,在周期表中,Z与Y、W均相邻;Y、Z和W三种元素的原子最外层电子数之和为17.则下列有关叙述正确的是( )
| A、Y、Z和W三种元素可能位于同一周期 |
| B、Y和W所形成的含氧酸均为强酸 |
| C、X、Y、Z和W可以组成原子的物质的量之比为5:1:4:1的离子化合物 |
| D、上述元素形成的氢化物中,W的氢化物相对分子质量最大,熔沸点最高 |