题目内容
1.下列化学用语正确的是( )| A. | 苯的最简式:C6H6 | B. | 乙醇的分子式:CH3CH2OH | ||
| C. | 乙烯的结构简式:CH2CH2 | D. | 2-乙基-1,3-丁二烯分子的键线式: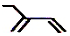 |
分析 A.苯的分子式为C6H6,最简原子比为1:1;
B.1个乙醇分子中含2个C、6个H、1个O;
C.结构简式中不能省略碳碳双键;
D.2-乙基-1,3-丁二烯含2个双键,2号C上有乙基,用线表示化学键,用折点表示C原子,以此表示键线式.
解答 解:A.苯的分子式为C6H6,最简原子比为1:1,最简式为CH,故A错误;
B.1个乙醇分子中含2个C、6个H、1个O,分子式为C2H6O,结构简式为CH3CH2OH,故B错误;
C.结构简式中不能省略碳碳双键,则结构简式为CH2=CH2,故C错误;
D.2-乙基-1,3-丁二烯含2个双键,2号C上有乙基,键线式为 ,故D正确;
,故D正确;
故选D.
点评 本题考查分子式、结构式、结构简式等,为高频考点,把握化学用语的区别、书写为解答的关键,侧重分析与应用能力的考查,注意化学用语的规范使用,题目难度不大.

练习册系列答案
相关题目
11.根据表(部分短周期元家的原子半径及主要化合价)信息,完成有关问题:
(1)A、B、D、E的简单离子半径由大到小的顺序是S2->O2->Na+>Al3+(用具体离子符号表示);
(2)B单质和C单质的化学性质相似,试写出C单质与强碱溶液反应的离子方程式Be+2OH-=BeO22-+H2↑;
(3)D和E组成的两种化合物中具有漂白性的是SO2,该化合物转化为另一种化合物的化学方程式为2SO2+O2$?_{△}^{催化剂}$2SO3 ;
(4)已知A的氢化物能与水反应生成一种可燃性气体和一种强碱,试写出该反应的化学方程式NaH+H2O=NaOH+H2↑.
| 元素代号 | A | B | C | D | E |
| 原子半径/nm | 0.186 | 0.143 | 0.089 | 0.104 | 0.074 |
| 主要化合价 | +1 | +3 | +2 | +6、-2 | -2 |
(2)B单质和C单质的化学性质相似,试写出C单质与强碱溶液反应的离子方程式Be+2OH-=BeO22-+H2↑;
(3)D和E组成的两种化合物中具有漂白性的是SO2,该化合物转化为另一种化合物的化学方程式为2SO2+O2$?_{△}^{催化剂}$2SO3 ;
(4)已知A的氢化物能与水反应生成一种可燃性气体和一种强碱,试写出该反应的化学方程式NaH+H2O=NaOH+H2↑.
12.某温度时,CaC2O4在水中的沉淀溶解平衡曲线如图所示,下列说法正确的是( )

| A. | 向CaC2O4饱和溶液中加入固体Na2C2O4可以由a点变到b点 | |
| B. | 通过蒸发可以由d点变到c点 | |
| C. | d点无CaC2O4沉淀生成 | |
| D. | a点对应的Ksp大于c点对应的Ksp |
9.下列叙述中正确的是( )
| A. | NH3、CO、CO2都是极性分子 | |
| B. | CH4、CCl4都是含有极性键的非极性分子 | |
| C. | 分子晶体熔点越高,其稳定性越增强 | |
| D. | CS2、H2O、C2H2都是直线形分子 |
6.下列化学用语的书写,正确的是( )
| A. | H2S的电子式: | B. | 硫原子的结构示意图: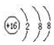 | ||
| C. | 氮气的电子式: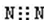 | D. | 水分子的结构式: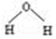 |
10.下列实验方案不能达到实验目的是( )
| 实验目的 | 实验方案 | |
| A | 证明溴乙烷发生消去反应有乙烯生成 | 向试管中加入适量的溴乙烷和NaOH的乙醇溶液,加热,将反产生的气体通入溴的四氯化碳溶液 |
| B | 检验卤代烃中卤原子的种类 | 将溴乙烷与氢氧化钠溶液共热,取冷却后反应液 滴加硝酸酸化后滴加硝酸银溶液 |
| C | 验证乙炔能被酸性高锰酸钾溶液氧化 | 将电石与饱和食盐水反应生成的气体通入酸性高锰酸钾溶液,观察溶液是否褪色 |
| D | 验证苯和液溴在FeBr3的催化下发生取代反应 | 将反应产生的混合气体先通入溴的四氯化碳溶液再通入AgNO3溶液中,观察是否有淡黄色沉淀生成 |
| A. | A | B. | B | C. | C | D. | D |
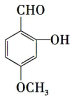 B.
B.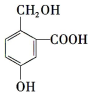 C.
C.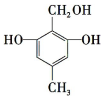 D.
D.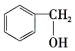
 ;D微粒的核外电子排布式为1s2 2s22p6 3s23p6.
;D微粒的核外电子排布式为1s2 2s22p6 3s23p6.