题目内容
用NA表示阿伏伽德罗常数的值.下列叙述正确的是( )
| A、0.1mol/LAlCl3溶液中含有的Cl-数目为0.3NA |
| B、室温下,42.0g己烯和丙烯的混合气体中含有的碳原子数为3NA |
| C、标准状况下,2.24LCl2与足量的NaOH溶液反应,转移的电子数目为0.2NA |
| D、100mL18.4mol/L硫酸与足量铜反应,生成SO2的分子数为0.92NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、缺少溶液的体积,无法计算;
B、以己烯和丙烯的最简式CH2计算;
C、氯气和氢氧化钠溶液发生歧化反应,转移电子数等于反应掉的氯气分子数;
D、随着反应的进行,浓硫酸浓度逐渐降低,铜与稀硫酸不反应.
B、以己烯和丙烯的最简式CH2计算;
C、氯气和氢氧化钠溶液发生歧化反应,转移电子数等于反应掉的氯气分子数;
D、随着反应的进行,浓硫酸浓度逐渐降低,铜与稀硫酸不反应.
解答:
解:A、缺少AlCl3溶液的体积,无法计算Cl-数目,故A错误;
B、己烯和丙烯的最简式CH2,42g混合气体中含有n(CH2)=
=3mol,因此N(C)=N(CH2)=3mol×NAmol-1=3NA,故B正确;
C、标准状况下,2.24LCl2的物质的量为0.1mol,分子数为0.1NA,氯气和氢氧化钠溶液发生歧化反应,转移电子数等于反应掉的氯气分子数,因此转移电子数为0.1NA,故C错误;
D、随着反应的进行,浓硫酸浓度逐渐降低,铜与稀硫酸不反应,因此生成SO2的分子数少于0.92NA,故D错误;
故选B.
B、己烯和丙烯的最简式CH2,42g混合气体中含有n(CH2)=
| 42g |
| 14g/mol |
C、标准状况下,2.24LCl2的物质的量为0.1mol,分子数为0.1NA,氯气和氢氧化钠溶液发生歧化反应,转移电子数等于反应掉的氯气分子数,因此转移电子数为0.1NA,故C错误;
D、随着反应的进行,浓硫酸浓度逐渐降低,铜与稀硫酸不反应,因此生成SO2的分子数少于0.92NA,故D错误;
故选B.
点评:本题考查了阿伏加德罗常数的计算,为高考高频考点,侧重于转移电子数、最简式应用、化学反应原理的应用,题目难度一般.

练习册系列答案
 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案
相关题目
我国科学家在世界上第一次为一种名为“钴酞菁”的分子(直径为1.3×10-9m、分子式为C32H16N8Co)恢复了磁性.已知该物质主要用于有机反应中的催化剂以及光电子等高新技术领域.下列说法中不正确的是( )
| A、“钴酞菁”分子所形成的分散系具有丁达尔效应 |
| B、该物质属于有机高分子化合物 |
| C、此项工作的研究表明,人们可以改变分子的某些物理性质 |
| D、此项研究结果可广泛应用于光电器件、生物技术等方面 |
在海洋底部存在大量称为“可燃冰”的物质,其蕴藏量是地球上煤、石油的几百倍,因而是一种等待开发的巨大能源物质.初步查明可燃冰是甲烷、乙烷等可燃性气体的水合物.有关可燃冰的下述推测中不正确的是( )
| A、高压、低温有助于可燃冰的形成 |
| B、构成可燃冰的原子间存在极性共价键 |
| C、可燃冰的微粒间可能存在一种比范德华力更强的相互作用力 |
| D、常温、常压下可燃冰是一种稳定的物质 |
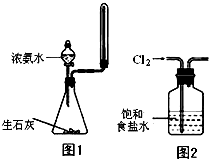 下列有关实验没有明显错误的是( )
下列有关实验没有明显错误的是( )| A、使用湿润过的pH试纸测量某溶液的pH |
| B、实验室可以用图1所示装置来制取少量氨气 |
| C、用量筒量取20 mL 0.50mol?L-1H2SO4溶液于烧杯中,加水80 mL,配制成0.10mol?L-1H2SO4溶液 |
| D、实验室用图2所示装置除去Cl2中的少量HCl |
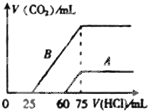 向10mL某浓度的NaOH溶液中通入CO2气体后得溶液M,因CO2通入量的不同,溶液M的组成也不同.若向M中逐滴加入0.1mol/L盐酸,产生的气体V(CO2)与加入盐酸的体积V(HCl)的关系有图示两种情况,则下列分析判断不正确的是(不考虑CO2的溶解)( )
向10mL某浓度的NaOH溶液中通入CO2气体后得溶液M,因CO2通入量的不同,溶液M的组成也不同.若向M中逐滴加入0.1mol/L盐酸,产生的气体V(CO2)与加入盐酸的体积V(HCl)的关系有图示两种情况,则下列分析判断不正确的是(不考虑CO2的溶解)( )| A、曲线A表明M中的溶质为NaOH、Na2CO3 |
| B、曲线B表明M中NaHCO3与Na2CO3的物质的量之比为1:2 |
| C、原NaOH溶液的物质的量浓度为0.75mol/L |
| D、由A.B可知,两次实验通入的CO2的体积比3:10 |
下列说法正确的是( )
| A、绿色化学就是研究绿色物质的化学 |
| B、烷烃是一类饱和链烃,其分子都是直线型的 |
| C、甲烷是烷烃中碳元素的质量分数最低的,也是最简单的烃 |
| D、“春蚕到死丝方尽,蜡炬成灰泪始干”中的“丝”和“泪”分别是指纤维素和油脂 |
下列关于卤素及其化合物的叙述正确的是( )
| A、HF水溶液可存放在玻璃试剂瓶中 |
| B、Br2可从KCl溶液中置换出氯 |
| C、F、Cl、Br、I的非金属性依次减弱 |
| D、HF、HCl、HBr、HI的稳定性依次增强 |
下列说法正确的是( )
| A、pH=6.8的溶液一定显酸性 |
| B、电离平衡常数(K)只与弱电解质本身有关,与其它外部因素无关 |
| C、0.1 mol?L-1的硫化钠溶液中:c(H+)+c(Na+)=c(OH-)+c(HS-)+c(S2-) |
| D、相同物质的量浓度的下列溶液中:①NH4Al(SO4)2、②NH4Cl、③CH3COONH4,则c(NH4+)由大到小的顺序是:①>②>③ |