题目内容
下列说法正确的是( )
| A、pH=6.8的溶液一定显酸性 |
| B、电离平衡常数(K)只与弱电解质本身有关,与其它外部因素无关 |
| C、0.1 mol?L-1的硫化钠溶液中:c(H+)+c(Na+)=c(OH-)+c(HS-)+c(S2-) |
| D、相同物质的量浓度的下列溶液中:①NH4Al(SO4)2、②NH4Cl、③CH3COONH4,则c(NH4+)由大到小的顺序是:①>②>③ |
考点:弱电解质在水溶液中的电离平衡,离子浓度大小的比较
专题:电离平衡与溶液的pH专题
分析:A、温度不确定,无法根据pH确定溶液的酸碱性;
B、电离平衡常数(K)只与弱电解质本身有关,和温度有关;
C、溶液中存在电荷守恒;
D、根据铵根离子水解平衡移动的影响因素来回答.
B、电离平衡常数(K)只与弱电解质本身有关,和温度有关;
C、溶液中存在电荷守恒;
D、根据铵根离子水解平衡移动的影响因素来回答.
解答:
解:A、温度不确定,无法根据pH确定溶液的酸碱性,pH=6.8的溶液不一定显酸性,还可能是中性、碱性,故A错误;
B、电离平衡常数(K)只与弱电解质本身有关,还和外部因素温度有关,故B错误;
C、0.1 mol?L-1的硫化钠溶液中:存在电荷守恒:c(H+)+c(Na+)=c(OH-)+c(HS-)+2c(S2-),故C错误;
D、①NH4Al(SO4)2中铝离子抑制铵根离子水解,②NH4Cl中铵根离子的水解不受影响,CH3COONH4中醋酸根离子促进铵根离子的水解,所以c(NH4+)由大到小的顺序是:①>②>③,故D正确.
故选D.
B、电离平衡常数(K)只与弱电解质本身有关,还和外部因素温度有关,故B错误;
C、0.1 mol?L-1的硫化钠溶液中:存在电荷守恒:c(H+)+c(Na+)=c(OH-)+c(HS-)+2c(S2-),故C错误;
D、①NH4Al(SO4)2中铝离子抑制铵根离子水解,②NH4Cl中铵根离子的水解不受影响,CH3COONH4中醋酸根离子促进铵根离子的水解,所以c(NH4+)由大到小的顺序是:①>②>③,故D正确.
故选D.
点评:本题考查学生弱电解质在水溶液中的电离平衡以及盐的水解原理的应用知识,属于综合知识的考查题,难度中等.

练习册系列答案
相关题目
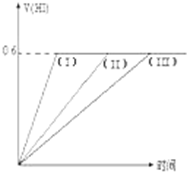 在一定温度下发生反应:I2(g)+H2(g)?2HI(g);并达平衡.HI的体积分数V(HI)%随时间变化如图曲线(II)所示.若改变反应条件,在甲条件下的变化如曲线(I)所示.在乙条件下的变化如曲线(III)所示.则甲条件、乙条件分别是( )
在一定温度下发生反应:I2(g)+H2(g)?2HI(g);并达平衡.HI的体积分数V(HI)%随时间变化如图曲线(II)所示.若改变反应条件,在甲条件下的变化如曲线(I)所示.在乙条件下的变化如曲线(III)所示.则甲条件、乙条件分别是( ) ①恒容条件下,升高温度
②恒容条件下,降低温度
③恒温条件下,缩小反应容器体积
④恒温条件下,扩大反应容器体积
⑤恒温恒容条件下,加入适当的催化剂.
| A、①⑤,③ | B、②⑤,④ |
| C、③⑤,② | D、③⑤,④ |
用NA表示阿伏伽德罗常数的值.下列叙述正确的是( )
| A、0.1mol/LAlCl3溶液中含有的Cl-数目为0.3NA |
| B、室温下,42.0g己烯和丙烯的混合气体中含有的碳原子数为3NA |
| C、标准状况下,2.24LCl2与足量的NaOH溶液反应,转移的电子数目为0.2NA |
| D、100mL18.4mol/L硫酸与足量铜反应,生成SO2的分子数为0.92NA |
设NA代表阿伏加德罗常数,下列叙述正确的是( )
| A、0.1 mol/L NaHCO3和0.1 mol/L Na2CO3混合溶液1L,HCO3-,CO32-的总数为0.2NA |
| B、向密闭容器中充入2molN2和3molH2,在一定条件下发生反应,达到平衡时,混合气体中NH3的体积分数为23.45%,则H2和NH3所含的H原子总数为6NA |
| C、若1L0.1 mol/L的CH3COOH溶液含CH3COO- 数为aNA,则1L0.3 mol/L的CH3COOH溶液含CH3COO- 数小于0.3aNA |
| D、反应N2+3H2?2NH3达平衡时,每形成6NA个N-H键,也生成14克N2 |
乙醇分子所含官能团的名称是( )
| A、乙氧基 | B、羟基 | C、乙基 | D、甲基 |
下列装置能达到实验目的是( )
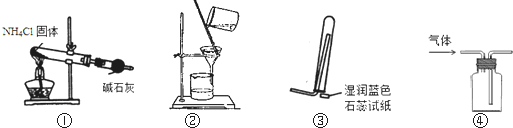

| A、用①装置制取干燥的氨气 |
| B、用②装置除去淀粉溶液中的NaCl |
| C、③装置可用于氨气的收集、检验 |
| D、④装置可用排空气法收集氢气 |
由乙烯和乙酸蒸气组成的混和气体中,若碳元素的质量百分含量为60%,则氧元素的质量百分含量为( )
| A、10% | B、20% |
| C、30% | D、无法确定 |
已知H2(g)+I2(g)?2HI(g),现有相同容积的体积可变的两个绝热容器甲和乙,甲中加入H2和I2各0.1mol,乙中加入HI 0.2mol,起始温度相同的条件下分别达到平衡.下列说法正确的是( )
| A、平衡时甲、乙两容器体积相等 |
| B、平衡时甲、乙两容器中c(H2)相等 |
| C、平衡时甲、乙两容器中反应速率v(H2)相等 |
| D、平衡时甲、乙两容器中气体总的物质的量相等 |
 在容积相同的不同密闭容器内,分别充入同量的N2和H2,在不同温度,任其发生反应N2+3H2?2NH3,在第7秒时分别测定其中NH3的体积分数φ(NH3),并绘成如图曲线.
在容积相同的不同密闭容器内,分别充入同量的N2和H2,在不同温度,任其发生反应N2+3H2?2NH3,在第7秒时分别测定其中NH3的体积分数φ(NH3),并绘成如图曲线.