题目内容
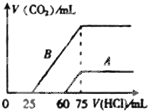 向10mL某浓度的NaOH溶液中通入CO2气体后得溶液M,因CO2通入量的不同,溶液M的组成也不同.若向M中逐滴加入0.1mol/L盐酸,产生的气体V(CO2)与加入盐酸的体积V(HCl)的关系有图示两种情况,则下列分析判断不正确的是(不考虑CO2的溶解)( )
向10mL某浓度的NaOH溶液中通入CO2气体后得溶液M,因CO2通入量的不同,溶液M的组成也不同.若向M中逐滴加入0.1mol/L盐酸,产生的气体V(CO2)与加入盐酸的体积V(HCl)的关系有图示两种情况,则下列分析判断不正确的是(不考虑CO2的溶解)( )| A、曲线A表明M中的溶质为NaOH、Na2CO3 |
| B、曲线B表明M中NaHCO3与Na2CO3的物质的量之比为1:2 |
| C、原NaOH溶液的物质的量浓度为0.75mol/L |
| D、由A.B可知,两次实验通入的CO2的体积比3:10 |
考点:化学方程式的有关计算
专题:图示题
分析:A.曲线A、B,开始没有气体,加入一定体积盐酸后生成气体,生成气体的反应为:HCO3-+H+=H2O+CO2↑,
若A中只有Na2CO3,开始发生CO32-+H+=HCO3-,前后两过程消耗HCl的体积相等,实际开始阶段消耗盐酸体积大于产生二氧化碳消耗的盐酸体积,故A曲线表明M中的溶质为NaOH、Na2CO3;
B.B曲线中,前后消耗盐酸的体积之比为1:2,则曲线B表明M中溶质为Na2CO3,
C.加入75mL盐酸时二氧化碳的体积达最大,此时溶液为氯化钠溶液,根据氯离子、钠离子守恒,计算出氢氧化钠的物质的量,再根据物质的量浓度的定义计算;
D.根据生成二氧化碳阶段消耗盐酸的体积,判断两次实验通入的CO2的体积之比.
若A中只有Na2CO3,开始发生CO32-+H+=HCO3-,前后两过程消耗HCl的体积相等,实际开始阶段消耗盐酸体积大于产生二氧化碳消耗的盐酸体积,故A曲线表明M中的溶质为NaOH、Na2CO3;
B.B曲线中,前后消耗盐酸的体积之比为1:2,则曲线B表明M中溶质为Na2CO3,
C.加入75mL盐酸时二氧化碳的体积达最大,此时溶液为氯化钠溶液,根据氯离子、钠离子守恒,计算出氢氧化钠的物质的量,再根据物质的量浓度的定义计算;
D.根据生成二氧化碳阶段消耗盐酸的体积,判断两次实验通入的CO2的体积之比.
解答:
解:A.曲线A、B,开始没有气体,加入一定体积盐酸后生成气体,生成气体的反应为:HCO3-+H+=H2O+CO2↑,若A中只有Na2CO3,开始发生CO32-+H+=HCO3-,前后两过程消耗HCl的体积相等,实际开始阶段消耗盐酸体积大于产生二氧化碳消耗的盐酸体积,故A曲线表明M中的溶质为NaOH、Na2CO3,故A正确;
B.B曲线中,前后消耗盐酸的体积之比为1:2,则曲线B表明M中溶质为Na2CO3,故B错误;
C.加入75mL盐酸时二氧化碳的体积达最大,此时溶液为NaCl溶液,根据Na元素守恒、氯离子守恒,则n(NaOH)=n(HCl)=0.075L×0.1mol/L=0.0075mol,则c(NaOH)=
=0.75mol/L,故C正确;
D.曲线A生成二氧化碳消耗盐酸体积为(75-60)mL=15mL,曲线B生成二氧化碳消耗盐酸体积为(75-25)mL=50mL,由HCO3-+H+=H2O+CO2↑可知,则两次实验通入的CO2的体积之比=15mL:50mL=3:10,故D正确,
故选B.
B.B曲线中,前后消耗盐酸的体积之比为1:2,则曲线B表明M中溶质为Na2CO3,故B错误;
C.加入75mL盐酸时二氧化碳的体积达最大,此时溶液为NaCl溶液,根据Na元素守恒、氯离子守恒,则n(NaOH)=n(HCl)=0.075L×0.1mol/L=0.0075mol,则c(NaOH)=
| 0.0075mol |
| 0.01L |
D.曲线A生成二氧化碳消耗盐酸体积为(75-60)mL=15mL,曲线B生成二氧化碳消耗盐酸体积为(75-25)mL=50mL,由HCO3-+H+=H2O+CO2↑可知,则两次实验通入的CO2的体积之比=15mL:50mL=3:10,故D正确,
故选B.
点评:本题考查混合物的计算,题目难度较大,本题关键是根据图象判断溶液溶质的成分,结合离子方程式计算.

练习册系列答案
相关题目
下列反应:①Na+H2O②Na2O+H2O③NO2+H2O ④Cl2+H2O⑤F2+H2O⑥SO2+H2O中,属于氧化还原反应,但水既不是氧化剂,又不是还原剂的是( )
| A、①③ | B、②⑥ | C、③④ | D、④⑤ |
抗生素是能抑制某些微生物生长的一类物质,最早发现的一种天然抗生素是( )
| A、青霉素 | B、阿司匹林 |
| C、红霉素 | D、吗啡 |
短周期元素X、Y、Z、W在周期表中的位置关系如图所示,则下列叙述中错误的是( )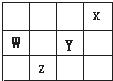

| A、四元素中,X的单质最稳定 |
| B、氢化物稳定性:HY>H2Z |
| C、原子半径:W>Y |
| D、W在周期表中的位置为:第2周期第5族 |
下列实验操作中,仪器需插入液面以下的有( )
①制取H2的简易装置中长颈漏斗的下端管口
②分馏石油时控制温度所用的温度计
③用水吸收NH3时的导气管
④制备Fe(OH)2时将NaOH溶液滴入FeSO4溶液中所用的胶头滴管
⑤用乙醇制备乙烯时所用的温度计
⑥向试管中的BaCl2溶液中滴加稀 H2SO4所用的胶头滴管.
①制取H2的简易装置中长颈漏斗的下端管口
②分馏石油时控制温度所用的温度计
③用水吸收NH3时的导气管
④制备Fe(OH)2时将NaOH溶液滴入FeSO4溶液中所用的胶头滴管
⑤用乙醇制备乙烯时所用的温度计
⑥向试管中的BaCl2溶液中滴加稀 H2SO4所用的胶头滴管.
| A、③⑤⑥ | B、②④ |
| C、①④⑤ | D、①②③④⑥ |
用NA表示阿伏伽德罗常数的值.下列叙述正确的是( )
| A、0.1mol/LAlCl3溶液中含有的Cl-数目为0.3NA |
| B、室温下,42.0g己烯和丙烯的混合气体中含有的碳原子数为3NA |
| C、标准状况下,2.24LCl2与足量的NaOH溶液反应,转移的电子数目为0.2NA |
| D、100mL18.4mol/L硫酸与足量铜反应,生成SO2的分子数为0.92NA |
合成氨所需的氢气可用煤和水作原料经多步反应制得,其中的一步反应为:CO(g)+H2O(g)
CO2(g)+H2(g)△H<0反应达到平衡后,为提高CO的转化率,下列措施中正确的是( )
| 催化剂 |
| A、增加压强 |
| B、升高温度 |
| C、增大H2O的浓度 |
| D、更换催化剂 |
乙醇分子所含官能团的名称是( )
| A、乙氧基 | B、羟基 | C、乙基 | D、甲基 |