题目内容
12.元素①~⑧在元素周期表中的位置如下:回答有关问题: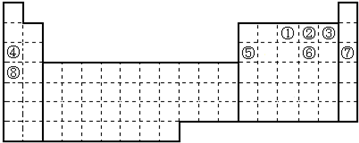
(1)画出⑥的离子结构示意图:
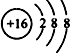 .
.(2)在①、②、④、⑤四种元素中,其离子半径按由大到小的排列顺序为r(N3-)>r(O2-)>r(Na+)>r(Al3+)(示例:用r(A2-)>r(B-)的形式表示).
(3)元素②、③氢化物的稳定性由强到弱的顺序为HF>H2O(填化学式).
(4)与③同一主族并且在短周期的元素的某种含氧酸可以消毒杀菌,写出该物质的电子式:
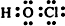 .
.
分析 由元素的位置可知,①~⑧分别为N、O、F、Na、Al、S、Ar、K,
(1)S的离子结构中有3个电子层,最外层电子数为8;
(2)具有相同电子排布的离子,原子序数大的离子半径小;
(3)非金属性越强,气态氢化物越稳定;
(4)与③同一主族并且在短周期的元素的某种含氧酸可以消毒杀菌,该物质为HClO.
解答 解:由元素的位置可知,①~⑧分别为N、O、F、Na、Al、S、Ar、K,
(1)S的离子结构中有3个电子层,最外层电子数为8,离子结构示意图为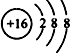 ,故答案为:
,故答案为: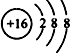 ;
;
(2)具有相同电子排布的离子,原子序数大的离子半径小,则离子半径为r(N3-)>r(O2-)>r(Na+)>r(Al3+),
故答案为:r(N3-)>r(O2-)>r(Na+)>r(Al3+);
(3)非金属性越强,气态氢化物越稳定,氢化物的稳定性由强到弱的顺序为HF>H2O,故答案为:HF>H2O;
(4)与③同一主族并且在短周期的元素的某种含氧酸可以消毒杀菌,该物质为HClO,其电子式为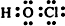 ,故答案为:
,故答案为: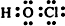 .
.
点评 本题考查位置、结构与性质,为高频考点,把握元素的位置推断元素等为解答的关键,侧重分析与应用能力的考查,注意元素周期律的应用,题目难度不大.

练习册系列答案
相关题目
2.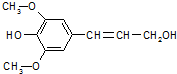 膳食纤维具有突出的保健功能,人体的“第七营养素”木质素是一种非糖类膳食纤维,其单体之一是芥子醇,结构简式如图所示.下列有关芥子醇的说法正确的是( )
膳食纤维具有突出的保健功能,人体的“第七营养素”木质素是一种非糖类膳食纤维,其单体之一是芥子醇,结构简式如图所示.下列有关芥子醇的说法正确的是( )
 膳食纤维具有突出的保健功能,人体的“第七营养素”木质素是一种非糖类膳食纤维,其单体之一是芥子醇,结构简式如图所示.下列有关芥子醇的说法正确的是( )
膳食纤维具有突出的保健功能,人体的“第七营养素”木质素是一种非糖类膳食纤维,其单体之一是芥子醇,结构简式如图所示.下列有关芥子醇的说法正确的是( )| A. | 不能与FeCl3溶液发生显色反应 | |
| B. | 分子中所有碳原子不可能在同一平面 | |
| C. | 分子式是C11H14O4,属于芳香族化合物 | |
| D. | 能发生氧化、取代、水解等反应 |
20.下列有关Na2CO3和NaHCO3的叙述错误的是( )
| A. | 水溶液都显碱性 | |
| B. | Na2CO3比NaHCO3稳定 | |
| C. | NaHCO3比Na2CO3更易溶于水 | |
| D. | 与足量盐酸反应得到等量的CO2时,消耗NaHCO3的质量比Na2CO3的质量要少 |
7.茅台酒中存在少量具有凤梨香味的物质X,其结构如图.下列说法正确的是( )


| A. | X分子式是C5H10O2 | |
| B. | X难溶于乙醇 | |
| C. | 分子式为 C4H8O2且官能团与X相同的物质有4种 | |
| D. | X完全燃烧后生成CO2和H2O的物质的量比为1:2 |
17.下列叙述正确的是( )
| A. | 500mL 0.5mol•L-1 K2SO4溶液中,K+的总数为NA | |
| B. | 2L 0.5mol•L-1 K2SO4溶液中阴离子所带电荷数为NA | |
| C. | 18g H2O中含有10NA个质子 | |
| D. | 2L水中溶有80g的氢氧化钠,溶液的物质的量浓度为2mol•L-1 |
4.将铜制印刷电路板置于过量的FeCl3溶液中,下列有关该过程的描述正确的是( )
| A. | 溶液中只含Cu2+、Fe2+、Fe3+ | B. | 溶液呈蓝色 | ||
| C. | 无固体析出 | D. | 发生了置换反应 |
10.L-多巴是一种有机物,它可用于帕金森综合症的治疗,其结构简式如图:

这种药物的研制是基于获得2000年诺贝尔生理学或医学奖和获得2001年诺贝尔化学奖的研究成果.下列关于L-多巴的叙述不正确的是( )

这种药物的研制是基于获得2000年诺贝尔生理学或医学奖和获得2001年诺贝尔化学奖的研究成果.下列关于L-多巴的叙述不正确的是( )
| A. | 该有机物可看作氨基酸,也可看作是酚类物质 | |
| B. | 能与盐酸发生反应 | |
| C. | 能发生取代反应,中和反应,缩聚反应 | |
| D. | 既能与溴水发生取代反应,又能与溴水发生加成反应 |