题目内容
3.在室温下,向100mL Cu (IO3)2饱和溶液中加入足量的经酸化的KI溶液,发生如下的反应:5I-+IO3-+6H+=3I2+3H2O,2Cu2++4I-=I2+2CuI,反应后,用0.11mol/L Na2S2O3溶液滴定(I2+2S2O32-=2I-+S4O62-),消耗了35.3mL Na2S2O3溶液.计算原饱和溶液中Cu (IO3)2的物质的量浓度.分析 设100 mL Cu (IO3)2饱和溶液中含Cu (IO3)2的物质的量为n
Cu (IO3)2=Cu2++2 IO3-
n n 2 n
5I-+IO3-+6H+=3I2+3H2O 2Cu2++4 I-=I2+2CuI
2 n 6 n n 0.5 n
I2 +2 S2O32-=2 I-+S4O62-
(6 n+0.5 n ) 0.0353 L×0.11 mol/L
2×(6 n+0.5 n )=0.0353 L×0.11 mol/L
解得n,然后根据c=$\frac{n}{V}$进行计算.
解答 解:设100 mL Cu (IO3)2饱和溶液中含Cu (IO3)2的物质的量为n
Cu (IO3)2=Cu2++2 IO3-
n n 2 n
5I-+IO3-+6H+=3I2+3H2O 2Cu2++4 I-=I2+2CuI
2 n 6 n n 0.5 n
I2 +2 S2O32-=2 I-+S4O62-
(6 n+0.5 n ) 0.0353 L×0.11 mol/L
2×(6 n+0.5 n)=0.0353 L×0.11 mol/L
∴n=0.0003 mol
∴c Cu (IO3)2=0.0003mol/0.1L=0.003mol/L,
答:原饱和溶液中Cu (IO3)2的物质的量浓度0.003 mol/L.
点评 本题考查能利用多个方程式的计算,找出关系式解题是的关键,然后根据公式进行计算,比较容易.

| A. | 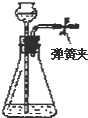 长颈漏斗内液面高度保持不变 | |
| B. | 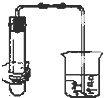 双手移去后.导管中水面与烧杯水面相平 | |
| C. | 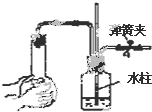 长导管内形成一段水柱 | |
| D. | 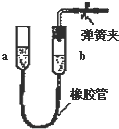 上移a管后,a、b两端液面形成了一段稳定的高度差 |
| A. | K 37ClO3与浓盐酸(HCl)在加热下生成氯气的化学方程式:K 37ClO3+6HCl═K 37Cl+3Cl2↑+3H2O | |
| B. | 表示氢气燃烧热的热化学方程式:H2 (g)+$\frac{1}{2}$O2(g)=H2O(g);△H=-241.8 kJ/mol | |
| C. | 将1~2 mL氯化铁饱和溶液逐滴加到20 mL 沸水中所发生反应的离子方程式:Fe3++3H2O$\frac{\underline{\;\;△\;\;}}{\;}$Fe (OH)3(胶体)+3H+ | |
| D. | 在氢氧化钡溶液中滴入硫酸氢钠溶液至中性:Ba2++OH-+H++SO42-=BaSO4↓+H2O |
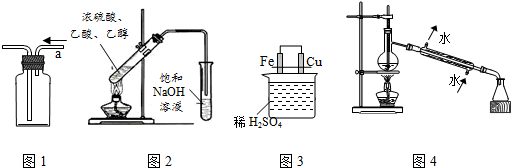
| A. | 用图1所示装置从a口进气可收集CH2=CH2 | |
| B. | 用图2所示装置制取并收集乙酸乙酯 | |
| C. | 用图3所示装置比较Fe、Cu的金属活动性 | |
| D. | 用图4所示装置进行石油的蒸馏实验 |
| A. | 1molCl2和足量的铁加热条件下反应,转移电子数一定为3NA | |
| B. | 常温常压下,8.8g CO2和N2O的混合气体所含电子数为4.4 NA | |
| C. | 常温下,PH=13的Ba(OH)2 溶液,0.1L,含OH-,0.02NA | |
| D. | 1 L 1 mol/L的乙醇水溶液中含有氢原子总数为6NA |
| A. | 2F2+H2O═4HF+O2 | B. | Si+2NaOH+H2O═Na2SiO3+2H2↑ | ||
| C. | 3NO2+H2O═2HNO3+NO | D. | P2O5+3H2O═2H3PO4 |
 .
. .
.