题目内容
11.关于如图所示化合物的说法正确的是( )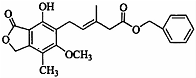
| A. | 分子中所有的原子共平面 | |
| B. | 既可以与FeCl3溶液发生显色反应.又可以与NaHCO3溶液反应放出CO2气体 | |
| C. | 1 mol该化合物最多可以与9mol H2发生加成反应 | |
| D. | 该物质能发生取代反应、氧化反应、加成反应 |
分析 A.分子中含有甲基、亚甲基,具有甲烷结构特点;
B.酚能和氯化铁发生显色反应,羧基能和碳酸氢钠反应;
C.碳碳双键和苯环能和氢气在一定条件下发生加成反应;
D.该物质中含有酯基、醚键、酚羟基和苯环,具有酯、醚、酚和苯的性质.
解答 解:A.分子中含有甲基、亚甲基,具有甲烷结构特点,所以所有原子不可能共平面,故A错误;
B.酚能和氯化铁发生显色反应,羧基能和碳酸氢钠反应,该物质中不含羧基,所以不能与碳酸氢钠反应,故B错误;
C.碳碳双键和苯环能和氢气在一定条件下发生加成反应,所以1 mol该化合物最多可以与7mol H2发生加成反应,故C错误;
D.该物质中含有酯基、醚键、酚羟基和苯环,具有酯、醚、酚和苯的性质,能发生取代反应、氧化反应、加成反应,故D正确;
故选D.
点评 本题考查有机物结构和性质,为高频考点,明确官能团及其性质关系是解本题关键,侧重考查酚、酯和苯的性质,注意碳酸氢钠和羧基反应但和酚羟基不反应,易错选项是B.

练习册系列答案
相关题目
1.在无色溶液中,下列离子能大量共存的是( )
| A. | Na+、NH4+、NO3-、MnO4- | B. | Na+、NO3?、SO42?、I? | ||
| C. | K +、Fe3+、Cl-、Br- | D. | Ba2+、Na+、OH-、CO32- |
19.下列说法正确的是( )
| A. | 0.1 mol•L-1 Na2CO3溶液中:c(HCO3-)=2c(H2CO3)+c(H+)-c(OH-) | |
| B. | 物质的量浓度相等的Na2SO3和NaHSO3溶液中:3c(Na+)=2[c(HSO3-)+c(H2SO3)+c(SO32-)] | |
| C. | 同浓度的下列溶液中,①NH4HSO4 ②NH4Cl ③NH3•H2O,c(NH4+)由大到小的顺序是:②>①>③ | |
| D. | 常温下,浓度均为0.1mol/L NaA和HA溶液中pH=8:c(HA)>c(Na+)>c(A-)>c(OH-)>c(H+) |
6.下列实验操作或处理事故的方法正确的是( )
| A. | 用干燥的pH试纸测定NaClO溶液的pH | |
| B. | 在耐高温的石英坩埚中进行熔化氢氧化钠固体的实验 | |
| C. | 用分液漏斗分离溴苯和水的混合物时,溴苯从下口放出,水从上口倒出 | |
| D. | 欲配制质量分数为10%的硫酸铜溶液,可准确称取10 g硫酸铜晶体溶于90 g水中 |
16.下列分子或离子在指定的分散系中一定能大量共存的一组是( )
| A. | 常温下水电离出的c(H+)•c(OH-)=1×10-20的溶液:Na+、Cl-、S2-、SO32- | |
| B. | 空气:C2H2、CO2、SO2、NO | |
| C. | 含Al3+的无色溶液:Na+、SO42-、K+、ClO-、HCO3- | |
| D. | 高锰酸钾溶液:H+、Na+、SO42-、NO3- |
3.常温下,向20 mL 0.10 mol•L-1 NaHCO3溶液中滴加0.10 mol•L-1 CaCl2溶液至pH=7,有白色沉淀生成,无气体放出.对反应所得混合液的下列说法错误的是( )
| A. | 存在电离平衡、水解平衡和沉淀溶解平衡 | |
| B. | c(Na+)=c(Cl-)>c(HCO3-)>c(CO32-)=c(Ca2+) | |
| C. | c(Na+)+2c(Ca2+)=c(HCO3-)+2c(CO32-)+c(Cl-) | |
| D. | 反应的离子方程式:2HCO3-+Ca2+═CaCO3↓+H2CO3 |
20.下列说法中正确的是( )
| A. | 10mL 0.5mol/L CH3COONa溶液与6mL 1mol/L盐酸混合:c(Cl-)>c(Na+)>c(CH3COO-)>c(H+)>c(OH-) | |
| B. | 等浓度的下列稀溶液:①硫酸氢钠 ②乙酸钠 ③醋酸 ④碳酸氢钠 ⑤硝酸钠 ⑥苯酚钠,它们的pH由小到大排列为:③⑤①④②⑥ | |
| C. | 常温下0.1 mol/L的下列溶液 ①NH4Al(SO4)2 ②NH4Cl ③NH3•H2O ④CH3COONH4中c (NH4+)由大到小的顺序是:②>①>④>③ | |
| D. | 在25℃时,将a mol•L-1的氨水与0.01 mol•L-1的盐酸等体积混合反应时溶液中c(NH4+)=c(Cl-).用含a的代数式表示NH3•H2O的电离常数Kb=$\frac{1{0}^{-9}}{a-0.01}$ |
1.下列离子方程式正确的是( )
| A. | 浓烧碱溶液中加入铝片:Al+4OH-=AlO2-+2H2O | |
| B. | 将磁性氧化铁溶于盐酸:Fe3O4+8H+=3Fe3++4H2O | |
| C. | 用铁电极电解氯化铁溶液:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$2OH-+H2↑+Cl2↑ | |
| D. | 等体积、等浓度的Ba(OH)2稀溶解与NH4HCO3稀溶液混合Ba2++2OH-+NH4++HCO3-=BaCO3↓+NH3•H2O+H2O |