题目内容
弱电解质区别于强电解质的理论根据是( )
| A、溶液的导电性差 |
| B、在溶液中离子与离子间存在电离平衡 |
| C、溶解度小 |
| D、在溶液中存在分子和离子之间的电离平衡 |
考点:弱电解质在水溶液中的电离平衡
专题:电离平衡与溶液的pH专题
分析:强电解质是指:在水溶液中或熔融状态下,能够完全电离的化合物.即溶于水的部分或者熔融状态时,可以完全变成阴阳离子的化合物.一般是强酸、强碱和大部分盐类.弱电解质是指:在水溶液里部分电离的电解质,包括弱酸、弱碱、水与少数盐.以此解答该题.
解答:
解:A.电解质的强弱与电离程度有关,与溶液的导电能力无关,溶液的导电性强弱取决于溶液中离子浓度的大小,离子浓度越大,导电性越强,如硫酸钡是强电解质,但它难溶于水,虽溶于水的部分能完全电离,可导电能力很弱,故A错误;
B.如电离出简单离子,无论是强电解质还是弱电解质,在溶液中离子与离子间都不存在离子平衡,不能用于证明,故B错误;
C.强弱电解质与溶解度无关,如硫酸钡是强电解质,但它难溶于水,乙酸易溶于水,但它是弱酸,是弱电解质,故C错误;
D.强电解质完全电离,不存在分子和离子之间的电离平衡,而弱电解质部分电离,则在溶液中存在分子和离子之间的电离平衡,故D正确.
故选D.
B.如电离出简单离子,无论是强电解质还是弱电解质,在溶液中离子与离子间都不存在离子平衡,不能用于证明,故B错误;
C.强弱电解质与溶解度无关,如硫酸钡是强电解质,但它难溶于水,乙酸易溶于水,但它是弱酸,是弱电解质,故C错误;
D.强电解质完全电离,不存在分子和离子之间的电离平衡,而弱电解质部分电离,则在溶液中存在分子和离子之间的电离平衡,故D正确.
故选D.
点评:本题考查了强弱电解质的判断,为高频考点,注意强弱电解质与导电能力、溶解度之间的关系,难度不大,抓住强电解质的定义中的关键词“完全电离”是解题的关键.

练习册系列答案
 导学与测试系列答案
导学与测试系列答案 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案
相关题目
 如图是元素周期表短周期的一部分,A、C两种元素的核外电子数之和等于B的核外电子数.下列叙述正确的是( )
如图是元素周期表短周期的一部分,A、C两种元素的核外电子数之和等于B的核外电子数.下列叙述正确的是( )| A、A元素位于第二周期、ⅥA族 |
| B、原子半径C>B>A |
| C、在一定条件下,A、B的气态氢化物都能够与氧气反应 |
| D、三种元素都存在最高价含氧酸,且都显强酸性 |
合理使用药物有利身心健康.下列说法正确的是( )
| A、因碘酒使蛋白质变性,故常用于外用消毒 |
| B、麻黄碱可用于止咳平喘,就是因为它能起到消炎作用 |
| C、长期大量使用阿司匹林有不良反应,应立即停药并静脉注射Na2CO3溶液 |
| D、能用于治疗胃酸过多的抗酸药有盘尼西林 |
一定量的锎(
Cf)是有用的中子源,在医学上常用作治疗恶性肿瘤的中子源.下列有关锎的说法错误的是( )
252 98 |
A、
| ||
B、
| ||
C、
| ||
| D、锎元素位于第6周期 |
化学是一门以实验为基础的学科,掌握基本实验方法和操作技能是做好化学实验的基础.下列有关化学实验基本知识的描述不正确的是( )
| A、丁达尔现象可用于区别FeCl3饱和溶液和Fe(OH)3胶体 |
| B、过滤和蒸发操作中均用到玻璃棒,但玻璃棒的作用不相同 |
| C、汽油和水的混合物可用分液的方法分离 |
| D、检验某溶液中是否含有SO42-的方法是先向该溶液中加入BaCl2溶液,再加入稀HNO3 |
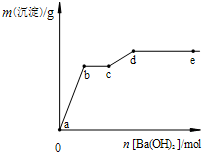 在含有4mol HCl和1mol MgSO4的混合溶液中逐滴加入Ba(OH)2溶液,产生的沉淀质量m与加入Ba(OH)2物质的量n之间的关系如图,下列说法正确的是( )
在含有4mol HCl和1mol MgSO4的混合溶液中逐滴加入Ba(OH)2溶液,产生的沉淀质量m与加入Ba(OH)2物质的量n之间的关系如图,下列说法正确的是( )| A、a→b时的沉淀的成分为BaSO4与Mg(OH)2 |
| B、b→c时发生的离子反应为:H++OH-→H2O |
| C、c→d时离子的物质的量:Ba2+可能大于Cl- |
| D、d→e时离子的物质的量:Ba2+一定大于OH- |
下列说法正确的是( )
| A、电子层数越多,原子半径一定越大 | ||||
B、已知2C+SiO2
| ||||
| C、第ⅥA族元素的氢化物中,稳定性最强的其沸点最低 | ||||
| D、按照元素周期表的排布规律,非金属元素最多为23种 |
