题目内容
化学是一门以实验为基础的学科,掌握基本实验方法和操作技能是做好化学实验的基础.下列有关化学实验基本知识的描述不正确的是( )
| A、丁达尔现象可用于区别FeCl3饱和溶液和Fe(OH)3胶体 |
| B、过滤和蒸发操作中均用到玻璃棒,但玻璃棒的作用不相同 |
| C、汽油和水的混合物可用分液的方法分离 |
| D、检验某溶液中是否含有SO42-的方法是先向该溶液中加入BaCl2溶液,再加入稀HNO3 |
考点:物质的检验和鉴别的基本方法选择及应用,物质的分离、提纯和除杂,化学实验方案的评价
专题:物质检验鉴别题,化学实验基本操作
分析:A.丁达尔现象为胶体特有的性质;
B.过滤中玻璃棒引流,蒸发中玻璃棒搅拌;
C.汽油和水的混合物分层;
D.应先加盐酸酸化,排除银离子、碳酸根离子等的干扰.
B.过滤中玻璃棒引流,蒸发中玻璃棒搅拌;
C.汽油和水的混合物分层;
D.应先加盐酸酸化,排除银离子、碳酸根离子等的干扰.
解答:
解:A.Fe(OH)3胶体具有丁达尔现象,而溶液不具有,则丁达尔现象可用于区别FeCl3饱和溶液和Fe(OH)3胶体,故A正确;
B.过滤中玻璃棒引流,蒸发中玻璃棒搅拌,则均使用了玻璃棒,但作用不同,故B正确;
C.汽油和水的混合物分层,然后分液可分离,故C正确;
D.应先加盐酸酸化,排除银离子、碳酸根离子等的干扰,则验某溶液中是否含有SO42-的方法是先向该溶液中加入稀盐酸,再加入BaCl2溶液,故D错误;
故选D.
B.过滤中玻璃棒引流,蒸发中玻璃棒搅拌,则均使用了玻璃棒,但作用不同,故B正确;
C.汽油和水的混合物分层,然后分液可分离,故C正确;
D.应先加盐酸酸化,排除银离子、碳酸根离子等的干扰,则验某溶液中是否含有SO42-的方法是先向该溶液中加入稀盐酸,再加入BaCl2溶液,故D错误;
故选D.
点评:本题考查化学实验方案的评价,为高频考点,涉及物质的鉴别、混合物分离提纯、实验基本操作及离子检验等,把握物质的性质及实验原理为解答的关键,注意实验操作的可行性、实验方案的可行性分析,题目难度不大.

练习册系列答案
相关题目
下列措施中,不能加快化学反应速率的是( )
| A、将食物储存在冰箱里 |
| B、往H2O2溶液中加入几滴FeCl3溶液 |
| C、用粉末状碳酸钙代替块状碳酸钙与稀盐酸反应 |
| D、用稀H2SO4溶液与锌粒反应时加入几滴CuSO4溶液 |
弱电解质区别于强电解质的理论根据是( )
| A、溶液的导电性差 |
| B、在溶液中离子与离子间存在电离平衡 |
| C、溶解度小 |
| D、在溶液中存在分子和离子之间的电离平衡 |
在氨水中存在下列电离平衡:NH3?H2O?NH4++OH-,下列情况能引起电离平衡向正向移动的有( )
①加NH4Cl固体 ②加NaOH溶液 ③加HCl ④加CH3COOH溶液 ⑤加水 ⑥加压.
①加NH4Cl固体 ②加NaOH溶液 ③加HCl ④加CH3COOH溶液 ⑤加水 ⑥加压.
| A、①③⑤ | B、①④⑥ |
| C、③④⑤ | D、①②④ |
NA代表阿伏加德常数,下列说法中,正确的是( )
| A、在同温同压时,相同体积的任何气体单质所含的原子数目相同 |
| B、2 g氢气所含原子数目为NA |
| C、在常温常压下,11.2 L氮气所含的原子数目为NA |
| D、17 g氨气所含电子数目为10 NA |
地壳中化学元素含量前四为排序正确的是( )
| A、氧、硅、铁、铝 |
| B、铁、氧、铝、镁 |
| C、氧、硅、铝、铁 |
| D、硅、氧、铝、铁 |
滴有酚酞和氯化钠试液的湿润滤纸分别做甲乙两个实验,能发现附近变成红色的电极是( )


| A、a、c | B、b、d |
| C、a、d | D、b、c |
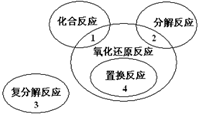 氧化还原反应与四种基本类型反应的关系如图所示,则下列化学反应属于1区的是( )
氧化还原反应与四种基本类型反应的关系如图所示,则下列化学反应属于1区的是( )| A、Cl2+2KBr═Br2+2KCl |
| B、2NaHCO3═Na2CO3+H2O+CO2 |
| C、4Fe(OH)2+O2+2H2O═4Fe(OH)3 |
| D、2Na2O2+2CO2═2Na2CO3+O2 |