题目内容
19.下列分子中所有原子都满足最外层为8电子结构的是( )| A. | PCl5 | B. | BF3 | C. | CCl4 | D. | NH3 |
分析 对于ABn型共价化合物元素化合价绝对值+元素原子的最外层电子层=8,则该元素原子满足8电子结构,据此判断.
解答 解:A、PCl5中P元素化合价为+5,P原子最外层电子数为5,所以5+5=10,P原子不满足8电子结构;Cl元素化合价为-1,Cl原子最外层电子数为7,所以1+7=8,Cl原子满足8电子结构,故A错误;
B、BF3中B元素化合价为+3,B原子最外层电子数为3,所以3+3=6,B原子不满足8电子结构;F元素化合价为-1,F原子最外层电子数为7,所以1+7=8,F原子满足8电子结构,故B错误;
C、CCl4中C元素化合价为+4,C原子最外层电子数为4,所以4+4=8,C原子满足8电子结构;Cl元素化合价为-1,Cl原子最外层电子数为7,所以1+7=8,Cl原子满足8电子结构,故C正确;
D、NH3中N元素化合价为-3,N原子最外层电子数为5,所以3+5=8,O原子满足8电子结构;H元素化合价为+1,H原子最外层电子数为1,所以1+1=2,H原子不满足8电子结构,故D错误;
故选C.
点评 本题考查8电子结构的判断,难度不大,清楚元素化合价绝对值+元素原子的最外层电子层=8,则该元素原子满足8电子结构是关键,注意离子化合物不适合.

练习册系列答案
 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案
相关题目
15.如表是元素周期表的一部分,针对表中的①~⑧种元素,填写下列空白:
(用元素符号或化学式作答)
(1)在这些元素中,化学性质最不活泼的是Ar;
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是HClO4,
(3)形成化合物种类最多的元素是C;
(4)它们的氢化物分子间存在氢键的氢化物分子式是NH3、H2O
(5)在这些元素中,最活泼的金属在空气中加热反应的产物溶于水时反应的离子方程式为:2Na2O2+2H2O═4Na++4OH-+O2↑.
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
(1)在这些元素中,化学性质最不活泼的是Ar;
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是HClO4,
(3)形成化合物种类最多的元素是C;
(4)它们的氢化物分子间存在氢键的氢化物分子式是NH3、H2O
(5)在这些元素中,最活泼的金属在空气中加热反应的产物溶于水时反应的离子方程式为:2Na2O2+2H2O═4Na++4OH-+O2↑.
14.物质的结构决定物质的性质.请回答下列涉及物质结构和性质的问题: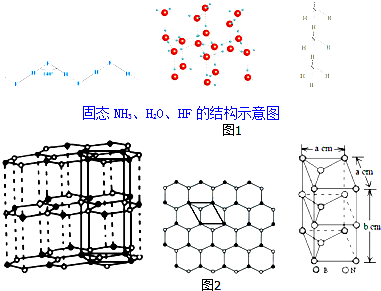
(1)基态Cu2+的电子排布式为1s22s22p63s23p63d9,其最外电子层的电子数为17.
(2)利用价层电子对互斥理论(VSEPR theory)预测多原子分子或离子立体构型时,认为价层电子间互斥力(F)的大小决定了夹角(∠)的大小:F(孤电子对间)>F(孤电子对-双键电子)>F(双键电子-单键电子)>F(单键电子间),则a.∠(孤-孤夹角)、b.∠(孤-双夹角)、c.∠(双-单夹角)、d.∠(单-单夹角)由大到小的排序为abcd(填编号);XeF4中Xe价层电子数为6对,画出其VSEPR模型(含中心原子的孤电子对)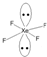 .
.
(3)在图1中,除NH3、H2O、HF外的同主族氢化物的沸点随周期数增大而升高的原因是同为分子晶体,物质的组成与结构相似,相对分子质量越大,分子间作用力越大;
已知固态NH3、H2O、HF的氢键键能和结构如表:
根据如表固态NH3、H2O、HF的结构示意图解释H2O、HF、NH3沸点依次降低的原因:单个氢键的键能是(HF)n>冰>(NH3)n,而平均每个分子含氢键数:冰中2个,(HF)n和(NH3)n只有1个,气化要克服的氢键的总键能是冰>(HF)n>(NH3)n.
(4)石墨型BN呈白色,亦称“白石墨”,“白石墨”在一定条件下可转化为金刚石型BN.“白石墨”的结构示意图和晶胞如图2(中图是晶胞底面从“白石墨”中的截取情况),则“白石墨”的密度为$\frac{100}{\sqrt{3}{N}_{A}{a}^{2}b}$g•cm-3(以含a、b的代数式表示).

(1)基态Cu2+的电子排布式为1s22s22p63s23p63d9,其最外电子层的电子数为17.
(2)利用价层电子对互斥理论(VSEPR theory)预测多原子分子或离子立体构型时,认为价层电子间互斥力(F)的大小决定了夹角(∠)的大小:F(孤电子对间)>F(孤电子对-双键电子)>F(双键电子-单键电子)>F(单键电子间),则a.∠(孤-孤夹角)、b.∠(孤-双夹角)、c.∠(双-单夹角)、d.∠(单-单夹角)由大到小的排序为abcd(填编号);XeF4中Xe价层电子数为6对,画出其VSEPR模型(含中心原子的孤电子对)
 .
.(3)在图1中,除NH3、H2O、HF外的同主族氢化物的沸点随周期数增大而升高的原因是同为分子晶体,物质的组成与结构相似,相对分子质量越大,分子间作用力越大;
已知固态NH3、H2O、HF的氢键键能和结构如表:
| 物质 | 氢键X-H…Y | 键能/kJ•mol-1 |
| (HF)n | F-H…F | 28.1 |
| 冰 | O-H…O | 18.8 |
| (NH3)n | N-H…N | 5.4 |
(4)石墨型BN呈白色,亦称“白石墨”,“白石墨”在一定条件下可转化为金刚石型BN.“白石墨”的结构示意图和晶胞如图2(中图是晶胞底面从“白石墨”中的截取情况),则“白石墨”的密度为$\frac{100}{\sqrt{3}{N}_{A}{a}^{2}b}$g•cm-3(以含a、b的代数式表示).
11.1g H2的热值为142.9KJ热量,下列反应的热化学方程式正确的是( )
| A. | H2+O2═2H2O△H=-571.6KJ/mol | |
| B. | H2 (g)+$\frac{1}{2}$O2(g)═H2O (l)△H=-142.9KJ/mol | |
| C. | H2 (g)+$\frac{1}{2}$O2(g)═H2O (l)△H=-285.8KJ/mol | |
| D. | 2H2(g)+O2(g)═2H2O (g)△H=-571.6KJ/mol |
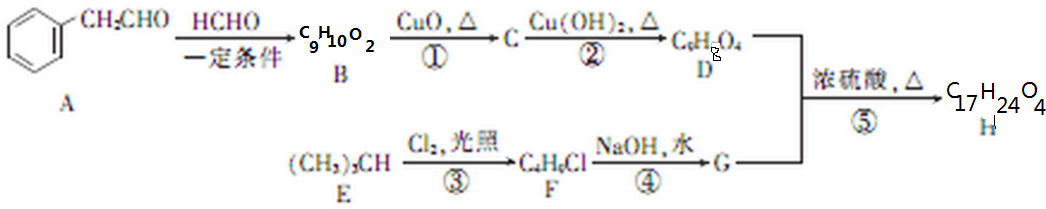
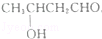
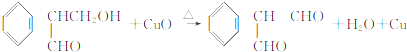
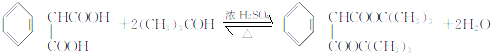
 (不考虑立体异构)?
(不考虑立体异构)?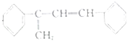 的合成路线.
的合成路线.