题目内容
4.下列电离方程式中,书写正确的是( )| A. | Cu(OH)2=Cu2++2 OH- | B. | NH3•H2O?NH4++OH- | ||
| C. | HF=H++F- | D. | H3PO43?3H++PO43- |
分析 A.氢氧化铜为弱电解质,部分电离用可逆号;
B.一水合氨为弱电解质,部分电离;
C.氢氟酸为弱酸,部分电离,用可逆号;
D.磷酸为多元弱酸,分步电离,以第一步为主.
解答 解:A.氢氧化铜为弱电解质,部分电离用可逆号,电离方程式:Cu(OH)2 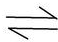 Cu2++2 OH-,故A错误;
Cu2++2 OH-,故A错误;
B.一水合氨为弱电解质,部分电离,电离方程式:NH3•H2O  NH4++OH-,故B正确;
NH4++OH-,故B正确;
C.氢氟酸为弱酸,部分电离,电离方程式:HF  H++F-,故C错误;
H++F-,故C错误;
D.磷酸为多元弱酸,分步电离,以第一步为主,电离方程式:H3PO4  H++H2PO4-,故D错误;
H++H2PO4-,故D错误;
故选:B.
点评 本题考查了电解质的电离方程式的书写,明确电解质强弱是解题关键,注意弱电解质部分电离,用可逆符号.

练习册系列答案
相关题目
12.在2L 0.5mol/L 的Na2SO4溶液中,含有Na+( )
| A. | 0.5mol | B. | 1mol | C. | 2mol | D. | 23g |
19.下列条件下,两瓶气体所含的原子数一定相等的是( )
①同质量不同密度的CO和N2
②同温同体积的H2和Cl2
③同体积同密度的O2和O3
④同压同体积的N2O和CO2.
①同质量不同密度的CO和N2
②同温同体积的H2和Cl2
③同体积同密度的O2和O3
④同压同体积的N2O和CO2.
| A. | ①③ | B. | ①② | C. | ②④ | D. | ③④ |
9.下图是吸热反应的是( )
| A. |  | B. |  | C. |  | D. |  |
16.下列有关盐类水解的叙述中正确的是( )
| A. | 溶液呈中性的盐一定是强酸、强碱生成的盐 | |
| B. | 含有弱酸根盐的水溶液一定呈碱性 | |
| C. | 盐溶液的酸碱性主要决定于形成盐的酸和碱的相对强弱 | |
| D. | 强酸强碱盐的水溶液一定呈中性 |
13.NA为阿伏加德罗常数的值,下列物质所含粒子数为0.2NA的是( )
| A. | 标准状况下,2.24 LCl2中含有的共价键数 | |
| B. | 100g质量分数为16.2%HBr溶液中的氢原子数 | |
| C. | 3.9g Na202晶体中所含的离子总数 | |
| D. | 0.1mol H2S和0.1 mol SO2混合后,体系中的硫原子数 |
14.精炼铜的过程中,电解质溶液中的[Fe2+]、[Zn2+]会逐渐增大而影响进一步电解. 甲同学设计下图除杂方案:
已知:
请回答下列问题:
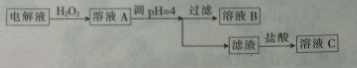
(1)加入H2O2目的是将Fe2+氧化为Fe3+.
(2)乙同学认为应将方案中的pH调节至8,你认为此观点不正确(填“正确”或“不正确”)理由是同时会使Cu2+生成沉淀而除去.
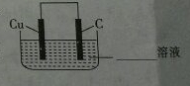
(3)利用铜棒、石墨棒和溶液C(填“B”或“C”)可设计一个原电池.该原电池的正极反应式为Fe3++e-=Fe2+.请在下图中完成该原电池的设计(标出电解质溶液和电子流动方向).
已知:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 | Zn(OH)2 |
| 开始沉淀时的pH | 2.3 | 7.5 | 5.6 | 6.2 |
| 完全沉淀时的pH | 3.9 | 9.7 | 6.4 | 8.0 |

(1)加入H2O2目的是将Fe2+氧化为Fe3+.
(2)乙同学认为应将方案中的pH调节至8,你认为此观点不正确(填“正确”或“不正确”)理由是同时会使Cu2+生成沉淀而除去.
(3)利用铜棒、石墨棒和溶液C(填“B”或“C”)可设计一个原电池.该原电池的正极反应式为Fe3++e-=Fe2+.请在下图中完成该原电池的设计(标出电解质溶液和电子流动方向).
