题目内容
15.如图为氢氧燃料电池原理示意图,按照此图的提示,回答下列问题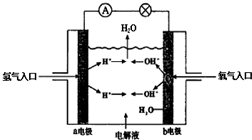
(1)a电极为负极,b电极为正极
(2)写出该电池的电极反应:负极:酸性环境下:2H2-4e-=4H+;碱性环境:2H2-4e-+4OH=4H2O正极:碱性环境下:O2+2H2O+4e-=4OH-,酸性环境下:O2+4H++4e-=2H2O.
分析 氢氧燃料电池中,氢气易失电子发生氧化反应,所以通入氢气的电极是负极,负极上氢气失电子发生氧化反应,则负极的电极反应式为:H2-2e-═2H2;
氧气易得电子发生还原反应,所以通入氧气的电极是正极,正极上氧气得电子发生还原反应,则正极的电极反应式为:O2+4e-+2H2O═4OH-.
解答 解:(1)燃料电池中,通入燃料氢气的电极a是负极,所以a电极是负极,b是正极,故答案为:负;正;
(2)a电极为负极,负极上氢气失电子发生氧化反应,酸性环境下,则负极的电极反应式为:2H2-4e-=4H+;b电极为正极,正极上氧气得电子发生还原反应,则正极的电极反应式为:O2+4H++4e-=2H2O,碱性环境下,负极上:2H2-4e-+4OH=4H2O;正极上:O2+2H2O+4e-=4OH-,
故答案为:酸性环境下:2H2-4e-=4H+;碱性环境:2H2-4e-+4OH=4H2O;正极上:碱性环境下:O2+2H2O+4e-=4OH-,酸性环境下:O2+4H++4e-=2H2O.
点评 本题考查了燃料电池,正负极的判断以及电极反应的书写,难度不大.

练习册系列答案
相关题目
3.下列说法错误的是( )
| A. | O3与SO2的结构相似 | B. | 硫粉不溶于水,易溶于CS2中 | ||
| C. | Be(OH)2是两性氢氧化物 | D. | 在相同条件下,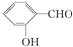 的沸点高于 的沸点高于 |
10.下列说法正确的是( )
| A. | Na、Al、Fe金属单质在一定条件下与水反应都生成H2和对应的碱 | |
| B. | H2O2、Na202、SO2都具有漂白性且漂白原理相同 | |
| C. | 饱和Na2C03溶液中通入CO2溶液会变浑浊 | |
| D. | 可用石灰水吸收尾气中的S02气体 |
20.雷雨天闪电时空气中有臭氧生成,下列说法正确的是( )
| A. | 16O2和18O3互为同位素 | |
| B. | O2和O3的相互转化是物理变化 | |
| C. | 等物质的量的O2和O3含有相同的质子数 | |
| D. | 等质量的O2和O3含有相同的O原子数 |
7.图是元素周期表的一部分,表中的①~⑩中元素,用元素符号或化学式填空回答:
(1)在这些元素中,化学性质最不活泼的原子的原子结构示意图为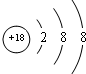
(2)地壳中含量最多的金属元素的名称是铝
(3)用电子式表示②与④形成化合物的过程 .
.
(4)这些元素中的最高价氧化物对应的水化物中,酸性最强的是HClO4(用化学式作答,下同),碱性最强的是KOH.
(5)写出⑤与氢氧化钠反应的化学方程式:2Al+2NaOH+2H2O=2NaAlO2+3H2↑.写出⑤的氢氧化物与氢氧化钠溶液反应的离子方程式:Al (OH)3+OH-=AlO2-+2H2O.
(6)②和⑥,②和⑨形成的化合物含有的化学键类型分别是共价键,离子键.
| 族 周 期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ||||||
| 三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 四 | ⑨ | ⑩ |

(2)地壳中含量最多的金属元素的名称是铝
(3)用电子式表示②与④形成化合物的过程
 .
.(4)这些元素中的最高价氧化物对应的水化物中,酸性最强的是HClO4(用化学式作答,下同),碱性最强的是KOH.
(5)写出⑤与氢氧化钠反应的化学方程式:2Al+2NaOH+2H2O=2NaAlO2+3H2↑.写出⑤的氢氧化物与氢氧化钠溶液反应的离子方程式:Al (OH)3+OH-=AlO2-+2H2O.
(6)②和⑥,②和⑨形成的化合物含有的化学键类型分别是共价键,离子键.
5.下列有关“化学与生活”的叙述不正确的是( )
| A. | 漂白粉漂白织物利用了物质氧化性 | |
| B. | 点燃爆竹后,硫燃烧生成SO2 | |
| C. | 包装用材料聚乙烯和聚氯乙烯都属于烃 | |
| D. | PX项目的主要产品对二甲苯属于不饱和烃 |

 .
. .
.